
5配位化合物与配位平衡ppt课件.ppt

lj****88









亲,该文档总共85页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

5配位化合物与配位平衡ppt课件.ppt
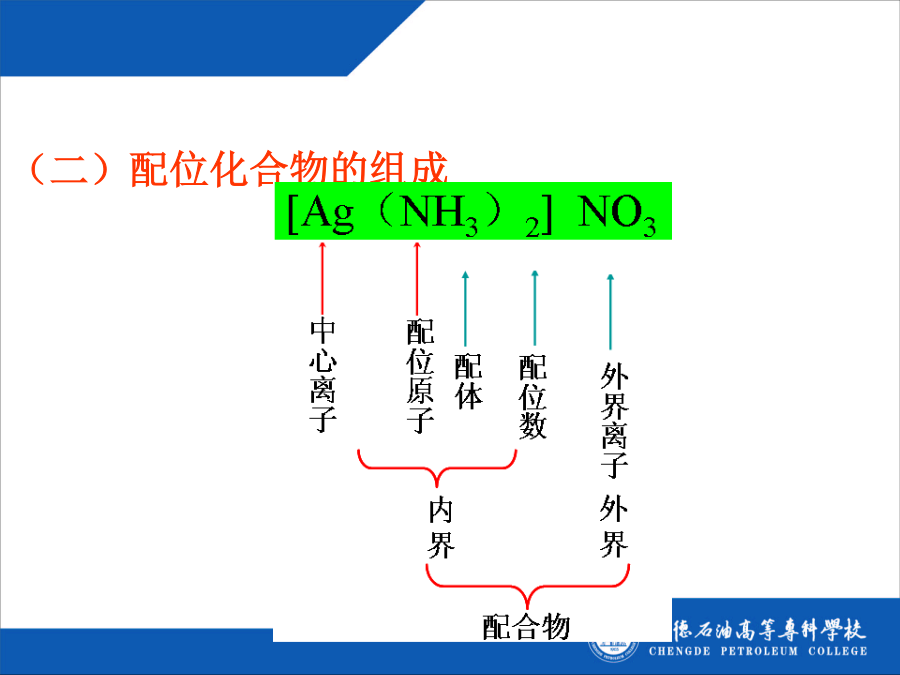
4一配位化合物一配位化合物一配位化合物eg:[Cu(H2O)4]2+eg:H[AuCl4]2配位分子不带电荷的电中性配位化合物。[CoCl3(NH3)3]、[Ni(CO)4]、[Fe(CO)5]等。3配位化合物含有配离子的化合物以及中性配位分子统称为配位化合物,简称配合物。[KAl(SO4)2.12H2O]是复盐而不是配位化合物(二)配位化合物的组成1内界在配合物化学式中用方括号表示内界。配合物的内界能稳定地存在于晶体及水溶液中。它是配合物的特征部分,由中心离子与配体结合而成,它的结构和性质与其他离子不同

5配位化合物与配位平衡.ppt
4一配位化合物一配位化合物一配位化合物eg:[Cu(H2O)4]2+eg:H[AuCl4]2配位分子不带电荷的电中性配位化合物。[CoCl3(NH3)3]、[Ni(CO)4]、[Fe(CO)5]等。3配位化合物含有配离子的化合物以及中性配位分子统称为配位化合物,简称配合物。[KAl(SO4)2.12H2O]是复盐而不是配位化合物(二)配位化合物的组成1内界在配合物化学式中用方括号表示内界。配合物的内界能稳定地存在于晶体及水溶液中。它是配合物的特征部分,由中心离子与配体结合而成,它的结构和性质与其他离子不同

配位化合物与配位平衡.pptx
1、日常生活中:蓝墨水渍、铁锈,可以用草酸洗去,原因在于草酸与Fe3+形成了Fe(C2O4)33-配合物;2、定影剂2S2O32-+AgBrAg(S2O3)23-;3、叶绿素为Mg的配合物;4、与生命有关的:人体中输氧的血红素―铁配合物;起血凝作用的为钙的配合物;5、已证实多种顺铂([PtCl2(NH3)2])及其一些类似物对子宫癌、肺癌有明显疗效。1.熟悉配位化合物的基本概念、组成和命名;1相关的定义和命名组成为CoCl3·6NH3的化合物第一次制备出时,人们认为它是由两个简单化合物(CoCl3和NH

配位化合物与配位平衡.pptx
第二单元课题4一配位化合物一配位化合物一配位化合物eg:[Cu(H2O)4]2+eg:H[AuCl4]2配位分子不带电荷的电中性配位化合物。[CoCl3(NH3)3]、[Ni(CO)4]、[Fe(CO)5]等。3配位化合物含有配离子的化合物以及中性配位分子统称为配位化合物,简称配合物。[KAl(SO4)2.12H2O]是复盐而不是配位化合物(二)配位化合物的组成1内界在配合物化学式中用方括号表示内界。配合物的内界能稳定地存在于晶体及水溶液中。它是配合物的特征部分,由中心离子与配体结合而成,它的结构和性质与

配位化合物与配位平衡.ppt
第七章配位化合物与配位平衡7.1配合物与螯合物7.2配位平衡及其影响因素7.3配位滴定法7.1配合物与螯合物配离子(Complexion):由配位键结合而成,如Cu(NH3)42+,配合物与复盐的区别:配合物含有配合键。复盐溶于水后均为简单离子,无复杂离子,如明矾KAl(SO4)2·12H2O。阳离子d区、ds区中性原子Fe(CO)5p区的某些金属离子Sn2+、Pb2+、Bi3+等极少数高价非金属Si(Ⅵ)、B(Ⅲ)与中心离子(或原子)以配位键结合的原子提供电子对。N,O,Cl,F,S…表7.1常见的配体
