
一种猪细小病毒病毒样颗粒的纯化方法及其应用.pdf

Ja****23






亲,该文档总共11页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

一种猪细小病毒病毒样颗粒的纯化方法及其应用.pdf
本发明公开了一种猪细小病毒病毒样颗粒的纯化方法及其应用,属于生物制品分离纯化技术领域。该方法包括如下步骤:将表达的猪细小病毒病毒样颗粒的培养物进行澄清,收集上清液并用二乙烯亚胺灭活,以得到半成品;调节半成品的pH值酸性;将调节pH值后的半成品加入到用第一缓冲液平衡过的弱阴离子交换柱中,并用第二缓冲液洗脱弱阴离子交换柱,收集各个出峰组分;用聚丙烯酰胺凝胶电泳确定的各个峰的活性蛋白组分。根据本发明的纯化方法得到的猪细小病毒病毒样颗粒纯度高达90%,回收率高达99%,且该纯化方法利于生产操作,为猪细小病毒杆状病

一种猪圆环病毒3型病毒样颗粒的纯化方法及其应用.pdf
本发明公开了一种猪圆环病毒3型病毒样颗粒的纯化方法及其应用,属于生物制品分离纯化技术领域。本发明将表达猪圆环病毒3型病毒样颗粒的培养物进行澄清,澄清液灭活后调pH以便于挂柱,然后,利用更易于猪圆环病毒3型病毒样颗粒挂柱的MMC(复合阳离子)交换柱进行纯化,利用合适的缓冲液洗脱得到纯化样品。本发明方法得到的猪圆环病毒3型病毒样颗粒的纯度高达90%,回收率高达95%。且本发明方法利于生产操作,为猪圆环病毒3型杆状病毒载体灭活疫苗的制备提供了更加安全可靠的途径。

病毒或病毒样颗粒的纯化方法.pdf
本发明的目的在于提供能够简便地纯化病毒或病毒样颗粒的方法。本发明的病毒或病毒样颗粒的纯化方法包括:使包含上述病毒或病毒样颗粒的液体与包含选自镁、钙及铝中的1种以上元素的水不溶性无机化合物接触的工序。

一种猪圆环病毒3型病毒样颗粒及其构建方法和应用.pdf
本发明涉及一种猪圆环病毒3型病毒样颗粒及其构建方法和应用,属于病毒样颗粒制备技术领域。本发明提供了一种重组质粒,所述重组质粒以pSMA质粒作为基础载体,插入优化好的Cap全长基因,所述优化好的Cap全长基因的核苷酸序列如SEQIDNO.1所示。本发明克服了现有真核表达系统及传统原核表达系统的不足,使利用原核表达系统可溶性表达猪圆环病毒3型完整Cap蛋白并成功实现病毒样颗粒的制备方法成为可能,且得到的病毒样颗粒免疫原性高,成本低。
一种猪瘟病毒病毒样颗粒疫苗的制备方法及应用.pdf
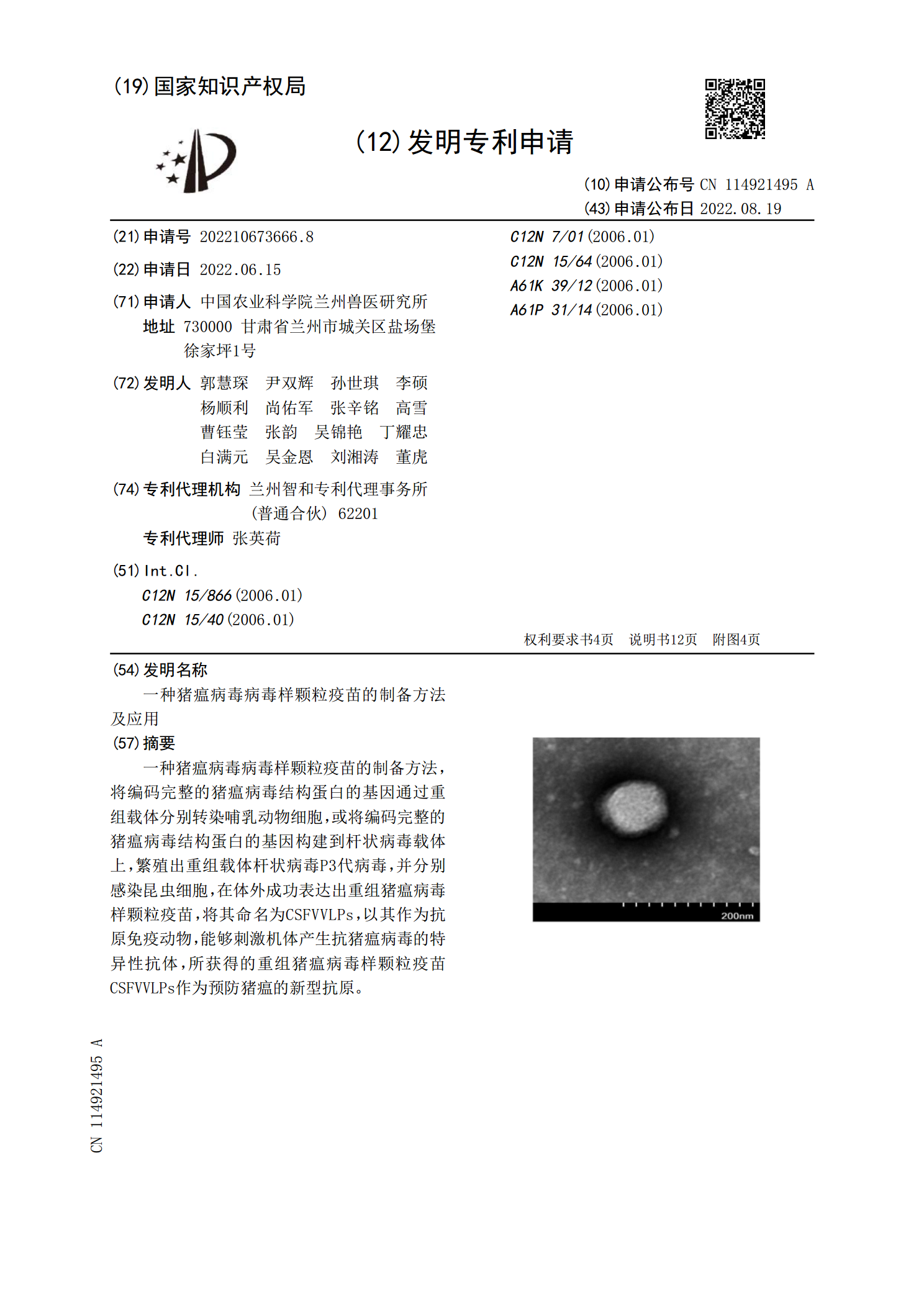
一种猪瘟病毒病毒样颗粒疫苗的制备方法,将编码完整的猪瘟病毒结构蛋白的基因通过重组载体分别转染哺乳动物细胞,或将编码完整的猪瘟病毒结构蛋白的基因构建到杆状病毒载体上,繁殖出重组载体杆状病毒P3代病毒,并分别感染昆虫细胞,在体外成功表达出重组猪瘟病毒样颗粒疫苗,将其命名为CSFVVLPs,以其作为抗原免疫动物,能够刺激机体产生抗猪瘟病毒的特异性抗体,所获得的重组猪瘟病毒样颗粒疫苗CSFVVLPs作为预防猪瘟的新型抗原。
