
结核分枝杆菌融合蛋白LT29构建及其表达纯化方法和应用.pdf

努力****弘毅









亲,该文档总共25页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料
结核分枝杆菌融合蛋白LT29构建及其表达纯化方法和应用.pdf
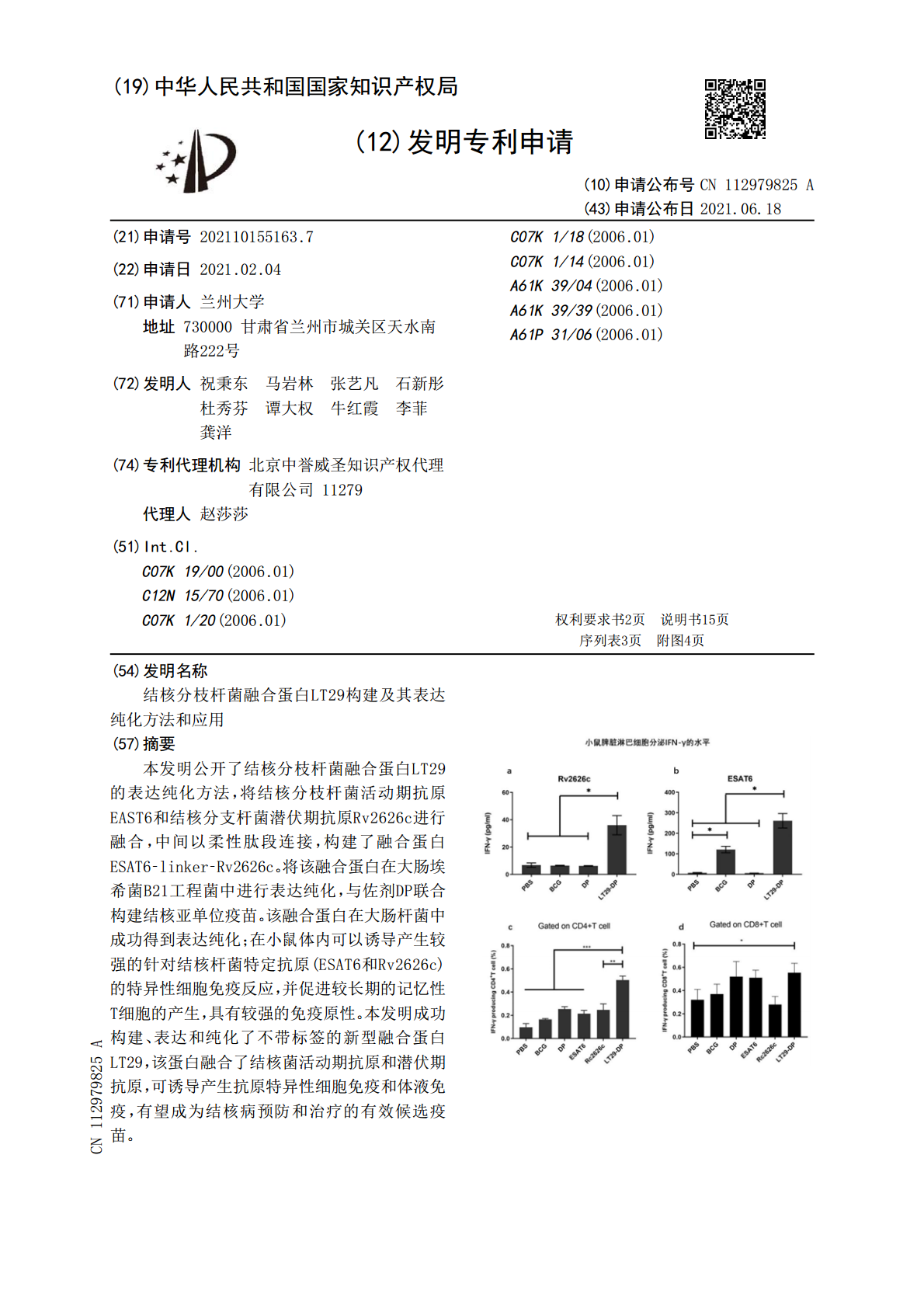
本发明公开了结核分枝杆菌融合蛋白LT29的表达纯化方法,将结核分枝杆菌活动期抗原EAST6和结核分支杆菌潜伏期抗原Rv2626c进行融合,中间以柔性肽段连接,构建了融合蛋白ESAT6‑linker‑Rv2626c。将该融合蛋白在大肠埃希菌B21工程菌中进行表达纯化,与佐剂DP联合构建结核亚单位疫苗。该融合蛋白在大肠杆菌中成功得到表达纯化;在小鼠体内可以诱导产生较强的针对结核杆菌特定抗原(ESAT6和Rv2626c)的特异性细胞免疫反应,并促进较长期的记忆性T细胞的产生,具有较强的免疫原性。本发明成功构建、

结核分枝杆菌融合蛋白BfrB-GrpE及制备方法和应用.pdf
本发明公开了结核分枝杆菌融合蛋白BfrB‑GrpE及制备方法和应用,该结核分枝杆菌融合蛋白BfrB‑GrpE,由结核分枝杆菌复制和休眠期免疫优势抗原BfrB和休眠期免疫优势抗原GrpE联合构建而成;本发明利用基因工程技术,成功构建、表达和纯化了不带有任何标签的结核分枝杆菌融合蛋白BG,解决了融合蛋白所带有的标签可能会影响到动物实验以及后期临床试验的后续问题,并且通过盐析与疏水层析相结合的方法使该无标签融合蛋白得到了有效的纯化;而且其具有表达产量高,表达稳定,对温度及盐离子浓度不敏感且在上清表达等优点,能进

一种人结核分枝杆菌融合蛋白及其应用.pdf
本发明公开了一种人结核分枝杆菌融合蛋白及其应用。该融合蛋白同时包含ESAT6/CFP10/TB7.7多肽序列,因而命名为融合蛋白ect。该融合蛋具有刺激人T细胞释放γ-干扰素(IFN-γ)的能力。应用融合蛋白ect可以检测活动性结核病和潜伏性结核感染者,并能排除卡介苗(BCG)接种者。

人BAF45D融合蛋白表达和纯化方法及应用.pdf
本发明公开了一种人BAF45D融合蛋白表达和纯化方法及应用,包括:构建人BAF45D原核表达载体,获得重组质粒pGEX‑5X‑1‑BAF45D;GST‑BAF45D融合蛋白的原核表达:将所述重组质粒pGEX‑5X‑1‑BAF45D转入Rosetta(DE3)大肠杆菌,经IPTG诱导表达,获得菌体沉淀;破碎细菌,收集上清;GST‑BAF45D融合蛋白的纯化:将经过原核表达获得的上清经GSTResin离心纯化。该方法可实现菌体的高效表达,并获得高活性的GST‑BAF45D融合蛋白,从而能够将其与人胚胎干细胞

浅谈重组结核分枝杆菌Mr-38-000蛋白的表达、纯化和鉴定.docx
浅谈重组结核分枝杆菌Mr38000蛋白的表达、纯化和鉴定摘要从H37Rv基因组中扩增Mr38000蛋白基因并高效表达和纯化。用PCR技术从结核分枝杆菌H37Rv基因组中扩增Mr38000蛋白序列,将其与pGEM-T-Easy载体连接转化DH5α,构建重组克隆载体pGEM-T-Easy/Mr38000,测序正确后将目的基因片断克隆入pQE-80L原核表达载体并转化DH5α,IPTG诱导目的蛋白表达。经Western-blot鉴定目的基因与(His)6融合表达,将已表达的蛋白质通过Ni-NTA亲和色谱柱进行纯
