
(新课改省份专版)高考化学一轮复习 8.2 理解层面 元素周期表、元素周期律学案(含解析)-人教版高三全册化学学案.doc

春景****23






亲,该文档总共15页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料
(新课改省份专版)高考化学一轮复习 8.2 理解层面 元素周期表、元素周期律学案(含解析)-人教版高三全册化学学案.doc
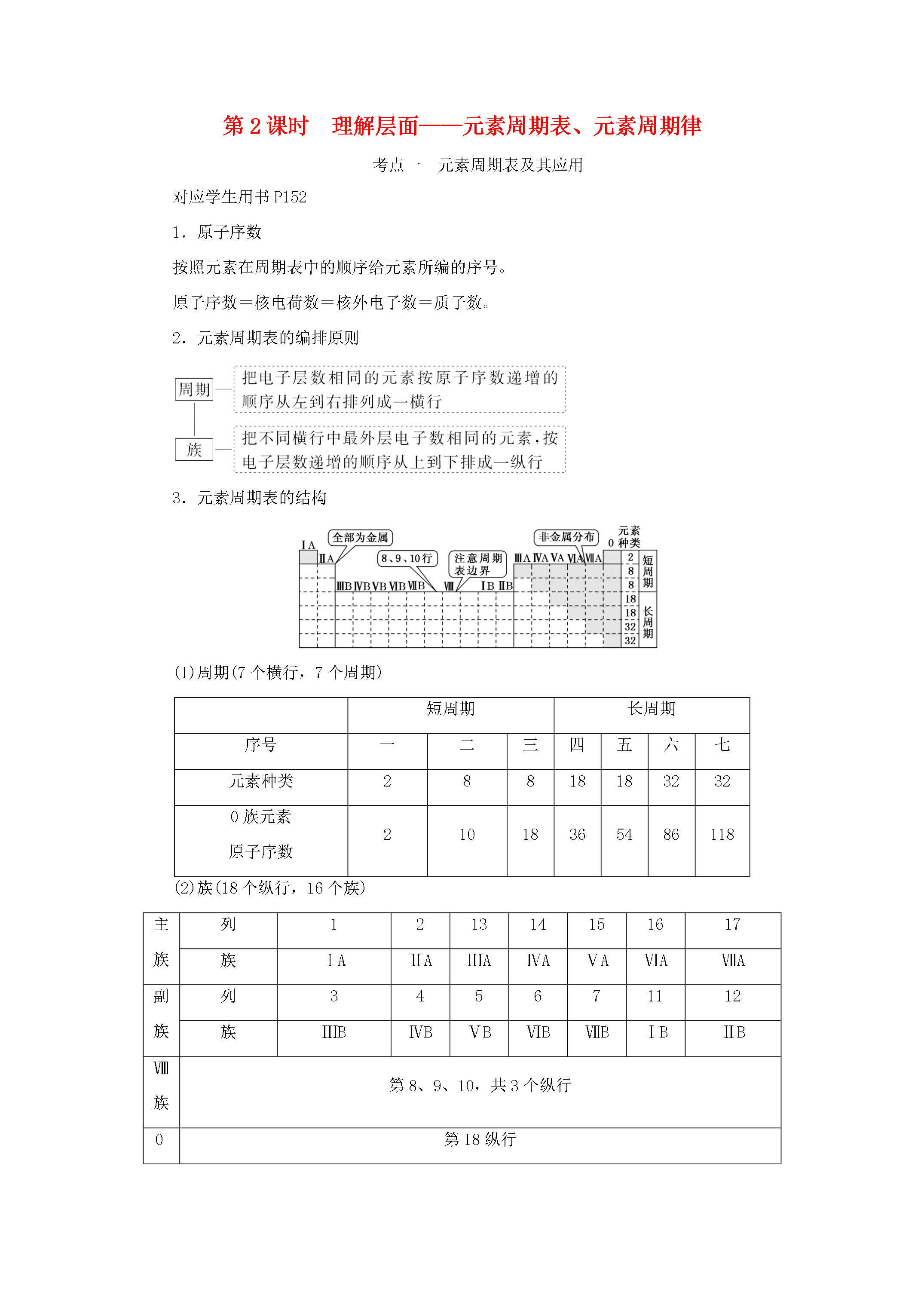
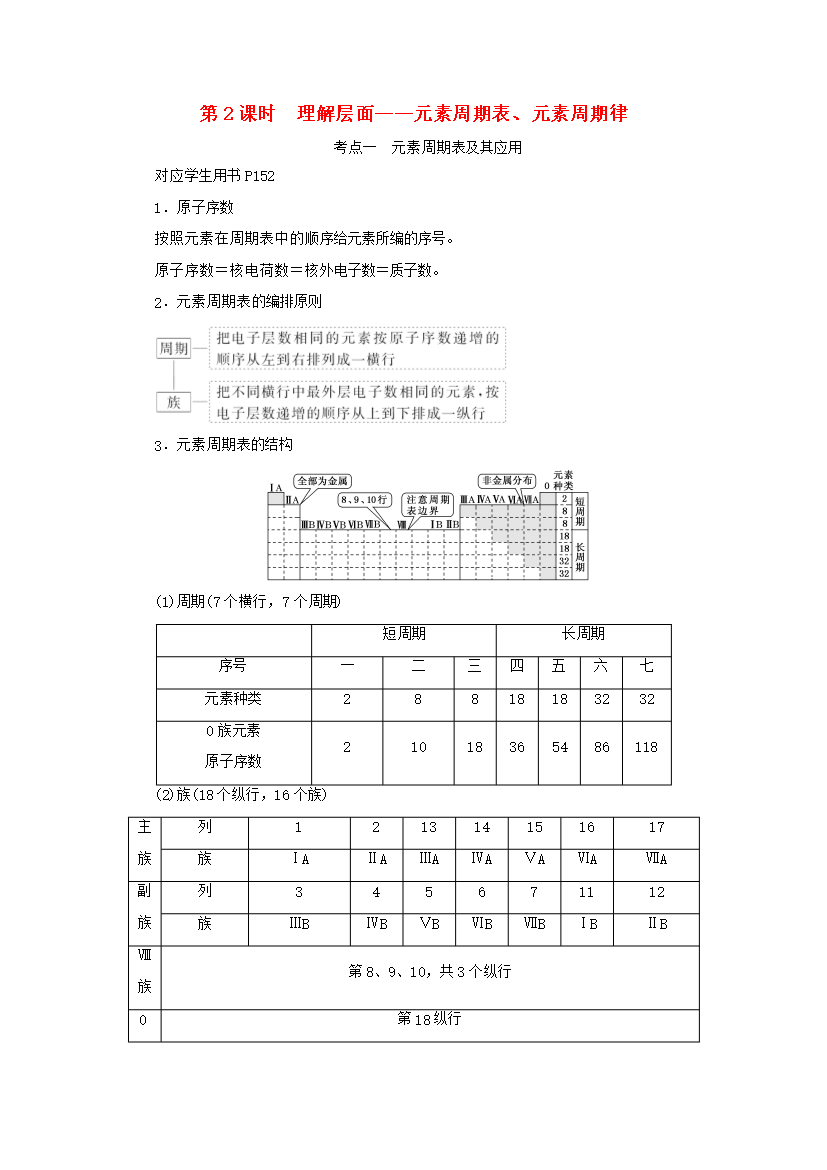
第2课时理解层面——元素周期表、元素周期律考点一元素周期表及其应用对应学生用书P1521.原子序数按照元素在周期表中的顺序给元素所编的序号。原子序数=核电荷数=核外电子数=质子数。2.元素周期表的编排原则3.元素周期表的结构(1)周期(7个横行7个周期)短周期长周期序号一二三四五六七元素种类288181832320族元素原子序数21018365486118(2)族(18个纵行16个族)主族列121314151617族ⅠAⅡAⅢAⅣAⅤAⅥAⅦA副族列345671112族ⅢBⅣBⅤBⅥBⅦBⅠBⅡB

(新课改省份专版)高考化学一轮复习 8.4 认识层面 晶体结构与性质学案(含解析)-人教版高三全册化学学案.doc
第4课时认识层面——晶体结构与性质知识点一晶体和晶胞1.晶体与非晶体(1)晶体与非晶体的区别比较晶体非晶体结构特征结构粒子周期性有序排列结构粒子无序排列性质特征自范性有无熔点固定不固定异同表现各向异性各向同性二者区别方法间接方法测定其是否有固定的熔点科学方法对固体进行X射线衍射实验(2)获得晶体的三条途径①熔融态物质凝固。②气态物质冷却不经液态直接凝固(凝华)。③溶质从溶液中析出。2.晶胞(1)概念:晶胞是描述晶体结构的基本单元。(2)晶体中晶胞的排列——无隙并置①无隙:相邻晶胞之间没有任何间隙。②并置
(新课改省份专版)高考化学一轮复习 8.3 认识层面 分子结构与性质学案(含解析)-人教版高三全册化学学案.doc
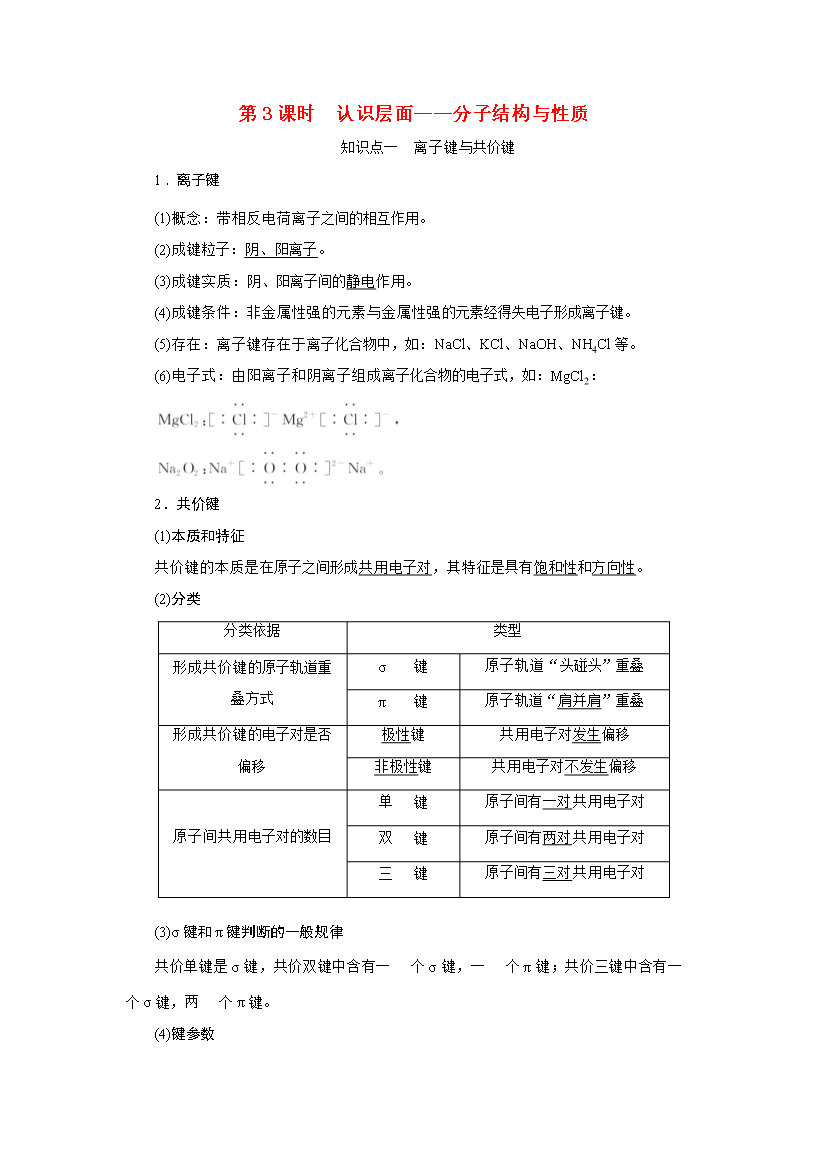
第3课时认识层面——分子结构与性质知识点一离子键与共价键1.离子键(1)概念:带相反电荷离子之间的相互作用。(2)成键粒子:阴、阳离子。(3)成键实质:阴、阳离子间的静电作用。(4)成键条件:非金属性强的元素与金属性强的元素经得失电子形成离子键。(5)存在:离子键存在于离子化合物中如:NaCl、KCl、NaOH、NH4Cl等。(6)电子式:由阳离子和阴离子组成离子化合物的电子式如:MgCl2:2.共价键(1)本质和特征共价键的本质是在原子之间形成共用电子对其特征是具有饱和性和方向性。(2)分类分类依
(新课改省份专版)高考化学一轮复习 8.3 认识层面 分子结构与性质学案(含解析)-人教版高三全册化学学案.doc
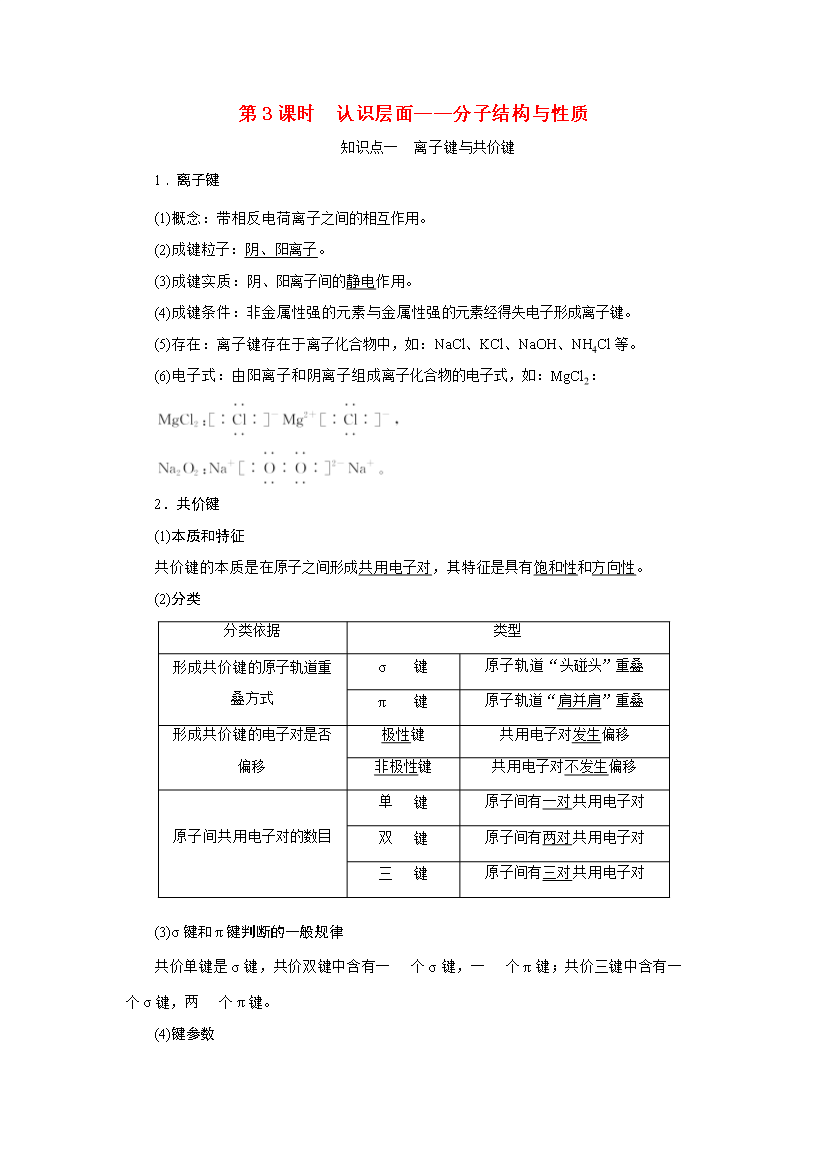
第3课时认识层面——分子结构与性质知识点一离子键与共价键1.离子键(1)概念:带相反电荷离子之间的相互作用。(2)成键粒子:阴、阳离子。(3)成键实质:阴、阳离子间的静电作用。(4)成键条件:非金属性强的元素与金属性强的元素经得失电子形成离子键。(5)存在:离子键存在于离子化合物中如:NaCl、KCl、NaOH、NH4Cl等。(6)电子式:由阳离子和阴离子组成离子化合物的电子式如:MgCl2:2.共价键(1)本质和特征共价键的本质是在原子之间形成共用电子对其特征是具有饱和性和方向性。(2)分类分类依

(新课改省份专版)高考化学一轮复习 8.1 认识层面 原子结构、核外电子排布学案(含解析)-人教版高三全册化学学案.doc
第八章元素周期律物质结构与性质考试要求教学建议1.认识原子结构、元素性质以及元素在元素周期表中位置的关系。2.知道元素、核素的涵义了解原子核外电子的排布。3.知道元素周期表的结构以第三周期的钠、镁、铝、硅、磷、硫、氯以及碱金属和卤族元素为例了解主族元素性质的递变规律。4.认识物质是由原子、离子、分子等微粒构成的微粒之间存在不同类型的相互作用。5.认识离子键、共价键的本质。6.认识分子间存在相互作用知道范德华力和氢键是两种常见的分子间作用力了解分子内氢键和分子间氢键在自然界中的广泛存在及重要作用。7.认
