
(讲练测)高考化学一轮复习 专题6.3 化学键(讲)(含解析)-人教版高三全册化学教案.doc

一条****发啊









亲,该文档总共11页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

(讲练测)高考化学一轮复习 专题6.3 化学键(讲)(含解析)-人教版高三全册化学教案.doc
专题6.3化学键1、了解化学键的定义。2、了解离子键、共价键的形成。3、了解化学键与化学反应的关系。一、化学键1.化学键的概念与分类(1)概念:相邻原子间的强相互作用。(2)分类根据形成过程不同化学键可分为离子键和共价键。2.离子键(1)概念:带有相反电荷的阴、阳离子之间的强烈的相互作用(2)成键粒子:阴、阳离子。(3)成键实质:静电作用。(4)形成条件:通常是活泼金属与活泼非金属元素的原子相结合。(5)表示方法①用电子式表示离子化合物的形成过程Na2S:;CaCl2:。②写出下列物质的电子式
(讲练测)高考化学一轮复习 专题11.2 物质的检验(讲)(含解析)-人教版高三全册化学教案.doc
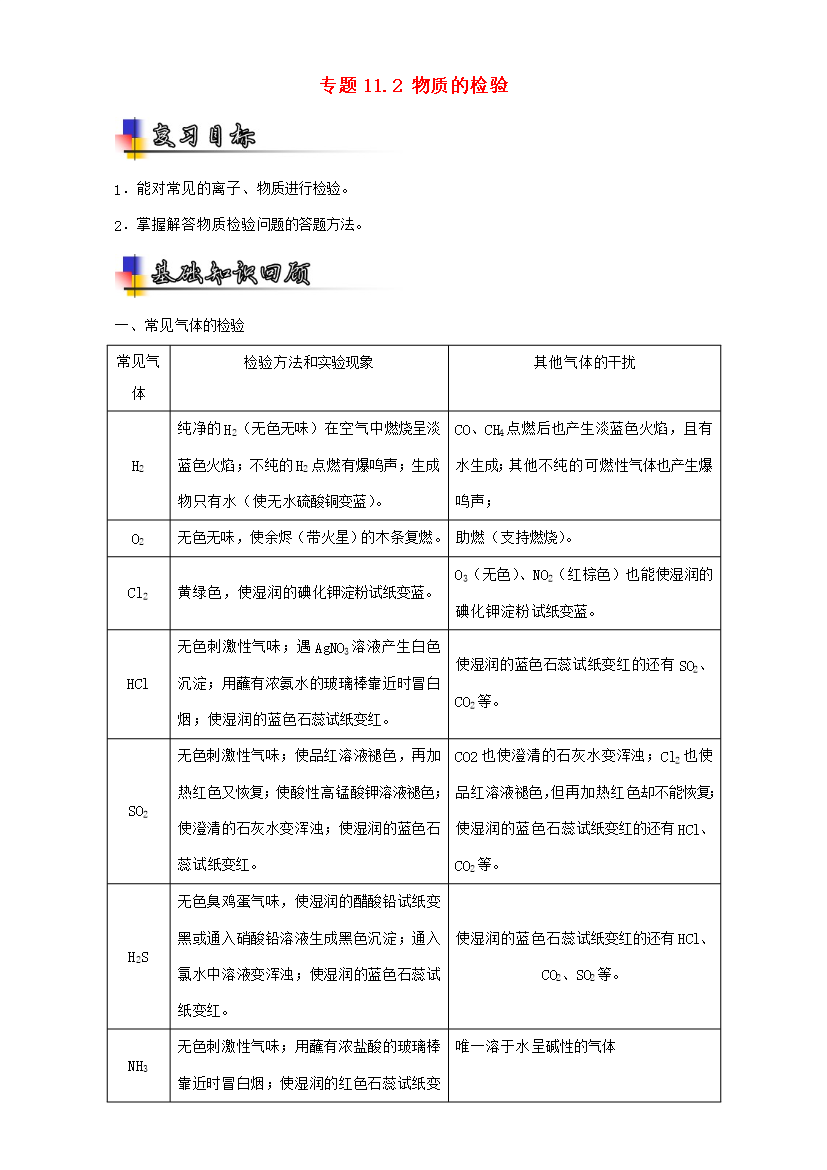
专题11.2物质的检验1.能对常见的离子、物质进行检验。2.掌握解答物质检验问题的答题方法。一、常见气体的检验常见气体检验方法和实验现象其他气体的干扰H2纯净的H2(无色无味)在空气中燃烧呈淡蓝色火焰;不纯的H2点燃有爆鸣声;生成物只有水(使无水硫酸铜变蓝)。CO、CH4点燃后也产生淡蓝色火焰且有水生成;其他不纯的可燃性气体也产生爆鸣声;O2无色无味使余烬(带火星)的木条复燃。助燃(支持燃烧)。Cl2黄绿色使湿润的碘化钾淀粉试纸变蓝。O3(无色)、NO2(红棕色)也能使湿润的碘化钾淀粉试纸变蓝。HCl无

(讲练测)高考化学一轮复习 专题4.5 氨和铵盐(讲)(含解析)-人教版高三全册化学教案.doc
专题4.5氨和铵盐1、掌握氨及铵盐的性质及用途、2、掌握NH4+的检验。2、掌握氨的实验室制法。3、初步了解常见化肥。一、氨1、物理性质氨气是无色有刺激性气味的气体易液化可作制冷剂常温、常压下1体积的水可溶解700体积的氨气。液氨与氨水的区别液氨氨水形成氨气液化氨气溶于水物质分类纯净物混合物微粒种类NH3NH3、NH3·H2O、H+、H2O、NH4+、OH-存在条件常温常压下不能存在常温常压下可存在2、分子结构电子式:空间结构:三角锥形。3、氨的化学性质(1)与水的反应

(讲练测)高考化学一轮复习 专题11.3 物质的分离与提纯(讲)(含解析)-人教版高三全册化学教案.doc
专题11.3物质的分离与提纯能对常见的物质进行分离和提纯。掌握过滤、分液、蒸馏等操作的步骤及要求。一、物质分离、提纯的常用物理方法1、物质分离、提纯的区别(1)物质的分离将混合物的各组分分离开来获得几种纯净物的过程。(2)物质的提纯将混合物中的杂质除去而得到纯净物的过程又叫物质的净化或除杂。2、物质分离、提纯的常用物理方法图1图2图3图4图5(1)如图1方法、装置的名称:过滤。适用范围:把不溶性固

(讲练测)高考化学一轮复习 专题8.3 化学平衡移动(讲)(含解析)-人教版高三全册化学教案.doc
专题8.3化学平衡移动理解影响化学平衡的因素(浓度、温度、压强、催化剂等)认识其一般规律。理解化学平衡常数的定义并能进行简单计算。能正确分析化学平衡图像。一、化学平衡移动1、概念可逆反应达到平衡状态以后若反应条件(如温度、压强、浓度等)发生了变化平衡混合物中各组分的浓度也会随之改变从而在一段时间后达到新的平衡状态。这种由原平衡状态向新平衡状态的变化过程叫做化学平衡的移动。2、过程3、平衡移动方向与反应速率的关系(1)v正>v逆平衡向正反应方向移动。(2)v正=v逆平衡不移动。(3)
