
高考化学实验专题8:实验设计评价.doc

山柳****魔王










亲,该文档总共12页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

高考化学实验专题8:实验设计评价.doc
高考化学实验专题8:实验设计评价I.基本要求了解化学实验是科学探究过程中的一种重要方法。能根据实验试题要求.做到:1.设计、评价或改进实验方案。2.了解控制实验条件的方法。3.分析或处理实验数据,得出合理结论。4.绘制和识别典型的实验仪器装置图。II.基本内容1.化学实验方案设计的一般步骤:化学实验方案设计物质的制备实验方案设计物质的性质实验方案设计物质的检验实验方案设计综合性实验方案设计实验目的→实验原理→方案设计→仪器选择与组装→实验操作→实验现象与数据记录→数据处理与分析→实验报告。2.化学实验方案

高考化学实验设计与评价专题演练.doc
高考化学实验设计与评价专题演练2019从开始用火的原始社会到使用各种人造物质的现代社会人类都在享用化学成果。查字典化学网为大家推荐了高考化学实验设计与评价专题演练请大家仔细阅读希望你喜欢。1.玻璃棒是化学实验中常用的仪器其作用是用于搅拌、过滤或转移液体时引流。下列有关实验过程中一般不需要使用玻璃棒进行操作的是()①用pH试纸测定Na2CO3溶液的pH②从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl③实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀④用

高考化学实验专题复习实验设计的评价 人教版.rar
实验设计的评价考试大纲中的实验能力(1)用正确的化学实验基本操作,完成规定的“学生实验”的能力。(2)观察记录实验现象,分析实验结果和处理实验数据,得出正确结论的能力。(3)初步处理实验过程中的有关安全问题的能力。(4)能识别和绘制典型的实验仪器装置图的能力。(5)根据实验试题的要求,设计或评价简单实验方案的能力。透视高考:1、(03上海、04天津)实验室制备氨气,下列方法中适宜选用的是()2、(2004上海)CuS和Cu2S都能溶于硝酸,它们高温灼烧的产物相同,以下鉴别CuS和Cu2S两种黑色粉末的方法

2008高考化学专题复习17 化学实验设计与评价.doc
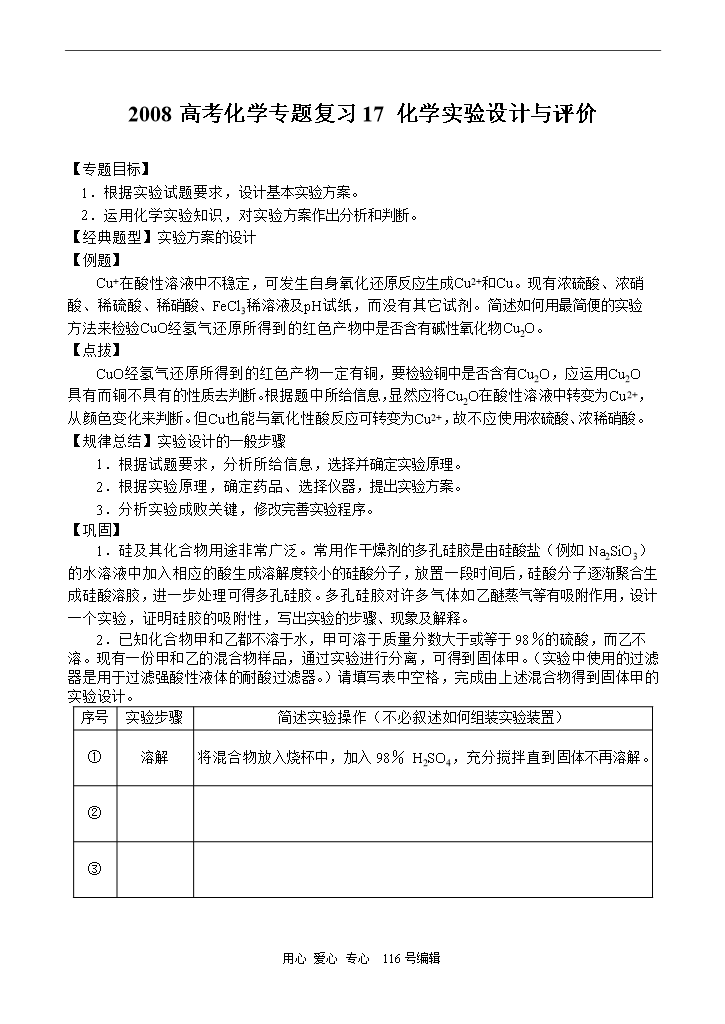
用心爱心专心116号编辑2008高考化学专题复习17化学实验设计与评价【专题目标】1.根据实验试题要求,设计基本实验方案。2.运用化学实验知识,对实验方案作出分析和判断。【经典题型】实验方案的设计【例题】Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu。现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸,而没有其它试剂。简述如何用最简便的实验方法来检验CuO经氢气还原所得到的红色产物中是否含有碱性氧化物Cu2O。【点拔】CuO经氢气还原所得到的红色产物一定有铜,要检验铜中是否
2008高考化学专题复习17 化学实验设计与评价.doc
用心爱心专心116号编辑2008高考化学专题复习17化学实验设计与评价【专题目标】1.根据实验试题要求设计基本实验方案。2.运用化学实验知识对实验方案作出分析和判断。【经典题型】实验方案的设计【例题】Cu+在酸性溶液中不稳定可发生自身氧化还原反应生成Cu2+和Cu。现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸而没有其它试剂。简述如何用最简便的实验方法来检验CuO经氢气还原所得到的红色产物中是否含有碱性氧化物Cu2O。【点拔】CuO经氢气还原所得到的红色产物一定有铜要检验铜中是否
