
药物对肝脏的毒性作用专家讲座.pptx

王子****青蛙









亲,该文档总共41页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

药物对肝脏的毒性作用专家讲座.pptx
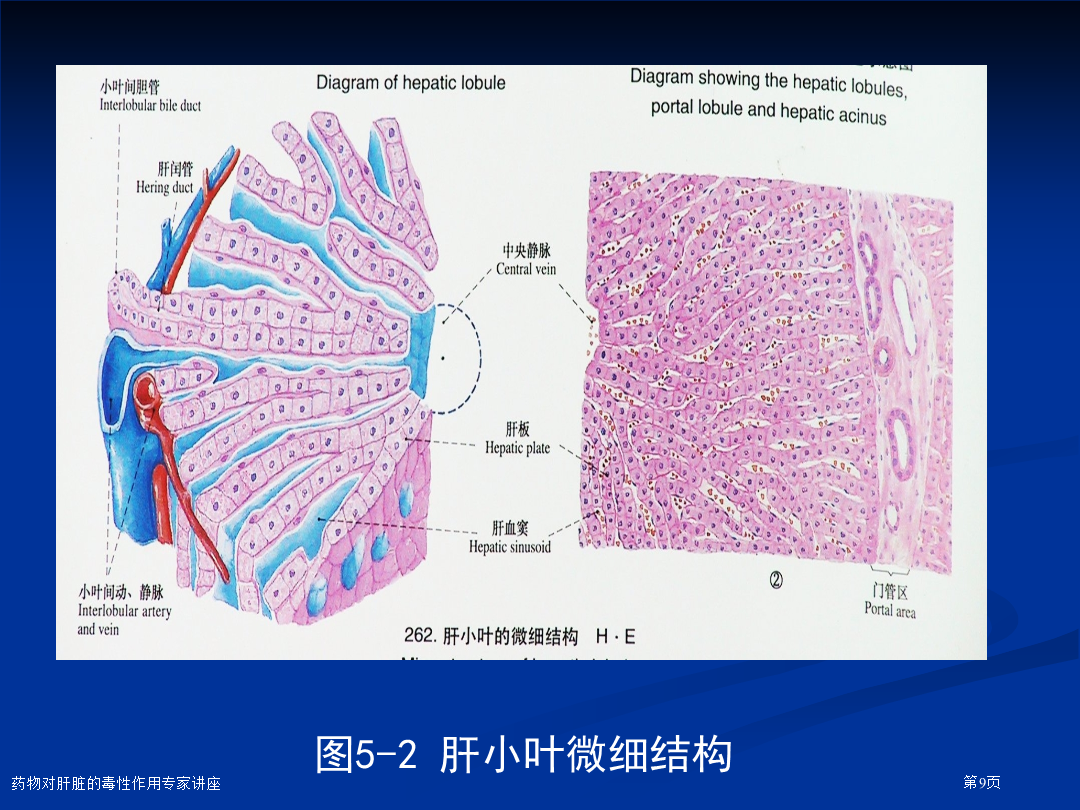
第五章药品对肝脏毒性作用一、肝脏损伤生理学与形态学基础(一)肝脏血液循环(二)肝脏功效1)消化与吸收功效2)代谢功效3)去除功效4)解毒与排泄功效表5-1肝脏主要功效及功效障碍后果肝小叶三区(图5-3)小叶中心区:毒性化学物主要靶位带中区门周区肝腺泡三带(图5-3)1带:与血液入口相邻(≈门周区)2带3带:与中央静脉相邻(≈小叶中心区)图5-1肝小叶模式图图5-2肝小叶微细结构腺泡分带现象1)肝细胞各组分水平沿腺泡分带呈浓度梯度分布肝细胞中氧浓度:1带>2带>3带;胆盐浓度:1带>2带>3带2)肝细胞蛋白

药物对肝脏的毒性作用专家讲座.pptx
第五章药品对肝脏毒性作用一、肝脏损伤生理学与形态学基础(一)肝脏血液循环(二)肝脏功效1)消化与吸收功效2)代谢功效3)去除功效4)解毒与排泄功效表5-1肝脏主要功效及功效障碍后果肝小叶三区(图5-3)小叶中心区:毒性化学物主要靶位带中区门周区肝腺泡三带(图5-3)1带:与血液入口相邻(≈门周区)2带3带:与中央静脉相邻(≈小叶中心区)图5-1肝小叶模式图图5-2肝小叶微细结构腺泡分带现象1)肝细胞各组分水平沿腺泡分带呈浓度梯度分布肝细胞中氧浓度:1带>2带>3带;胆盐浓度:1带>2带>3带2)肝细胞蛋白

药物对肝脏的毒性作用.pptx
第三章药品对肝脏毒性作用第一节肝脏结构、功效与毒性关系(一)肝小叶hepaticlobule肝基本结构单位图肝小叶微细结构胆小管(bilecanaliculi)(镀银法)肝脏特点肝脏主要生理功效1、代谢功效第二节肝脏毒物分类和特点第二节肝脏毒物分类及特点第二节肝脏毒物分类及特点第二节肝脏毒物分类及特点第二节肝脏毒物分类及特点第二节肝脏毒物分类及特点肝脏毒物评价标准分类所属类别所属类别第三节药品引发肝损害类型及机理第三节药品引发肝损害类型及机理肝损害类型药品性肝损害机理二、药品性肝损害机理死亡模式引发肝坏死

3药物对肝脏的毒性作用.pptx
第三章一、肝脏损伤的组织形态学与生理学基础肝的脏面肝脏的超微结构肝小叶模式图猪肝中央静脉肝板(肝索)肝细胞肝血窦窦周隙(Disse隙)胆小管肝门管区肝腺泡(Hepaticacinus):相邻两个肝小叶之间的小叶间动脉、小叶间静脉和小叶间胆管发出的终末支为中轴两对角为中央静脉构成的椭圆形柱状体是肝的最小功能单位。肝小叶与肝腺泡示意图解剖学概念1.肝小叶三区小叶中心区:毒性化学物的主要靶位带中区门周区(外周小叶)2.肝腺泡三带1带:与血液入口相邻(≈门周区)2带:过渡区

药物对肝脏的毒性作用ppt课件.ppt
第三章药物对肝脏的毒性作用第一节肝脏的结构、功能与毒性关系(一)肝小叶hepaticlobule肝的基本结构单位图肝小叶微细结构胆小管(bilecanaliculi)(镀银法)肝脏的特点肝脏的主要生理功能1、代谢功能第二节肝脏毒物的分类和特点第二节肝脏毒物的分类及特点第二节肝脏毒物的分类及特点第二节肝脏毒物的分类及特点第二节肝脏毒物的分类及特点第二节肝脏毒物的分类及特点肝脏毒物的评价标准分类所属类别所属类别第三节药物引起的肝损害类型及机理第三节药物引起的肝损害类型及机理肝损害类型药物性肝损害机理二、药物性
