
物理化学(00001)市公开课一等奖百校联赛特等奖课件.pptx

胜利****实阿








亲,该文档总共79页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

物理化学(00001)市公开课一等奖百校联赛特等奖课件.pptx
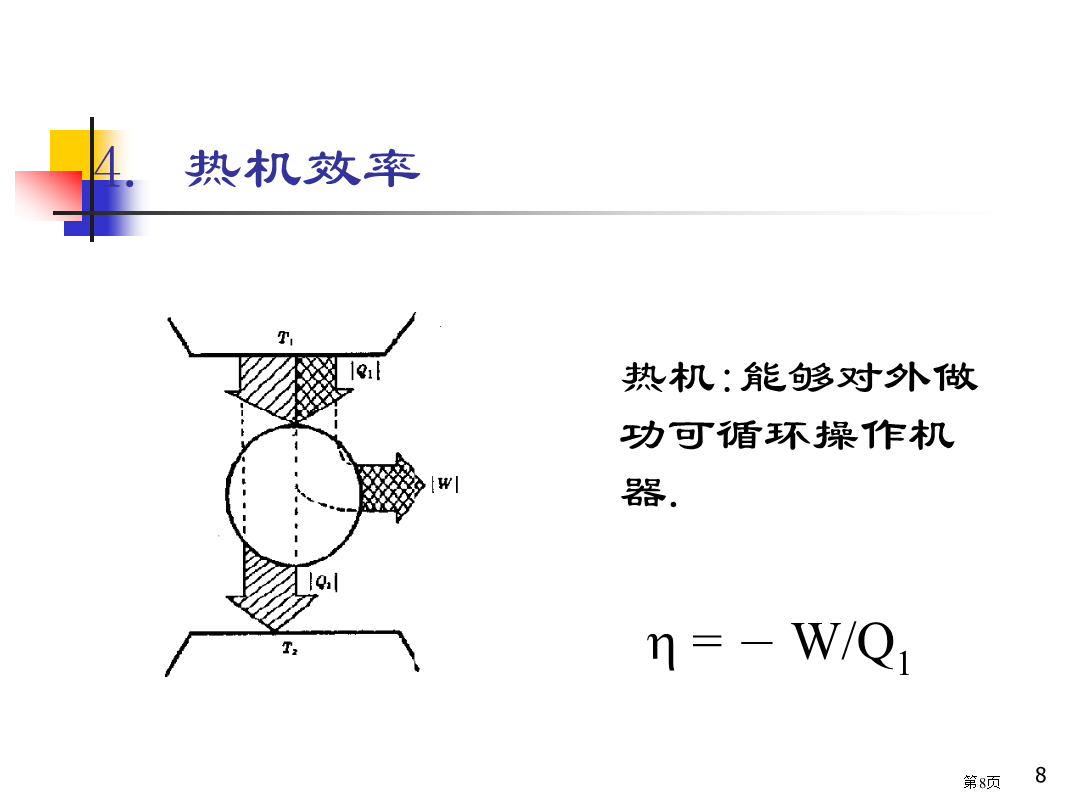
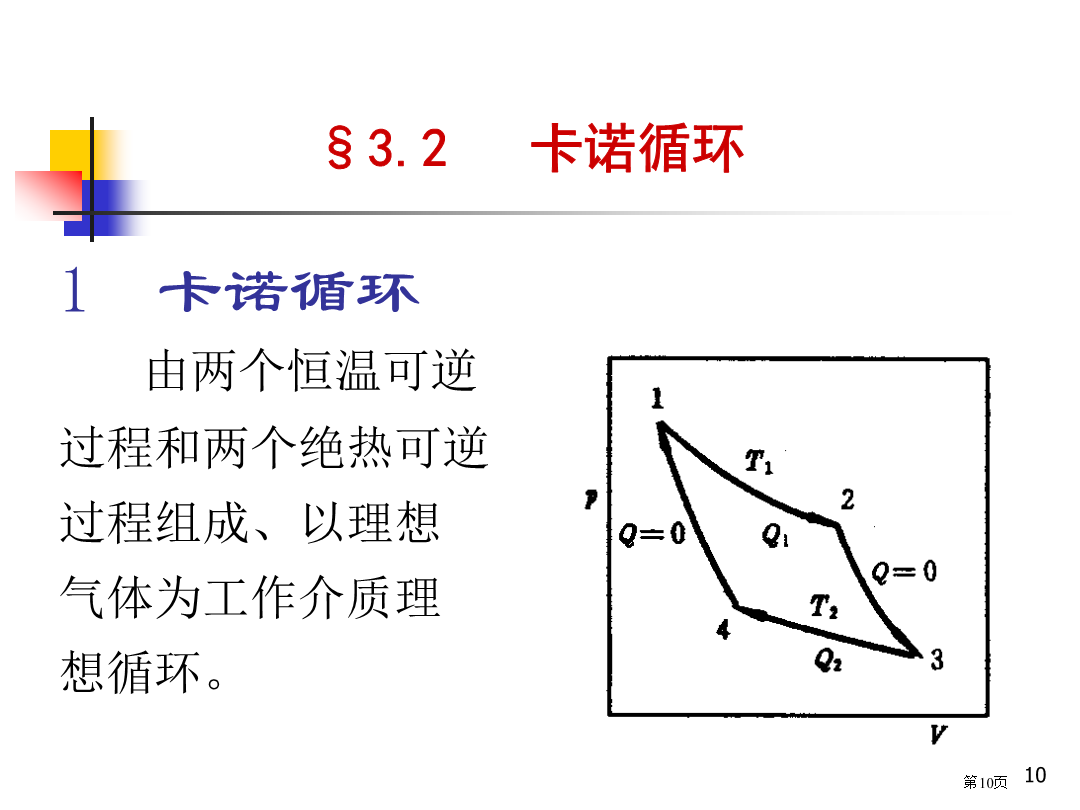
第三章热力学第二定律Chapter3theSecondLowofThermodynamics主要内容定义:自动发生改变,即无需外力帮忙,任其自然,不去管它,即可发生改变。(1)水从高往低处流,它逆过程水从低往高处流不会自动进行。(3)锌片投入硫酸铜溶液引发置换反应,它逆过程也不会自动发生。等等……2.自发过程逆向进行环境必须对系统做功1)自发过程是热力学不可逆过程。4.热机效率5.热力学第二定律1卡诺循环由两个恒温可逆过程和两个绝热可逆过程组成、以理想气体为工作介质理想循环。(1)等温可逆膨胀经一循环后,

生物必修一(00002)(00001)市公开课一等奖百校联赛特等奖课件.pptx
第3节ATP主要起源——细胞呼吸1.呼吸作用与物质燃烧有什么共同点?自主学习呼吸作用一、有氧细胞呼吸过程示意图有氧呼吸三个阶段有氧呼吸①主要场所:1.产生[H]阶段是:2.哪个阶段有水生成:3.哪个阶段释放出最多能量:无氧呼吸:普通是指细胞在缺氧条件下,经过酶催化作用,把葡萄糖等有机物分解为不彻底氧化产物,同时释放出少许能量过程。无氧呼吸总反应式无氧呼吸意义:1、呼吸作用能为生物体生命活动提供能量。五、细胞呼吸原理应用1.发酵技术2.农业生产细胞呼吸为植物吸收营养物质、细胞分裂、植株生长和发育等提供能量和

有机化学课件(00001)市公开课一等奖百校联赛特等奖课件.pptx
第八章醛酮醌§1醛、酮概述二、异构2.系统命名法§2醛、酮物理性质§3醛、酮化学性质羰基化合物主要化学性质:例2:丙烯合成α-羟基丁酸2.与亚硫酸氢钠加成α-羟基磺酸钠用稀酸或弱减(如碳酸钠)处理,又可得到原来醛或脂肪族甲基酮。3.与醇加成(4)酮普通不形成半缩酮或缩酮。5.与格氏试剂反应说明(1)利用此反应可制伯、仲、叔醇,较原来羰基化合物增加一个R′,是增碳反应。比如:1.由乙烯(或丙烯)制备2-丁醇2.丙烯制备丁醇6.与氨及氨衍生物反应相当于:①同胺反应③同肼、苯肼、2,4-二硝基苯肼反应④同氨基脲

物理化学实验w市公开课一等奖百校联赛特等奖课件.pptx
物理化学试验试验一、燃烧热测定1.1摩尔物质完全氧化时反应热称为燃烧热,所谓完全氧化是指CCO2(g),H2H2O(l),SSO2(g),而N、卤素、银等元素变为游离状态。如在25oC苯甲酸燃烧热-3226.8kj/mol。C7H6O2(s)+71/2O2(g)→7CO2(g)+3H2O(l)燃烧热可在恒容或恒压情况下测定,由热力学第一定律可知:在不做非膨胀功情况下,恒容燃烧热Qv=Δu,恒压燃烧热Qp=ΔH,在氧弹式量热计中测得燃烧热为Qv,而普通热化学计算用值为Qp,这二者可经过下式进行换算:Qp=Q

历史必修三复习ppt课件(00001)市公开课一等奖百校联赛特等奖课件.pptx
第二单元中国古代文艺长廊甲骨文小篆宋风俗画诗经第二单元中国古代文艺长廊(江苏历史,1)“自楚骚、唐律争妍竞畅,而民间性情之响,遂不得列于诗坛,于是别之曰‘山歌’,言田夫野竖矢口寄兴之所为,荐绅学士家不道也。……山歌虽俚甚矣,独非《郑》、《卫》(国风之篇)之遗欤?”据明代冯梦龙这段话,与山歌相同、能表达“民间性情之响”是()A.《诗经》B.楚辞C.汉赋D.唐诗【考点】古代中国文学时代特征【解析】本题考查知识再现与材料解读能力。依据材料信息“山歌虽俚甚矣,独非《郑》、《卫》(国风之篇)之遗欤?”可知《诗经》中
