
药物不良反应的预警专家讲座.pptx

胜利****实阿








亲,该文档总共80页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

药物不良反应的预警专家讲座.pptx
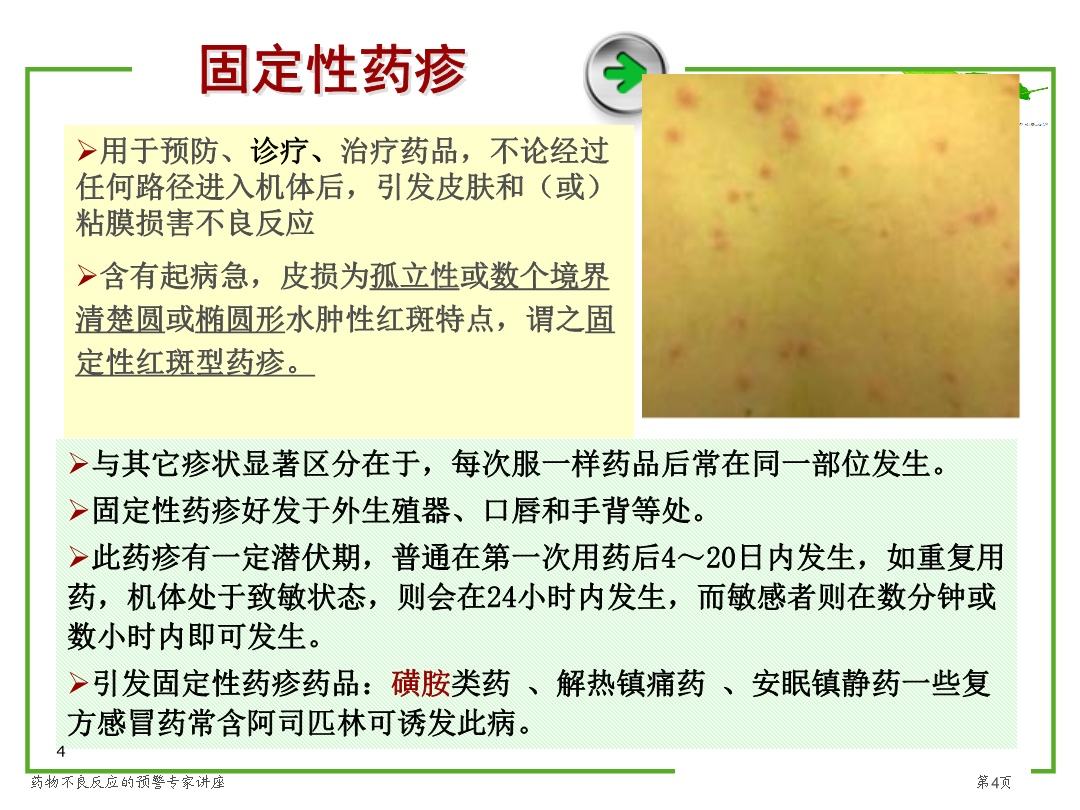
药品不良反应发生率越耒越高药品不良反应处理现实状况和迷惑固定性药疹第一部分含汞药品引发中毒;英格兰、威尔士地域1929~1948年间,死亡585人氨基比林引发严重白细胞降低症;1931~1934年间,仅美国就死亡1981人磺胺酏剂与肾衰;1937年服药后致358人中毒,其中107例死于尿毒症。主要是二甘醇(工业用)在体内经氧化代谢成草酸致肾损害所致。震惊世界“反应停事件”“反应停事件”没有涉及到美国FDA评审教授极力反对将反应停引入美国市场,因为在药品临床前试验中发觉:猴子在怀孕第23到31天内服用反应停

药物不良反应监测和药害事件预警专家讲座.pptx
第三章药品不良反应监测与药害事件预警2024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11/162024/11
药物不良反应培训专家讲座.pptx
药品不良反应adversedrugreactions,ADR药物不良反应(adversedrugreactionsADR)药品不良反应种类与临床表现●特异质反应(idiosyncraticreaction):产生与药品本身药理作用无关反应,系个体异常遗传原因所致药品依赖性(drugdependence)精神依赖性(psychicdependence)身体依赖性(physicaldependence)三致致癌作用(carcinogenesis)致畸作用(teratogenesis)致突变作用(mutagen

药物不良反应监测专家讲座.pptx
药品不良反应监测被反应停夺去胳膊孩子们为何仅有上市前评价是不够?TheRuleofThree(3倍定律)ADR监测系统ADRs监测范围药品不良反应监测方法自发呈报系统黄卡系统(Yellowcardsystem)蓝卡系统(Bluecardsystem)FDA医药产品监测项目(MedWatch)呈报内容基本要求自发呈报基本作用SIGNAL优点:监测范围广,参加人员多不受时间、空间限制是ADR主要信息源自发呈报在ADR监测中地位汇报质量医院集中监测系统(Hospitalintensivemonitoring)医

药物不良反应监测和药害事件预警专业知识培训专家讲座.pptx
第三章药品不良反应监测与药害事件预警2024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/282024/1/28202
