
《高中化学人教版必修2》第二章 化学反应与能量.doc

my****25




在线预览结束,喜欢就下载吧,查找使用更方便
相关资料
新人教版高中化学必修2第二章 化学反应与能量.doc
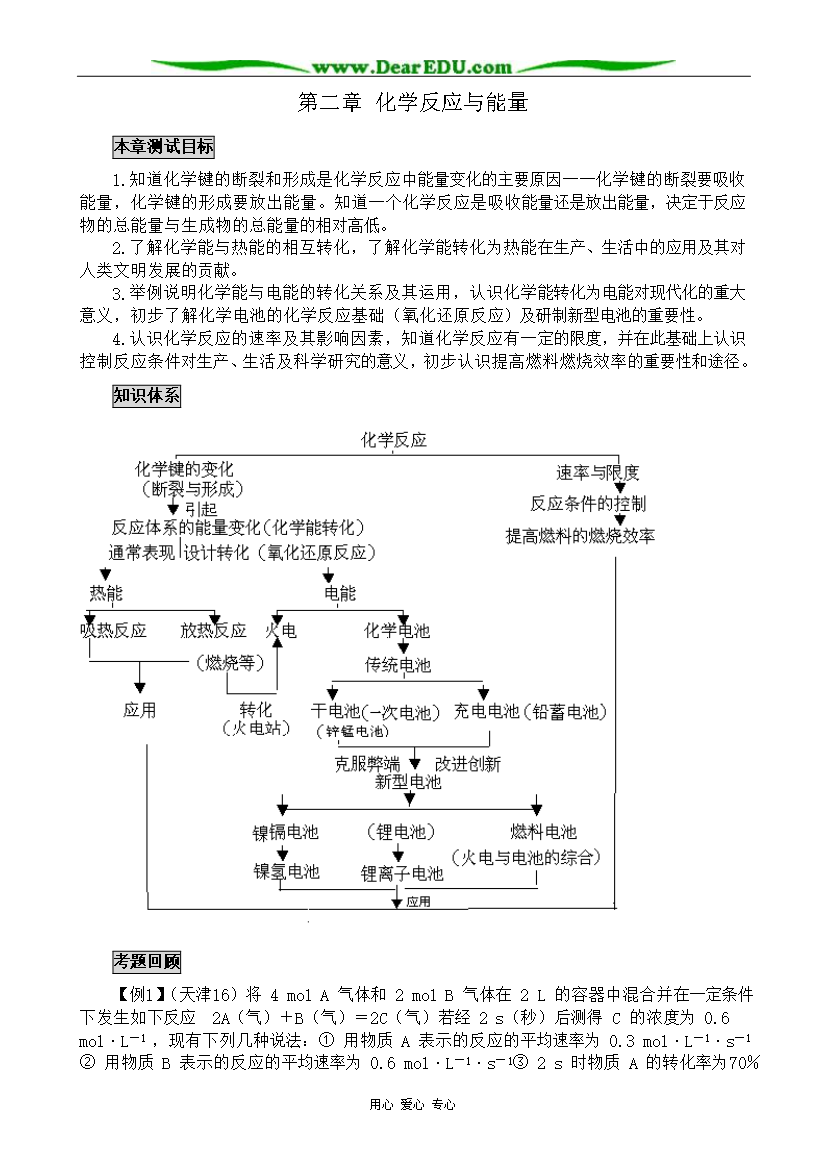
用心爱心专心第二章化学反应与能量本章测试目标1.知道化学键的断裂和形成是化学反应中能量变化的主要原因──化学键的断裂要吸收能量化学键的形成要放出能量。知道一个化学反应是吸收能量还是放出能量决定于反应物的总能量与生成物的总能量的相对高低。2.了解化学能与热能的相互转化了解化学能转化为热能在生产、生活中的应用及其对人类文明发展的贡献。3.举例说明化学能与电能的转化关系及其运用认识化学能转化为电能对现代化的重大意义初步了解化学电池的化学反应基础(氧化还原反应)及研制新型电池的重要性。4.认识化学反应的速率

新人教版高中化学必修2第二章 化学反应与能量.doc
用心爱心专心第二章化学反应与能量本章测试目标1.知道化学键的断裂和形成是化学反应中能量变化的主要原因──化学键的断裂要吸收能量,化学键的形成要放出能量。知道一个化学反应是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对高低。2.了解化学能与热能的相互转化,了解化学能转化为热能在生产、生活中的应用及其对人类文明发展的贡献。3.举例说明化学能与电能的转化关系及其运用,认识化学能转化为电能对现代化的重大意义,初步了解化学电池的化学反应基础(氧化还原反应)及研制新型电池的重要性。4.认识化学反应的

《高中化学人教版必修2》第二章 化学反应与能量.doc
《高中化学人教版必修2》第二章化学反应与能量第三节化学反应速率与限度(课时2)【学习目标】1.了解影响化学反应速率的因素。2.通过实验探究,理解温度和催化剂对化学反应速率的影响。3.认识控制化学反应速率对人类生产、生活的意义。【学习重点】影响化学反应速率的因素。【导学流程】[创设情境]展示图片资料,使学生了解自然界或生产、生活中的化学反应进行有快、慢之分。4.影响化学反应速率的因素(1)内因:由反应物的决定(2)外因:(外界条件对化学反应速率的影响)活动元Ⅰ:温度对化学反应速率影响的探究实验操作试管中均为

高中化学:第二章化学反应与能量 教案 2 新人教版必修2.doc
用心爱心专心第二章化学反应与能量本章说明一、教学目标1.知道化学键的断裂和形成是化学反应中能量变化的主要原因──化学键的断裂要吸收能量,化学键的形成要放出能量。知道一个化学反应是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对高低。2.通过实例和实验,了解化学能与热能的相互转化,了解化学能转化为热能在生产、生活中的应用及其对人类文明发展的贡献。3.能举例说明化学能与电能的转化关系及其运用,认识化学能转化为电能对现代化的重大意义,初步了解化学电池的化学反应基础(氧化还原反应)及

高中化学:第二章化学反应与能量 教案 2 新人教版必修2.doc
用心爱心专心第二章化学反应与能量本章说明一、教学目标1.知道化学键的断裂和形成是化学反应中能量变化的主要原因──化学键的断裂要吸收能量化学键的形成要放出能量。知道一个化学反应是吸收能量还是放出能量决定于反应物的总能量与生成物的总能量的相对高低。2.通过实例和实验了解化学能与热能的相互转化了解化学能转化为热能在生产、生活中的应用及其对人类文明发展的贡献。3.能举例说明化学能与电能的转化关系及其运用认识化学能转化为电能对现代化的重大意义初步了解化学电池的化学反应基础(氧化
