
大学有机化学醇酚醚通用.ppt

YY****。。


亲,该文档总共110页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

大学有机化学醇酚醚通用.ppt
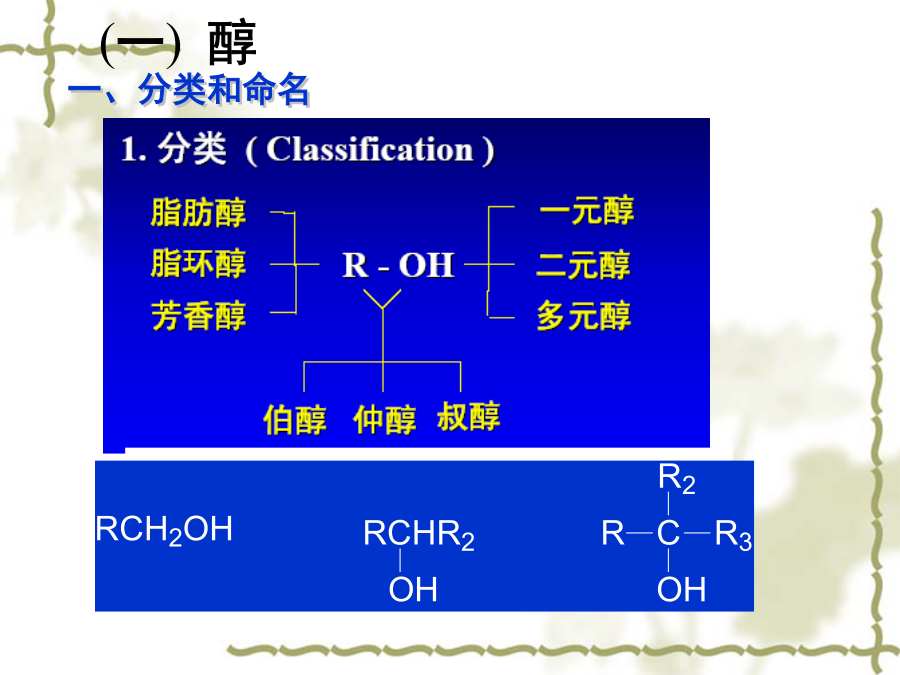
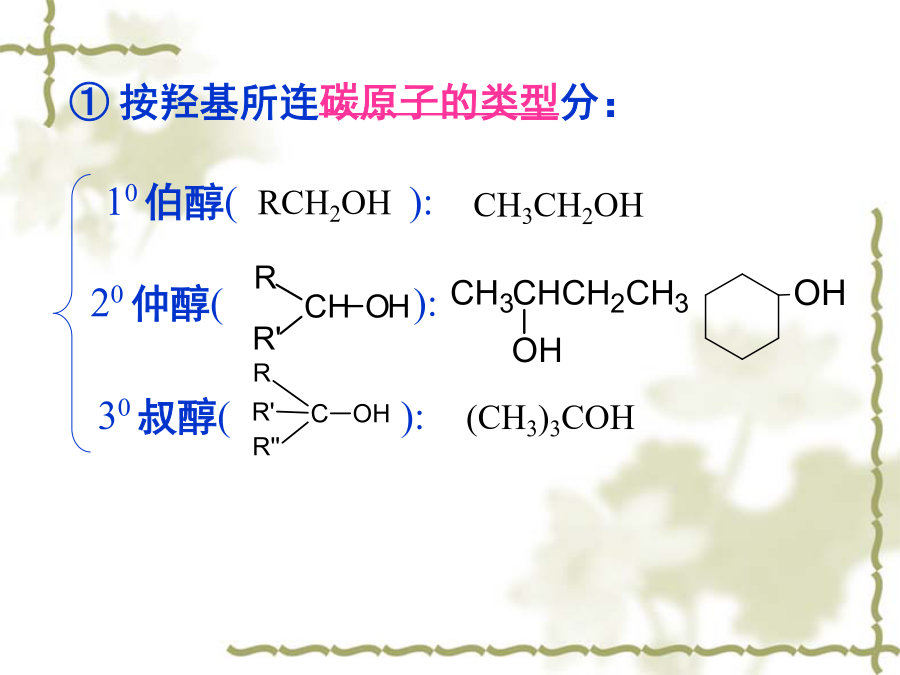
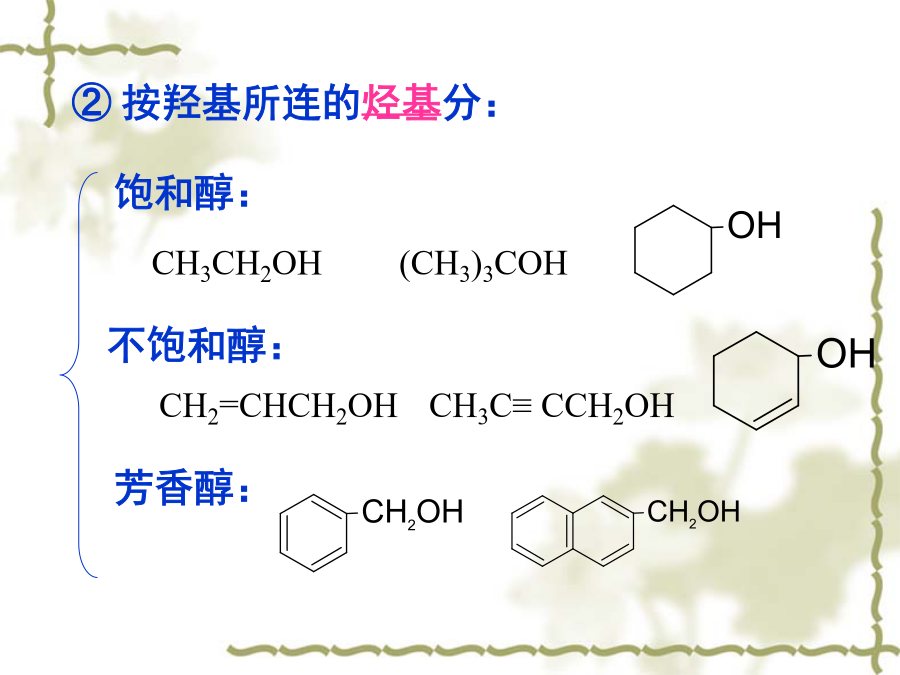
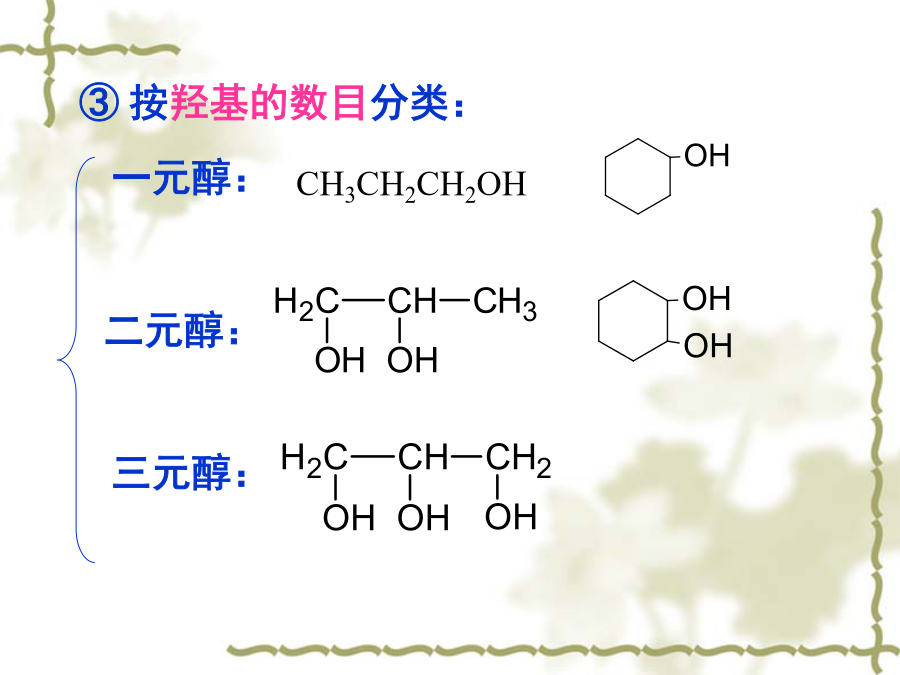
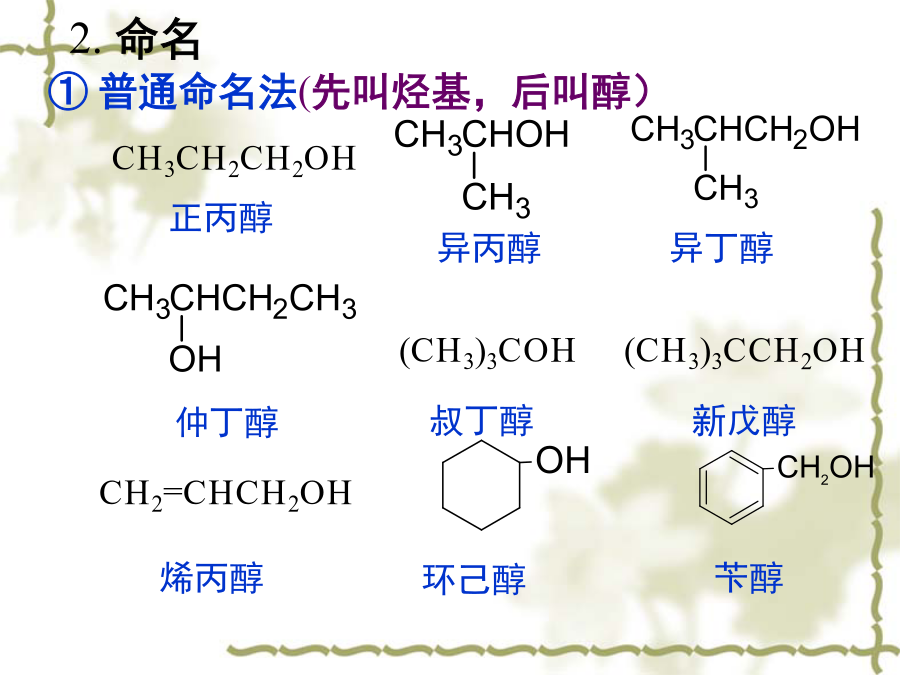
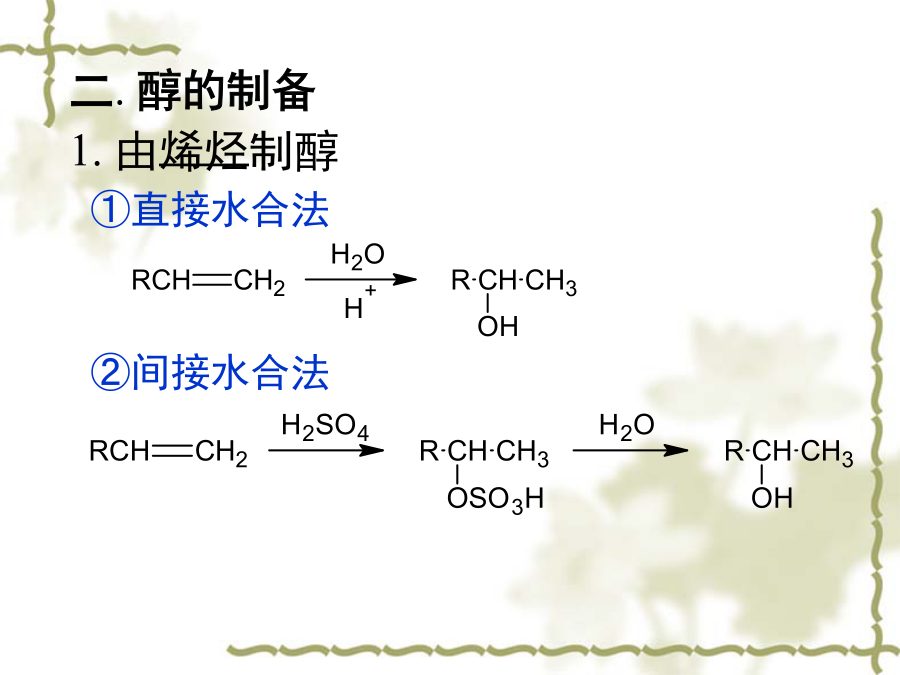
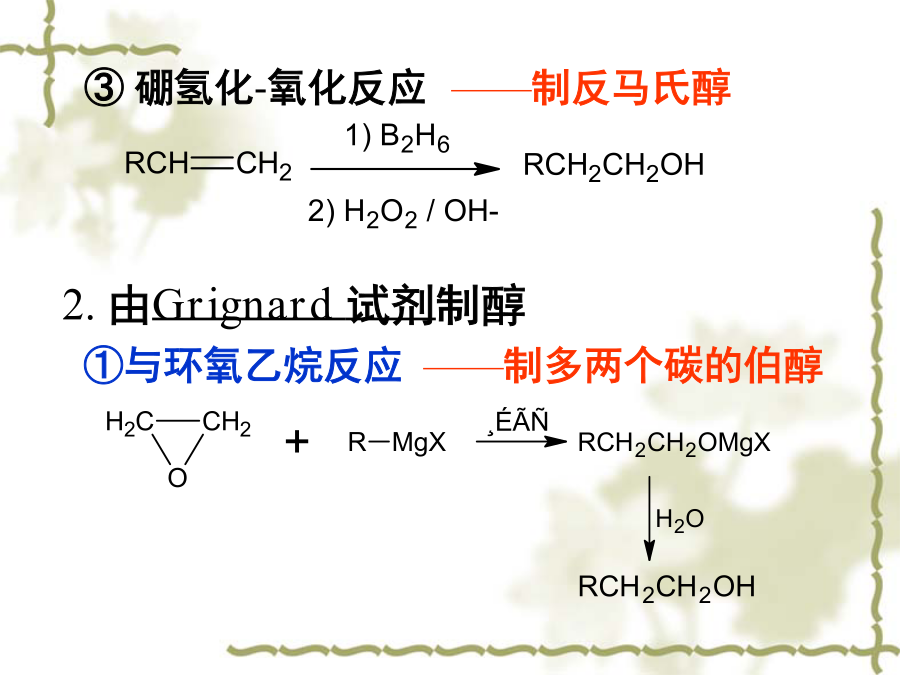
第十章醇醚Alcohols&Ethers一、分类和命名20仲醇():②按羟基所连的烃基分:③按羟基的数目分类:CH3CH2CH2OH②系统命名法(R)-1-苯基-1-丙醇二.醇的制备2.由Grignard试剂制醇②与醛、酮反应1)格式试剂与甲醛反应制伯醇2)格式试剂与一般醛反应制仲醇3)格式试剂与酮反应得叔醇注意:反应的第一步要绝对无水,因此两步一定要分开,制备格式试剂的卤代烃或者与格式试剂反应的化合物都不能含有活波氢(-OH,-NH2,-COOH,-CHO)3.醛、酮还原制醇三.醇的物理性质2.氢键对低

有机化学_醇酚醚.doc
醇酚醚(习题和答案)一、命名:1.(CH3)2CHOHCH32.3.4.5.6.7.8.(CH3)3CCH2OH9.10.CH3OC(CH3)311.12.13.C6H5CH2CHOHCH314.15.16.17.18.19.20.答案:1.3-甲基-2-丁醇2.2-丙烯-1-醇(烯丙醇)3.3-甲氧基-2-戊醇4.3-苯基-1,2-戊二醇5.1-甲基环己醇6.3,5-二甲基苯酚7.苦味酸8.新戊醇9.β-萘酚(2-萘酚)10.甲基叔丁基醚11.甲基乙烯基醚12.苯甲醚13

有机化学——07醇酚醚.ppt
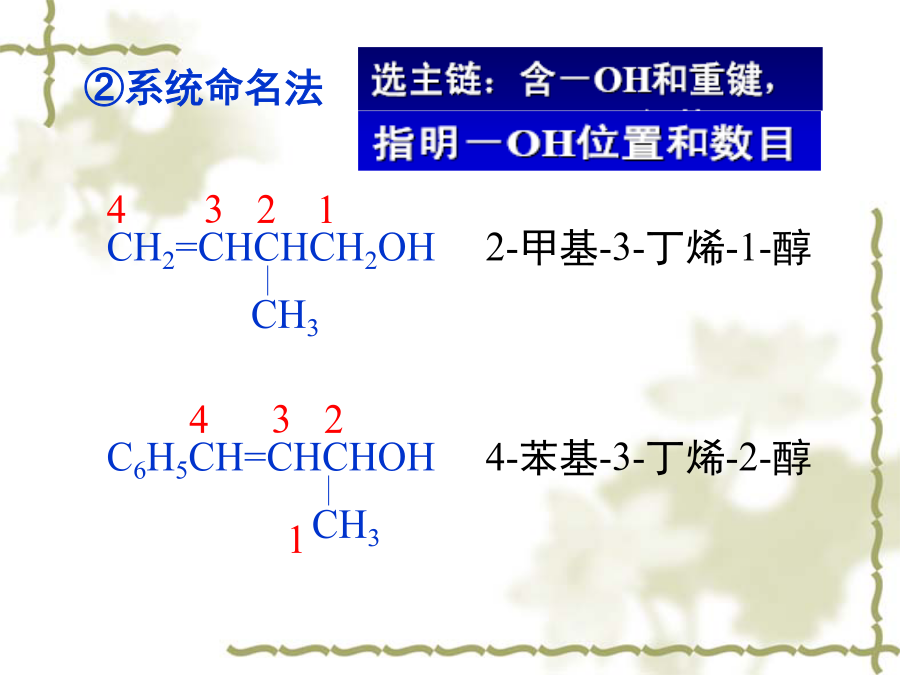
第七章醇、酚、醚2.根据所连的碳原子种类不同,醇可分为伯醇(1º醇)、仲醇(2º醇)和叔醇(3º醇)(二)醇的命名2.系统命名法这种命名法适合结构复杂的醇。其命名原则是(1)选择含有羟基的最长碳链为主链,按照主链碳原子数称为某醇(2)主链编号从靠近羟基一端开始,使羟基和取代基位次尽可能小(3)羟基所连的碳原子的位次写在醇名称之前(4)取代基的位次、数目、名称写在醇名称的前面不饱和醇命名:应选择含有羟基所连的碳原子和碳碳不饱和键在内的最长碳链作为主链,根据主链所含碳原子数称为“某烯(炔)醇”。编号时应使羟基
有机化学8醇酚醚.pdf
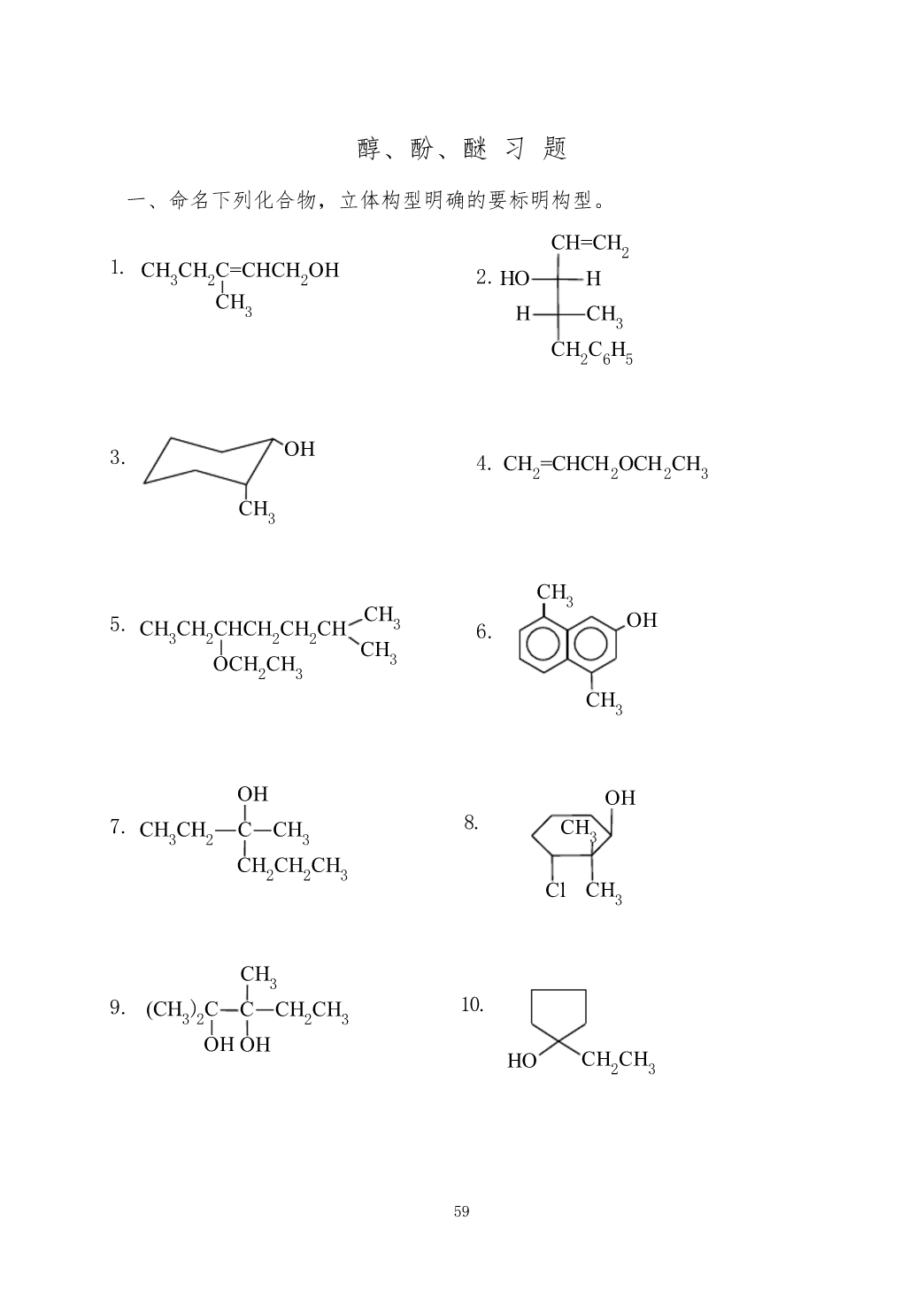
醇、酚、醚习题一、命名下列化合物,立体构型明确的要标明构型。CH=CH21.CH3CH2C=CHCH2OH2.HOHCH3HCH3CH2C6H5OH3.4.CH2=CHCH2OCH2CH3CH3CH35.CH3OHCH3CH2CHCH2CH2CH6.CHOCHCH323CH3OHOH7.8.CHCHCCHCH3323CH2CH2CH3ClCH3CH39.)10.(CH32CCCH2CH3OHOHHOCH2CH359CH11.CHCHOCHCH33212.CCHCHH3HOHCH2CH3OH13.CHCHC
【精选】有机化学醇、酚、醚(1).ppt
Ⅰ醇醇一般多元醇的羟基联在不同的碳上若联在同一碳上则不稳定:2)结构3)命名③多元醇:选择含羟基最多的碳链为主链三、化学性质的碱性比强所以醇化物遇水分解②弱碱性:通过羟氧原子上的未共用电子对与质子结合可以形成质子化的醇所以醇可溶于浓强酸中2)生成酯的反应3)与氢卤酸的反应例如:当反应按单分子历程进行时烷基有可能发生重排:伯醇则按双分子历程:4)脱水反应有可能发生重排:②分子间脱水:两分子醇发生分子间脱
