
地球周围的空气分解.ppt

YY****。。









亲,该文档总共48页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

地球周围的空气分解.ppt
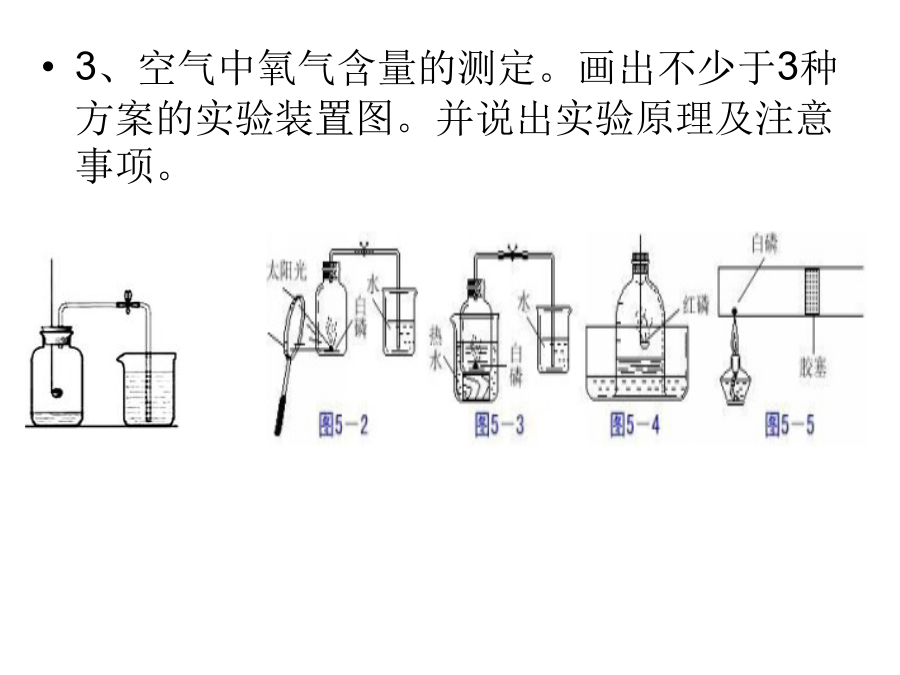
地球周围的空气一级主题一身边的化学物质二级主题一、地球周围的空气★考点1空气的主要成分(B)→A(14)气体的密度与其相对分子质量成正比,空气的平均相对分子质量为29如:He的相对分子质量为4,小于29,故氦气的密度小于空气的密度;O2的相对分子质量为32,大于29,故氧气的密度大于空气的密度。3、空气中氧气含量的测定。画出不少于3种方案的实验装置图。并说出实验原理及注意事项。(2)涉及反应:4P+5O2====2P2O5(3)实验现象:产生大量白烟,待燃烧停止,整个装置冷却至室温后,将c处的止水夹打开,

地球周围的空气.docx
第一讲地球周围的空气【知识点网络】空气︵混合物︶其它氮气78%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%(体积分数)空气的污染与保护危害:严重损害人体健康,影响作物生长,破坏生态平衡。全球气候变暖,臭氧层破坏和酸雨等。污染源:主要是有害气体(CO、SO2、氮的氧化物)和烟尘等。目前计入空气污染指数的项目为CO、SO2、NO2、O3和可吸入颗粒物等。环境保护:加强大气质量监测,改善环境状况,使用清洁能源,工厂的废气经处理过后才能排放,积极植树、造林、种草等。氧气︵纯净物︶性质物理性质

地球周围的空气.docx
地球周围的空气【知识导图】1.地球周围空气的组成2.常见气体的制取方法知识点一:知道空气的主要成分。空气的成分按体积计算:氮气占78%,氧气占21%,稀有气体占0.94%,二氧化碳占0.03%,其他气体与杂质占0.03%。空气中氧气体积分数的测定实验:红磷在密闭容器内燃烧,消耗掉氧气,生成白色固体P2O5,容器内气压减小,冷却后,打开弹簧夹,在外界大气压强作用下,集气瓶内水面上升。可通过燃烧后集气瓶内进入的水的体积来测定空气中氧气的体积分数(如图1—1)。知识点二:认识空气对人类生活的重要作用。空气是一种

地球周围的空气.doc
地球周围的空气文章摘要:空气,构成地球周围大气的气体。无色,无味,主要成分是氮气和氧气,还有极少量的氡、氦、氖、氩、氪、氙等稀有气体和水蒸气、二氧化碳和尘埃等。常温下的空气是无色无味的气体,液态空气则是一种易流动的浅黄色液体。一般当空气被液化时二氧化碳已经清除掉,因而液态空气的组成是20.95%氧,78.12%氮和0.93…

我们周围的空气分解.ppt
谜语一物到处有,用棒赶不走;眼睛看不见,手摸也没有;咀嚼无滋味,没它活不久。(打一物质)我们周围的空气通过这些实验,拉瓦锡得出了空气由氧气和氮气组成的,其中氧气约占空气总体积的1/5的结论。空气中氧气含量的测定①红磷燃烧发出黄白色火焰,放出大量的热,产生大量的白烟。②打开弹簧夹后,水顺着导管流入集气瓶,进入集气瓶中水的体积约瓶内空间的1/5。【思考】在实验操作中,水面上升的体积小于集气瓶总体积1/5,(即集气瓶中气体减少的体积会小于1/5),试分析可能的原因。【思考】能否用木炭、硫、镁代替红磷做实验?【思
