
不饱和烃PPT课件.ppt

lj****88




亲,该文档总共101页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

不饱和烃PPT课件.ppt
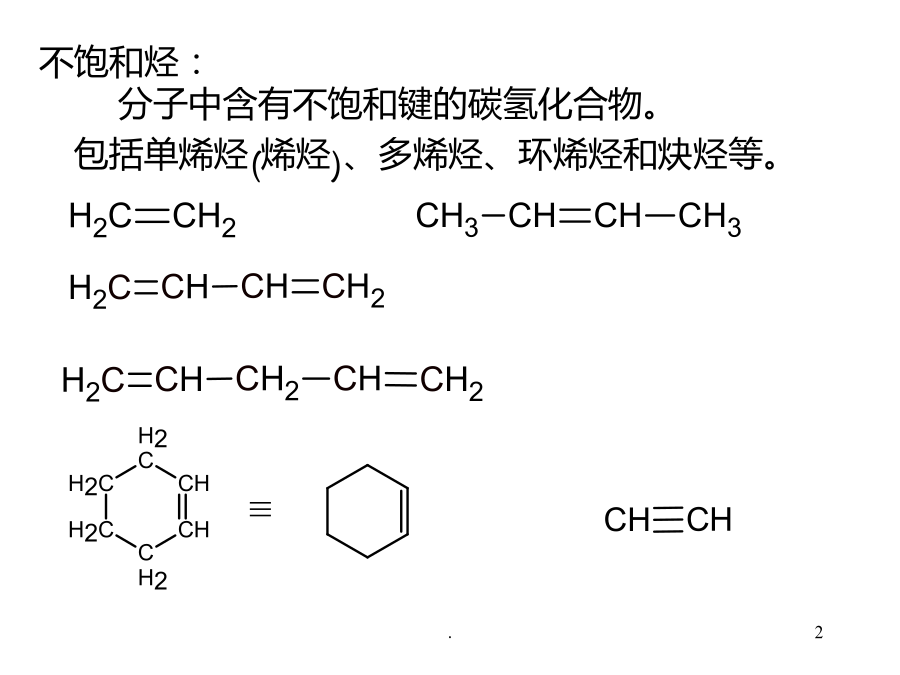
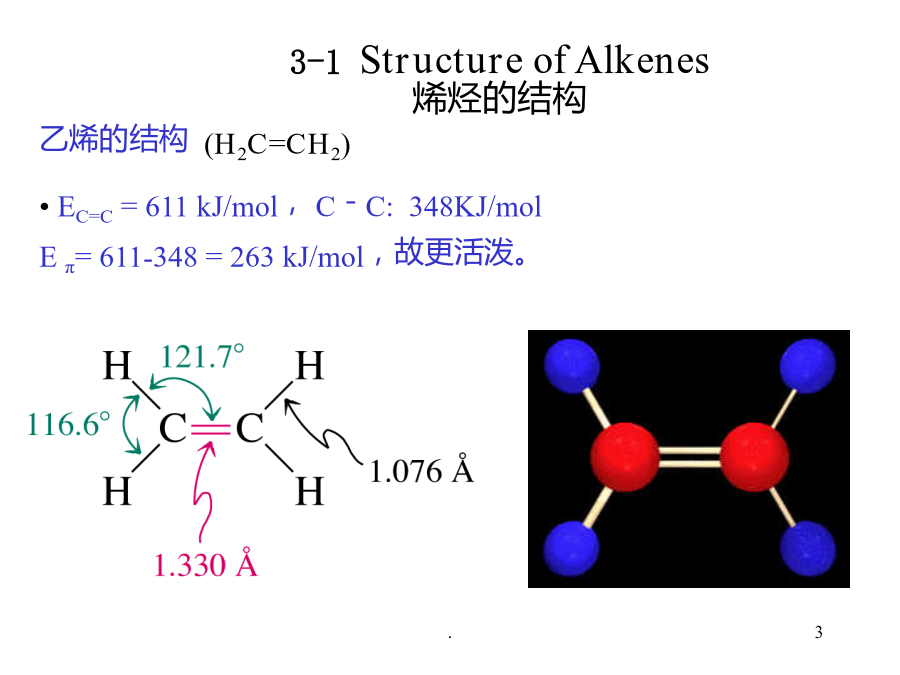
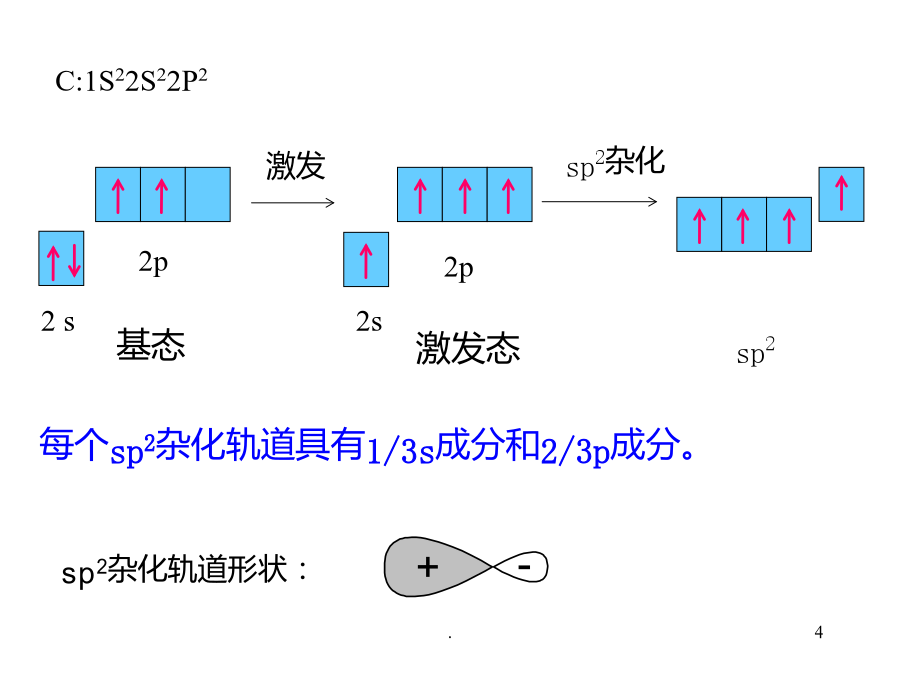
AAlkenes烯烃BAlkynes炔烃C双烯烃不饱和烃的结构、同分异构现象、命名物理性质、化学性质不饱和烃:分子中含有不饱和键的碳氢化合物。包括单烯烃(烯烃)、多烯烃、环烯烃和炔烃等。3-1StructureofAlkenes烯烃的结构每个sp2杂化轨道具有1/3s成分和2/3p成分。未参与杂化的p轨道6键的特点:1.成键原子不能绕两核连线自由旋转。2.键比键易断裂。3.电子云易极化。3-2NomenclatureandIsomerismofAlkenes烯烃的同分异构和命名烯烃:指单烯烃,分子中
不饱和脂肪烃PPT课件.ppt
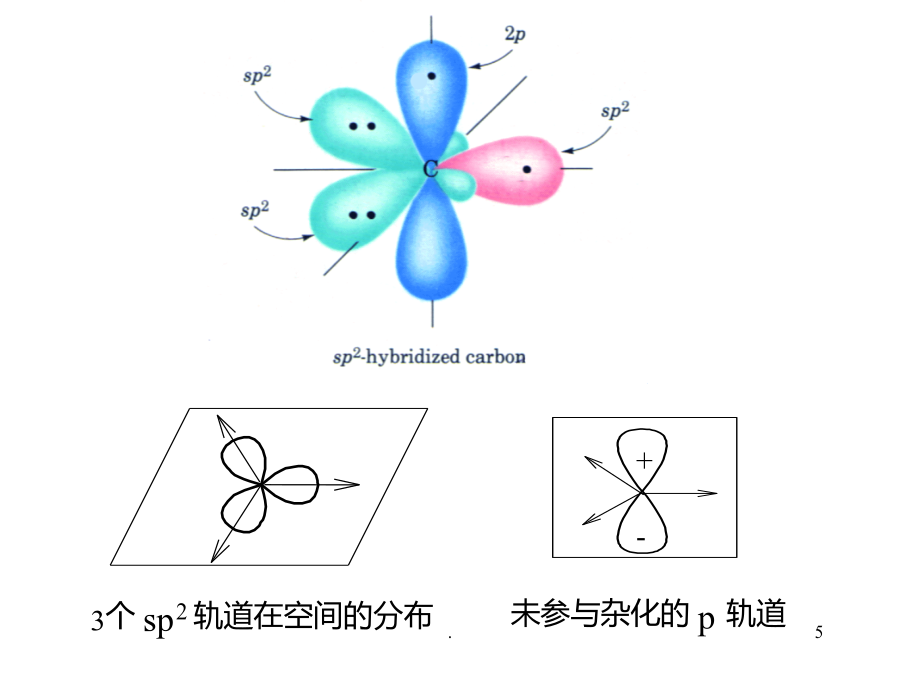
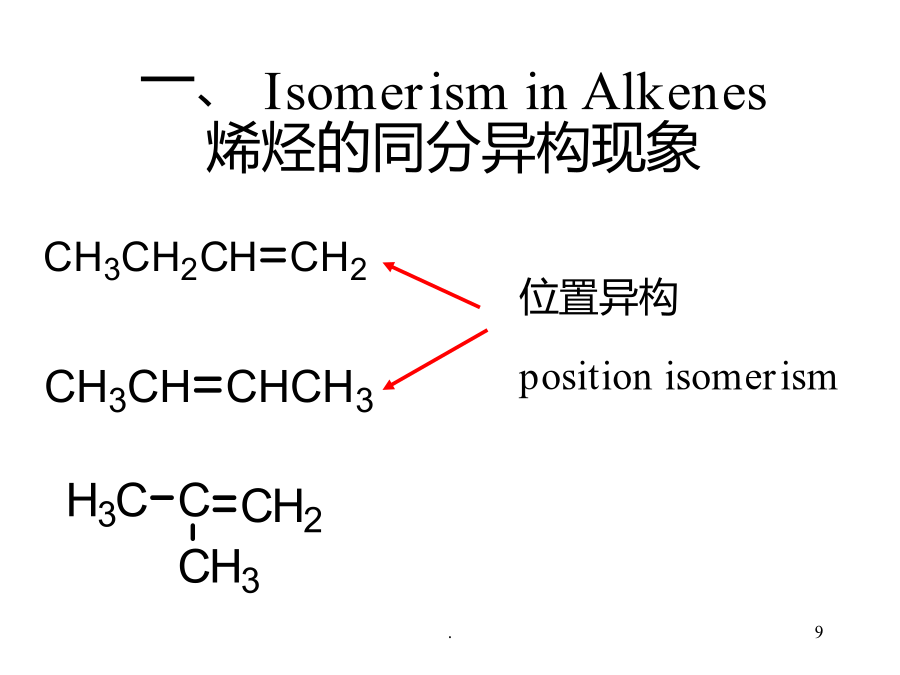
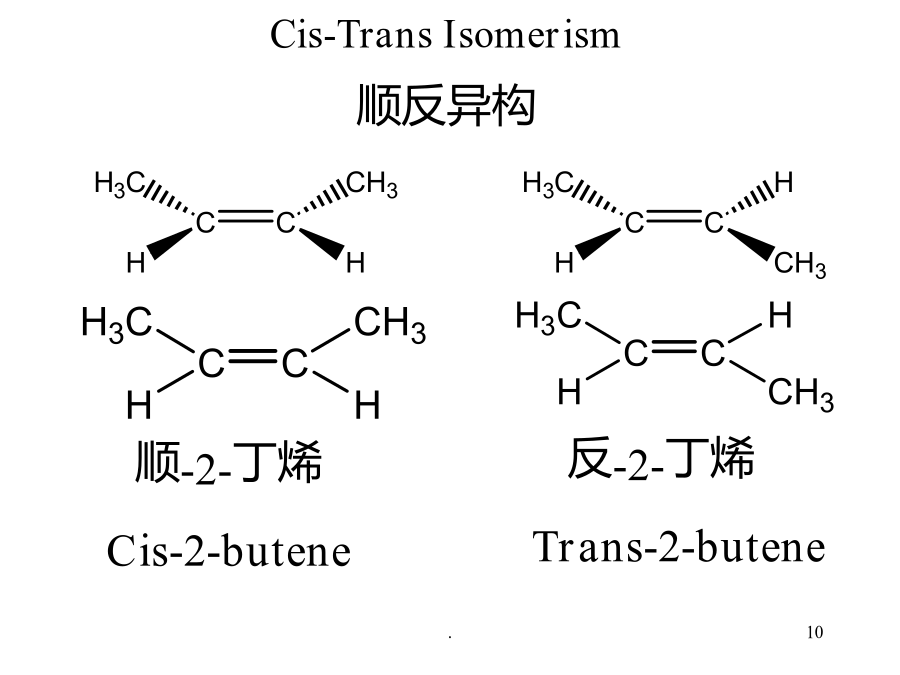
sp2杂化轨道:一个2s轨道和两个2p轨道的线性组合,杂化轨道夹角120o,三个轨道成平面三角形分布,未参与杂化的一个p轨道垂直于杂化轨道平面;p轨道与p轨道重叠形成键C二、命名和异构2、构型异构位置异构烯烃异构构型异构(configuration)顺(反)式异构体:相同的基团在双键的同(反)侧Z(E)式异构体:四个取代基不相同时,较优基团在双键的同(反)侧是不是顺式异构体?是不是顺反异构体?E-3-甲基-4-异丙基-3-庚烯三、物理性质烯烃的结构特征与反应活性:1、加成反应(1)加氢反应(2)与卤素加

高四3章不饱和烃3ppt课件.ppt
3.5.4氧化反应(1)环氧化反应例:(2)高锰酸钾氧化KMnO4氧化烯烃:炔烃用KMnO4氧化得羧酸或二氧化碳:随着工业臭氧发生器的改进,烯烃臭氧化反应在工业上得到了应用。炔烃臭氧化可生成α-二酮和过氧化氢,随后过氧化氢将α-二酮氧化成羧酸。(4)催化氧化3.5.5聚合反应炔烃二聚:(b)形成高聚物乙烯和丙烯共聚得到乙丙橡胶:3.5.6α-氢原子的反应(1)卤代反应烯烃的α-卤代反应为自由基反应,因为在光和热的情况下,有利于自由基的产生:下列反应也属于自由基取代反应,可在较低温度下进行:(2)α-C上的

高四3章不饱和烃3ppt课件.ppt
3.5.4氧化反应(1)环氧化反应例:(2)高锰酸钾氧化KMnO4氧化烯烃:炔烃用KMnO4氧化得羧酸或二氧化碳:随着工业臭氧发生器的改进,烯烃臭氧化反应在工业上得到了应用。炔烃臭氧化可生成α-二酮和过氧化氢,随后过氧化氢将α-二酮氧化成羧酸。(4)催化氧化3.5.5聚合反应炔烃二聚:(b)形成高聚物乙烯和丙烯共聚得到乙丙橡胶:3.5.6α-氢原子的反应(1)卤代反应烯烃的α-卤代反应为自由基反应,因为在光和热的情况下,有利于自由基的产生:下列反应也属于自由基取代反应,可在较低温度下进行:(2)α-C上的

不饱和烃-烯与炔烃.doc
不飽和烴-烯與炔烴不飽和烴有烯烴(alkenes)和炔烴(alkynes)兩種。一.烯烴烯分子中具有一個雙鍵,其通式為CnH2n。由於烯烴雙鍵處的高電子密度,分子在此位置具有特殊的反應性,因此化學性質較為活潑。烯烴的熔點、沸點、密度和溶解度等物理性質與同碳數的烷烴相似。密度小於水,當分子之碳數增多,則熔點、沸點亦隨之升高,C2~C4者為無色氣體,C5~C15為無色液體,C16以上者為固體,烯類易溶於有機溶劑中而不溶於水。碳數較少的烯烴可由石油分餾或由低碳數的烷烴製煉而得,至於碳數較多的烯烴可由C16至C2
