
用于检测A型猪轮状病毒的引物及探针、荧光定量PCR试剂盒及方法和应用.pdf

俊凤****bb










亲,该文档总共13页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

用于检测A型猪轮状病毒的引物及探针、荧光定量PCR试剂盒及方法和应用.pdf
本发明公开了一种用于检测A型猪轮状病毒的引物及探针、荧光定量PCR试剂盒及方法和应用,其中,引物的核苷酸序列如下:上游引物:5'GAATGCAGTTAAGACAAATGC3',下游引物:5'GTTACTTGAAGGTCGTGATTG3';探针的序列如下:5'FAM‑AATCCATAGACACGCCAGCGTCT‑BHQ13'。本发明的有益效果是:使用本发明的试剂盒能够快速、准确地实现对A型猪轮状病毒的检测;本发明的试剂盒在3.18x10
一种鸽轮状病毒A型荧光定量PCR检测的引物和探针及其试剂盒.pdf
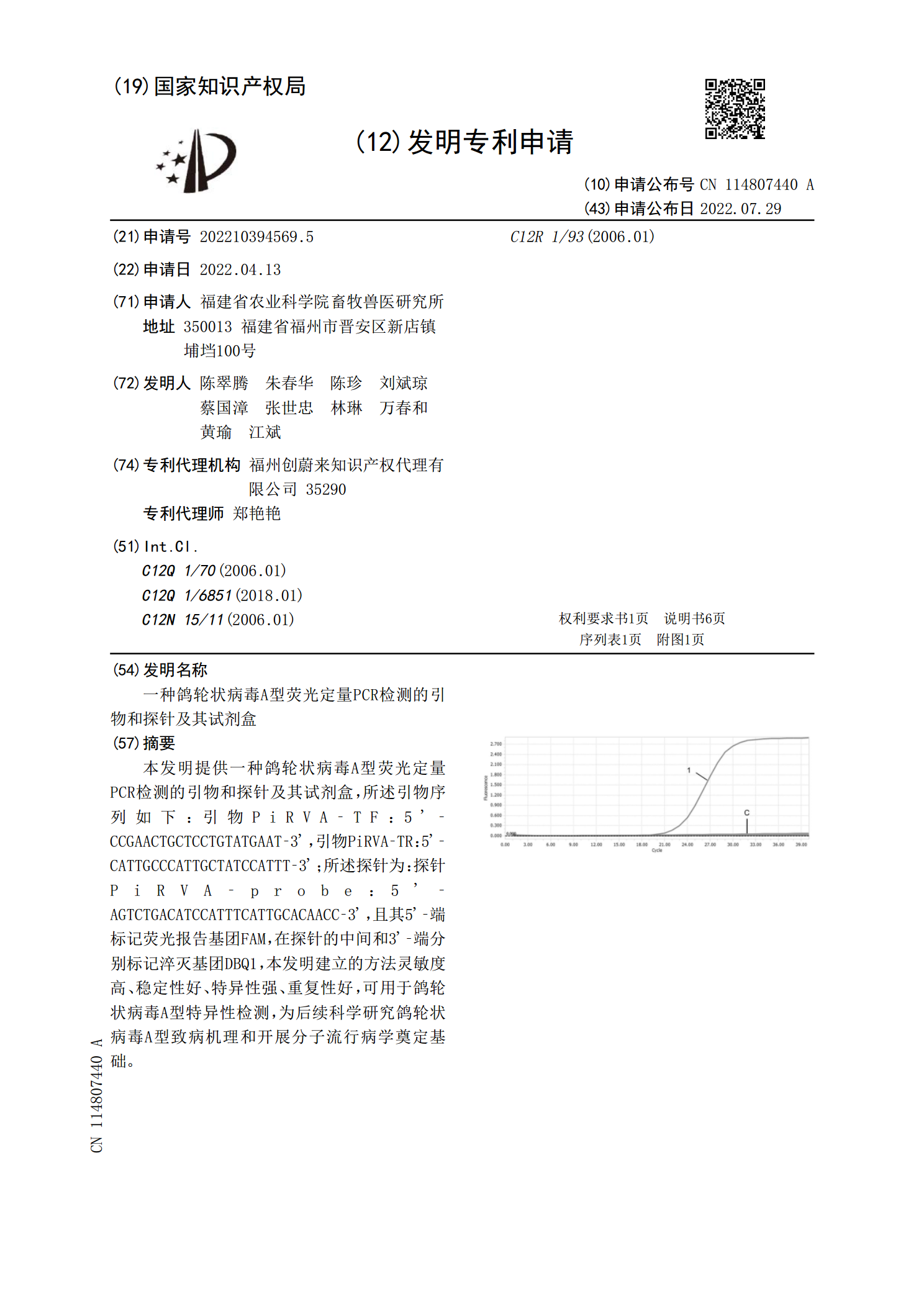
本发明提供一种鸽轮状病毒A型荧光定量PCR检测的引物和探针及其试剂盒,所述引物序列如下:引物PiRVA‑TF:5’‑CCGAACTGCTCCTGTATGAAT‑3’,引物PiRVA‑TR:5’‑CATTGCCCATTGCTATCCATTT‑3’;所述探针为:探针PiRVA‑probe:5’‑AGTCTGACATCCATTTCATTGCACAACC‑3’,且其5’‑端标记荧光报告基团FAM,在探针的中间和3’‑端分别标记淬灭基团DBQ1,本发明建立的方法灵敏度高、稳定性好、特异性强、重复性好,可用于鸽轮状病

4型和6型猪细小病毒双重荧光定量PCR检测的引物和探针组及试剂盒.pdf
本发明公开了4型和6型猪细小病毒双重荧光定量PCR检测的引物和探针组及试剂盒,所述引物和探针组由PPV6的上游引物PPV6?F、下游引物PPV6?R和探针PPV6?P以及PPV4的上游引物PPV4?F、下游引物PPV4?R和探针PPV4?P组成,所述PPV6?F、PPV6?R、PPV6?P、PPV4?F、PPV4?R、PPV4?P的核苷酸序列分别如SEQIDNO:1~SEQIDNO:6所示。本发明建立的双重荧光定量PCR检测方法对于猪细小病毒6型的检测灵敏度可达到7.7copies/μl,对于猪细小病毒4

一种用于EB病毒荧光定量PCR检测的引物和探针组、及试剂盒.pdf
本发明公开了一种用于EB病毒荧光定量PCR检测的引物和探针组、及试剂盒;引物和探针组包括上游引物,如SEQIDNO.1所示;下游引物,如SEQIDNO.2所示;探针,如SEQIDNO.3所示;探针的5’端标记有荧光基团,3’端标记有淬灭基团;试剂盒包括:核酸提取液、红细胞裂解液、PCR反应液、混合酶液、阴性质控品、临界阳性质控品、强阳性质控品和阳性标准品;该试剂盒通过特异性的引物和探针、在阴性质控品、临界阳性质控品、强阳性质控品的监控下,与阳性标准品进行同步测定,测得的结果具有灵敏度高、准确度

一种用于检测鸽轮状病毒A型的实时荧光定量PCR检测引物及其试剂盒.pdf
本发明提供一种用于检测鸽轮状病毒A型的实时荧光定量PCR检测引物及其试剂盒,引物序列如SEQIDNO.1‑2所示,具有很高的特异性和灵敏度。建立的方法能够对鸽群中鸽轮状病毒A型感染进行检测,简化操作程序、节约成本。实时荧光定量PCR反应结束后,通过观察其扩增曲线结合Tm值即可直接对结果进行判断。本发明的建立可填补国内外相关领域空白。
