
试题-全国-2009_2009届高考化学试题汇编:化学与技术(2).rar

景山****魔王










亲,该文档总共11页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

试题-全国-2009_2009届高考化学试题汇编:化学与技术(2).rar
用心爱心专心2009届高考化学试题汇编:化学与技术(2)1、(浙江省富阳新中2008(上)高三期中考试)(本题9分)碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO等杂质,提纯工艺路线如下:题24图-2题24图-1已知碳酸钠的溶解度(S)随温度变化的曲线如图(题24图-2)所示:回答下列问题:(1)滤渣的主要成分为_________________________。(2)“趁热过滤”的原因是_____________________
试题-全国-2009_2009届高考化学试题汇编:化学与技术.rar
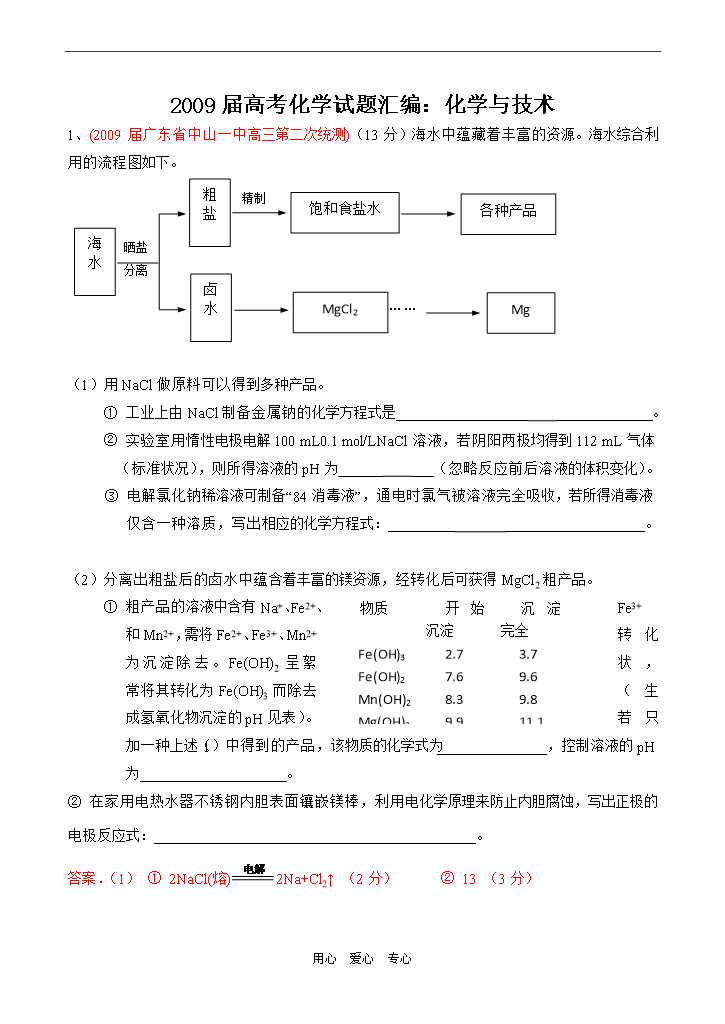
用心爱心专心2009届高考化学试题汇编:化学与技术1、(2009届广东省中山一中高三第二次统测)(13分)海水中蕴藏着丰富的资源。海水综合利用的流程图如下。海水晒盐分离粗盐卤水饱和食盐水各种产品MgCl2Mg精制……(1)用NaCl做原料可以得到多种产品。①工业上由NaCl制备金属钠的化学方程式是_______________________________。②实验室用惰性电极电解100mL0.1mol/LNaCl溶液,若阴阳两极均得到112mL气体(标准状况),则所得溶液的pH为_________(忽略

试题-全国-2009_2009届高考化学试题汇编:化学与技术(3).rar
用心爱心专心2009届高考化学试题汇编:化学与技术(3)1.(2008年重庆一中高2009级月考)下列有关工业生产的叙述正确的是A.用明矾净水是因为Al3+水解生成的Al(OH)3胶粒具有很强的吸附性B.合成氨生产过程中采用高温高压条件都是为了提高N2、H2的转化率C.硫酸工业中,在接触室安装热交换器是为了利用硫铁矿燃烧时放出的热量D.工业上将氨转变为硝酸及其他氮的化合物是氮的固定2.(江宁高级中学08~09学年度第一学期高三年级12月月考三校联考)(8分)镁及其合金是一种用途很广的金属材料,目前世界上6

试题-全国-2009_2009届高考化学试题汇编:电化学(2).rar
用心爱心专心2009届高考化学试题汇编:电化学(2)1.(13分)下表由元素周期表的前三周期去掉副族上方的空白区域后组合而成,表中虚线处为ⅡA、ⅢA族的连接处。请用相应的化学用语回答下列问题:abcdefgh(1)写出仅由e形成的两种带有相同电荷数的阴离子的符号:、。(2)h的单质能与g元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式。(3)上左图是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则其中柱形“8”代表。(填化学式)(4)b、c、d、e、f的氢化物的沸点

试题-全国-2009_2009届高考化学试题汇编:实验基础(2).rar
用心爱心专心2009届高考化学试题汇编:实验基础(2)1、(广东天河中学09高三模拟)(12分)已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质。工业废水泥污澄清溶液步骤1步骤2固体残渣CuSO4溶液步骤3CuSO4·5H2OHg(1)步骤1的主要操作是,需用到的玻璃仪器除烧杯外有。(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式),固体残渣的成分是(填化学式)。(3)步骤3中涉及的操作是:蒸发浓缩、、过滤、烘干。(4
