
第6章 醇和醚.ppt

ys****39










亲,该文档总共62页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

第6章 醇和醚.ppt
第6章醇和酚一、分类:根据羟基数目多少二、醇的命名(二)、系统命名例如:5-苯基-4-己烯-2-醇5-phenyl-4-hexen-2-ol(三)俗名:根据来源进行命名。三、醇的结构和物理性质四、物理性质(1)氢键羟基与水分子之间可以形成很强的氢键:醇氢键的形成,造成:醇的沸点比相应烷烃高低分子量的醇易溶于水醇分子中,由于氧原子的电负性较碳原子和氢原子大,C--O键和O--H键的极性较大,1、醇中氧氢键断裂反应醇和金属钠作用可放出氢生成醇钠。醇钠是白色固体、遇水水解生成醇和NaOH不同结构的醇与金属钠反应
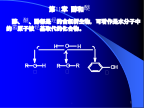
第章醇和醚PPT课件.ppt
第11章醇和醚(一)醇甲醇(methanol)丙三醇(propanetriol)苯甲醇(phenylmethanol)一、分类硫醇:RSH二、物性(自学)低级醇与MgCl2,CaCl2,CuSO4等形成结晶醇如:IR:O-H游离羟基3650~3500cm-1缔合羟基3500~3200cm-1峰形较宽NMR:O-Hδ=1~5ppmCH3OHRCH2OHR2CHOHδ(ppm):3.43.63.9三、化学性质1、醇的弱酸性(与金属反应)1)实验室中用于销毁残余的金属钠;2)可制备醇金属;醇金属是一种强碱、强亲

醇和醚.ppt
醇结构特点:2.分类3.命名②甲醇衍生物命名法:--------以甲醇作母体4-丙基-5-己烯-1-醇2-乙基-2-羟甲基-1,3-丙二醇硼氢化—氧化法两个独特之处:2、由醛、酮制备制3.卤代烃水解:二、醇的物理性质2.沸点(b.P.)3.水溶性1.与活泼金属反应从下列数据可以看到醇的酸性比水弱,但醇的共轭碱RO﹣的碱性却比OH﹣还要强。R-OH+HXR-X+H2O②反应速度与烃基结构有关:RCH2-OH+HXRCH2-OH2+XSN1历程如:3.与卤化磷和二氯亚砜反应(CH3)2SO4毒性大,但是很好的

醇和硫醇醚和硫醚(03).ppt
第九章醇和硫醇醚和硫醚(AlcoholsandThiols、EthersandThioethers)二.物理性质醇和物CaCl24C2H5OH酸性:ROH<H2O;碱性:RONa>NaOHSN1机制:(多数2o3o醇)反应按SN1历程,有碳正离子重排。2)与PX3、SOCl2反应3.成酯反应烷基二磷酸酯、烷基三磷酸酯在生物化学中非常重要。[讨论]氧化铝催化加热脱水(不发生重排)制混合醚(3o与1o醇)b.CrO3—吡啶、CrO3—H2SO4(稀)c.DCC-DMSO-羟基酸、1,2-二酮、-氨基酮及

醇和醚资料讲解.ppt
第一节醇第二节醚(一)醇的分类、同分异构和命名(二)醇的结构(三)醇的制法(四)醇的物理性质(五)醇的化学性质(六)多元醇(七)硫醇(自学)第九章醇和醚(一)醇的分类、同分异构和命名(二)醇的结构(三)醇的制法(三)醇的制法(丙)羟汞化-脱汞反应(丁)硼氢化-氧化反应(2)卤代烃水解(3)从Grignard试剂制备(4)醛、酮、羧酸和羧酸酯的还原羧酸最难还原,只能被LiAlH4还原:(四)醇的物理性质②溶解度:③光谱性质例2:乙醇液膜的IR谱图,只有缔合OH(3333cm-1);乙醇的CCl4稀溶液的IR
