
基本概念复习.ppt

kp****93









亲,该文档总共77页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

基本概念复习.ppt
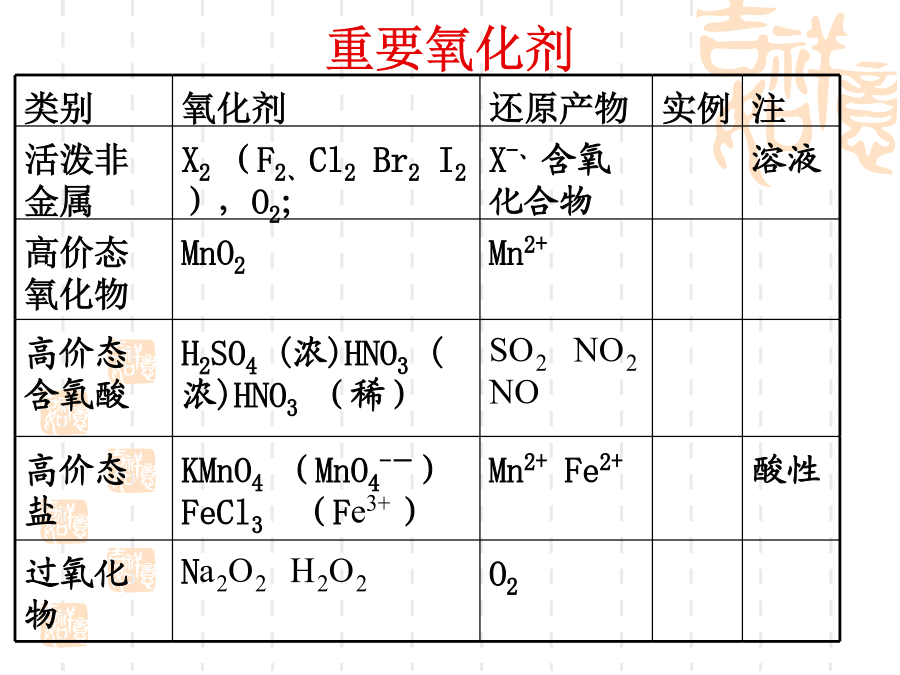
高中化学复习知识体系化学学科知识分为六大版块化学学科知识分为六大版块基本概念:五项主干知识复习方法建议一、氧化还原反应重点:常见氧化剂和还原剂重要氧化剂重要还原剂氧化剂还原剂强弱判断常见比较顺序例题关于氧化还原反应的简单计算新题境、新亮点难点例题②原无色有刺激性气味的气体与含1.5molY的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液全国2---10.已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2OIO3-→I2MnO4-→Mn2+HNO2→NO如果分别用等物质的量的这

基本概念复习.ppt
基本概念复习一、关于氧化还原反应概念2.常见的氧化剂、还原剂活泼的金属单质:无氧酸:低价化合物:非金属单质:练习:苹果汁是人们喜欢的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生,说明维生素C具有(A)氧化性(B)还原性(C)碱性(D)酸性思考:哪些事实证明铁比铜还原性强?3.氧化性还原性强弱的比较练习:96年试测题思考:下列物质能否反应?演示实验4.浓度、酸度、温度的影响演示实验:二、应用氧化还原概念解决问题成套装置:每部分的作用?

基本概念复习.ppt
基本概念复习一、关于氧化还原反应概念2.常见的氧化剂、还原剂活泼的金属单质:无氧酸:低价化合物:非金属单质:练习:苹果汁是人们喜欢的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生,说明维生素C具有(A)氧化性(B)还原性(C)碱性(D)酸性思考:哪些事实证明铁比铜还原性强?3.氧化性还原性强弱的比较练习:96年试测题思考:下列物质能否反应?演示实验4.浓度、酸度、温度的影响演示实验:二、应用氧化还原概念解决问题成套装置:每部分的作用?

基本概念复习.doc
让自己的进步每天看得见福州学大教育杨桥学习中心福州学大教育杨桥学习中心一对一授课学案授课教师:学生姓名:授课时间:本周重难点知识分析及精典练习巩固基本概念复习知识点1、物质的分类金属:Na、Mg、Al单质非金属:S、O、N氧化物纯净含氧酸:HNO3、H2SO4等物按酸根分无氧酸:HCl强酸:HNO3、H2SO4、HCl酸按强弱分弱酸:H2CO3、HClO、CH3COOH化一元酸:HCl、HNO3合按电离出的H个数二元酸:H2SO4、H2SO3物多元酸:H3PO4强碱:NaOH、Ba(OH)2物按强弱分质弱

基本概念复习.ppt
高三复习基本概念复习内容(一)、物质的组成、性质和分类核外电子2、元素四“同”的比较四“同”的比较元素在自然界的含量例、意大利科学家最近合成一种新型氧分子,它由4个氧原子构成,专家认为它液化后的能量、密度都比普通氧分子高得多,下列关于该分子叙述正确的是A.它是氧元素的另一种同位素B.它是氧元素的另一种同素异形体C.它的摩尔质量是64D.它将成为一种新型强力火箭推进燃料答案:B二、物质的分类:1.单质的分类2.氧化物的分类3.氢化物的分类例:“混盐”是指一种金属离子与多种酸根离子构成的盐,如:氯化硝酸钙[C
