
高三化学专题复习电解质溶液.doc

是你****岺呀







在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

高三化学专题复习电解质溶液.doc
专题电解质溶液常考的知识点:(1)弱酸或弱碱、盐类水解的平衡移动:升高温度、加水稀释、增大反应物的浓度或减小生成物浓度平衡正移。(2)酸、碱、盐对水的电离平衡的影响:酸、碱抑制水的电离,由水电离产生的c(H+)或c(OH-)小于10-7mol/L;盐促进水的电离,显酸性的盐溶液由水电离产生的c(H+)大于10-7mol/L。(3)不同的盐溶液中同种离子浓度的大小比较(看其他的粒子对水解平衡的影响)方法:一看个数,二看促进还是抑制(4)加水稀释的问题:①氢离子和氢氧根离子浓度不能同时减小②酸碱性一定是强酸强

高三化学专题复习专题八电解质溶液2.ppt
专题八电解质溶液(2)一、盐类的水解:(1)水解程度一般较小,不能进行到底。如:0.1mol/LNaAc,水解部分只占0.0075%。0.1mol/LNa2CO3,水解部分只占4%。(2)水解可促进水的电离。(3)水解可看作中和反应的逆反应。(1)强碱弱酸盐:阴离子水解,溶液呈碱性如:NaAcK2CO34、水解方程式的书写方法:(3)多元弱酸强碱盐(正盐):多元弱酸的酸根离子的水解是分步进行的,酸根离子带几个负电荷写几个方程式。其中第一步水解程度远远大于第二步电离。1、下列盐的水溶液中,哪些呈酸性()哪些

高三化学一轮复习-专题-电解质溶液.doc
电解质溶液1.已知一种c(H+)=1×10﹣3mol/L的一元酸溶液和一种c(OH﹣)=1×10﹣3mol/L的一元碱溶液等体积混合后溶液呈碱性,生成的盐可能是()A.强酸强碱盐B.强酸弱碱盐C.强碱弱酸盐D.上述三种盐均可能2.25℃时,向10mL0.01mol·L-1KOH溶液中滴加0.01mol·L-1苯酚溶液,混合溶液中粒子浓度关系正确的是()A.当pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-)B.当pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-)C.V[
高三化学高考专题复习教案七:电解质溶液人教版.doc
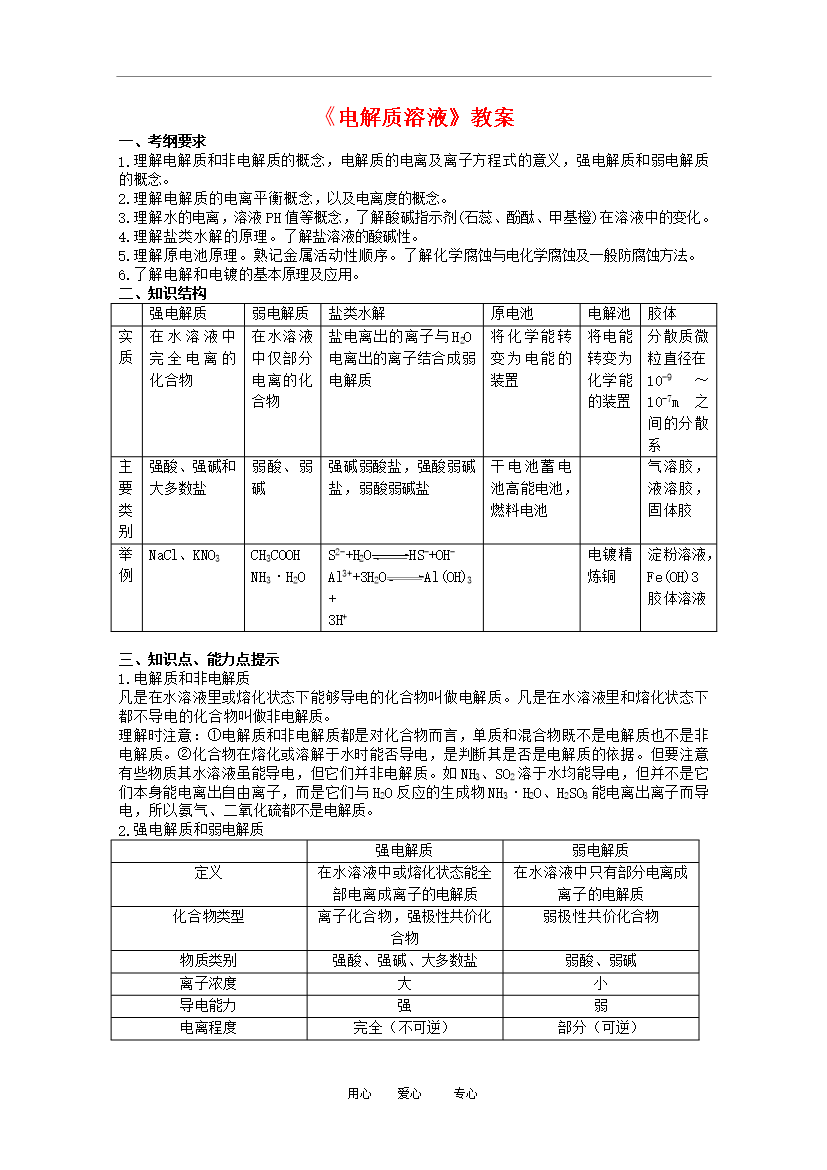
用心爱心专心《电解质溶液》教案一、考纲要求1.理解电解质和非电解质的概念电解质的电离及离子方程式的意义强电解质和弱电解质的概念。2.理解电解质的电离平衡概念以及电离度的概念。3.理解水的电离溶液PH值等概念了解酸碱指示剂(石蕊、酚酞、甲基橙)在溶液中的变化。4.理解盐类水解的原理。了解盐溶液的酸碱性。5.理解原电池原理。熟记金属活动性顺序。了解化学腐蚀与电化学腐蚀及一般防腐蚀方法。6.了解电解和电镀的基本原理及应用。二、知识结构强电解质弱电解质盐类水解原电池电解池胶体实质在水溶液中完

试题-全国-2009_高三化学专题复习电解质溶液.rar
用心爱心专心专题电解质溶液常考的知识点:(1)弱酸或弱碱、盐类水解的平衡移动:升高温度、加水稀释、增大反应物的浓度或减小生成物浓度平衡正移。(2)酸、碱、盐对水的电离平衡的影响:酸、碱抑制水的电离,由水电离产生的c(H+)或c(OH-)小于10-7mol/L;盐促进水的电离,显酸性的盐溶液由水电离产生的c(H+)大于10-7mol/L。(3)不同的盐溶液中同种离子浓度的大小比较(看其他的粒子对水解平衡的影响)方法:一看个数,二看促进还是抑制(4)加水稀释的问题:①氢离子和氢氧根离子浓度不能同时减小②酸碱性
