
β-氟代手性非天然氨基酸的制备方法.pdf

Th****s3










在线预览结束,喜欢就下载吧,查找使用更方便
相关资料
β-氟代手性非天然氨基酸的制备方法.pdf
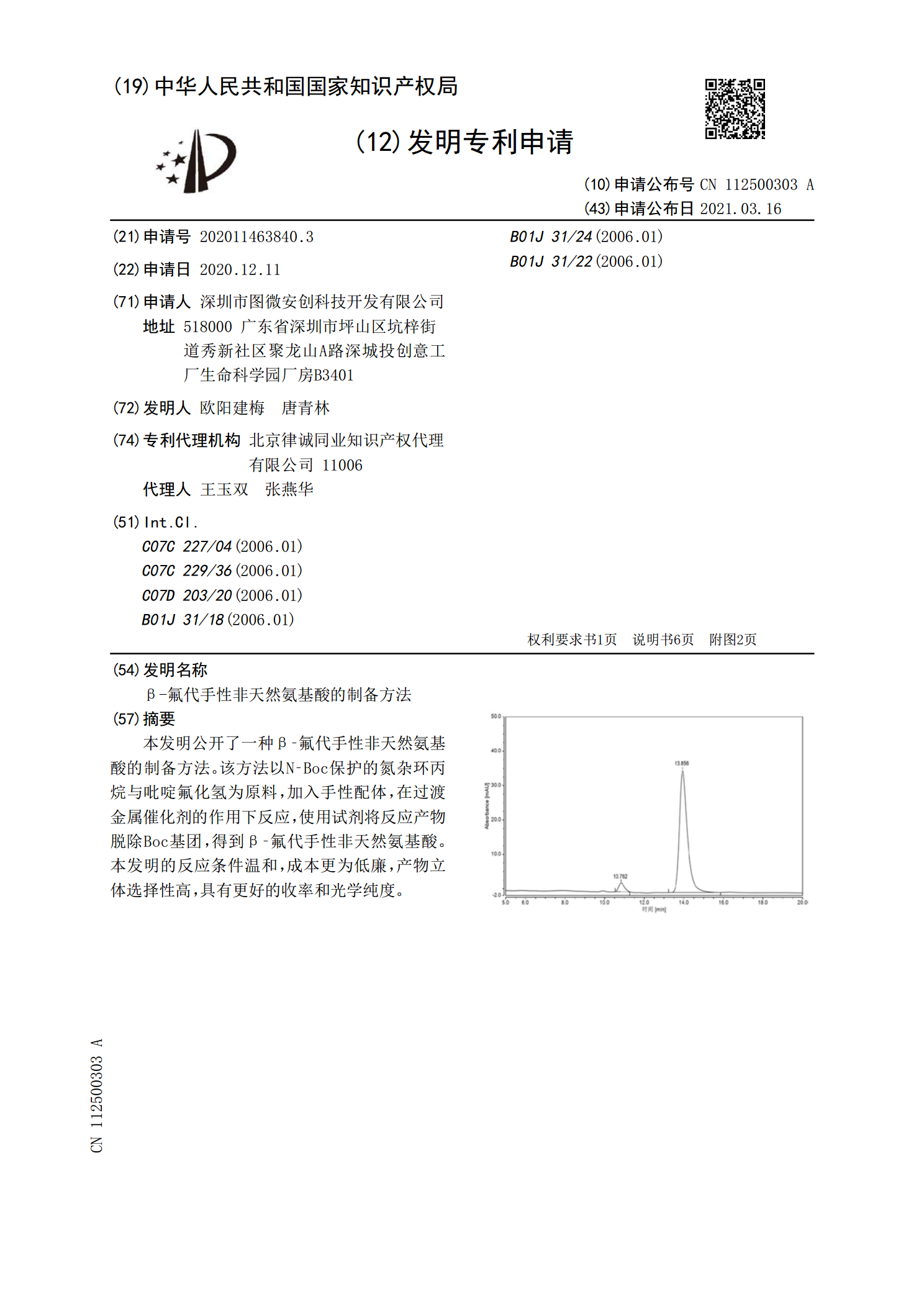
本发明公开了一种β‑氟代手性非天然氨基酸的制备方法。该方法以N‑Boc保护的氮杂环丙烷与吡啶氟化氢为原料,加入手性配体,在过渡金属催化剂的作用下反应,使用试剂将反应产物脱除Boc基团,得到β‑氟代手性非天然氨基酸。本发明的反应条件温和,成本更为低廉,产物立体选择性高,具有更好的收率和光学纯度。

酶法制备非天然手性氨基酸研究的开题报告.docx
酶法制备非天然手性氨基酸研究的开题报告一、选题背景手性分离是化学中广为应用的一个技术,因为分子的手性对其化学性质至关重要。这是因为手性分子在化学反应中的表现是不同的,如果两个互异手性的分子混杂在一起,会导致化学反应失活或生成非对映体纯的混合物。非对映体选择性催化(enantioselectivecatalysis)已经成为当代有机合成的重要领域。特别是对于非天然手性氨基酸的制备,其重要性更加显著。在医药、农药、食品添加剂、生物转化反应等行业中,非天然手性氨基酸的需求越来越大。酶是一种重要的生物催化剂,可有

手性β-氨基酸衍生物的制备方法.pdf
本发明提供了一种手性β‑氨基酸衍生物的制备方法。制备方法还包括以下步骤:S1,将第一溶剂、生物酶催化剂和氨基供体混合形成混合原料溶液;第一溶剂为醇类溶剂,或者为水和醇类溶剂的混合溶剂;S2,通过连续送料设备向混合原料溶液中以连续固体股流形式加入固体颗粒底物A进行酶促反应,得到手性β‑氨基酸衍生物。应用本发明的技术方案,更有效地改善了将底物溶解在有机溶剂中再滴加的弊端,解决了在酶促反应过程中底物容易成团析出的问题,促使手性β‑氨基酸衍生物收率更高。而且,本发明制备方法更加简洁、方便,原料更易得,可重复性更好

一种手性氨基酸的制备方法.pdf
本发明属于氨基酸技术领域,涉及一种手性氨基酸酯的制备方法。包括以下步骤:取DL‑氨基酸酯2mmo1溶于10ml乙酸乙酯;取拆分剂对DL氨基酸酯溶液进行手性拆分,对手性拆分过后DL氨基酸酯溶液的滴入10ml含1mmolRTTCA的乙酸乙酯溶液,搅拌反应30~60min,有大量白色沉淀或者粘稠油状物析出,分离出固体或油状物,即为RTTCA‑氨基酸酯盐。取RTTCA‑氨基酸酯盐加入1.5moL/LNaOH溶液使盐分解,再用乙酸乙酯萃取,分离出光学活性氨基酸酯,其光学纯度达到58%~69%,收率达到50%以上。

含有非天然氨基酸和多肽的组合物、涉及非天然氨基酸和多肽的方法以及非天然氨基酸和多肽的用途.pdf
本发明公开了非天然氨基酸和包括至少一个非天然氨基酸的多肽,以及制备所述非天然氨基酸和多肽的方法。所述非天然氨基酸本身或作为多肽的一部分可包括多种可能的官能团,但通常具有至少一个芳香族胺基。本发明还进一步公开了经翻译后修饰的非天然氨基酸多肽、实现所述修饰的方法以及纯化所述多肽的方法。所述经修饰非天然氨基酸多肽通常包括至少一个烷基化胺基。另外,本发明公开了使用所述非天然氨基酸多肽和经修饰非天然氨基酸多肽的方法,包括治疗、诊断和其它生物技术用途。
