
九年级化学上册 4.1原子的构成教案(2) 人教新课标版.doc

东耀****哥哥



在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

九年级化学上册 4.1 原子的构成教案2 人教新课标版.doc
第四单元物质构成的奥秘单元设计教材内容概述:本单元内容是初中化学“双基”的重要组成部分涵盖了本册教材双基内容的近一半是初中化学的核心内容。这一单元对学生来说十分重要既是他们今后学习化学的理论基础也是必不可少的学习工具。这部分内容比较抽象远离学生的生活经验再加上前三个单元学生学到的元素化合物知识不多(主要是空气、氧气和水)感性知识不充分这就给教学带来了一定的困难。本单元教材共分为原子的构成、元素、离子、化学式与化合价四个课题。它们包括原子结构模型、相对原子质量、元素、元素符号、核外电子排布、离子、

九年级化学上册 4.1 原子的构成教案2 人教新课标版.doc
第四单元物质构成的奥秘单元设计教材内容概述:本单元内容是初中化学“双基”的重要组成部分涵盖了本册教材双基内容的近一半是初中化学的核心内容。这一单元对学生来说十分重要既是他们今后学习化学的理论基础也是必不可少的学习工具。这部分内容比较抽象远离学生的生活经验再加上前三个单元学生学到的元素化合物知识不多(主要是空气、氧气和水)感性知识不充分这就给教学带来了一定的困难。本单元教材共分为原子的构成、元素、离子、化学式与化合价四个课题。它们包括原子结构模型、相对原子质量、元素、元素符号、核外电子排布、离子、

九年级化学上册 4.1原子的构成教案(2) 人教新课标版.doc
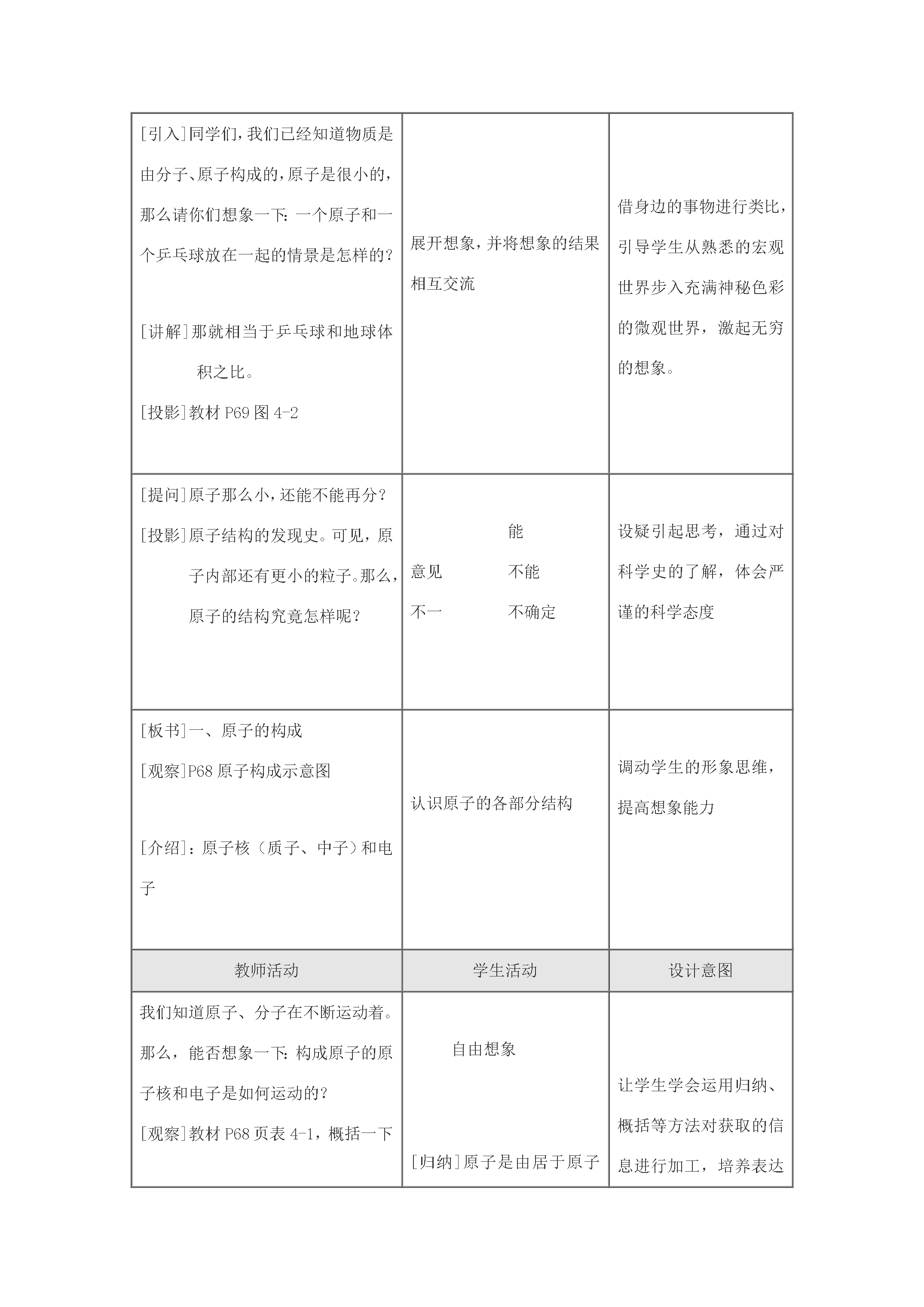
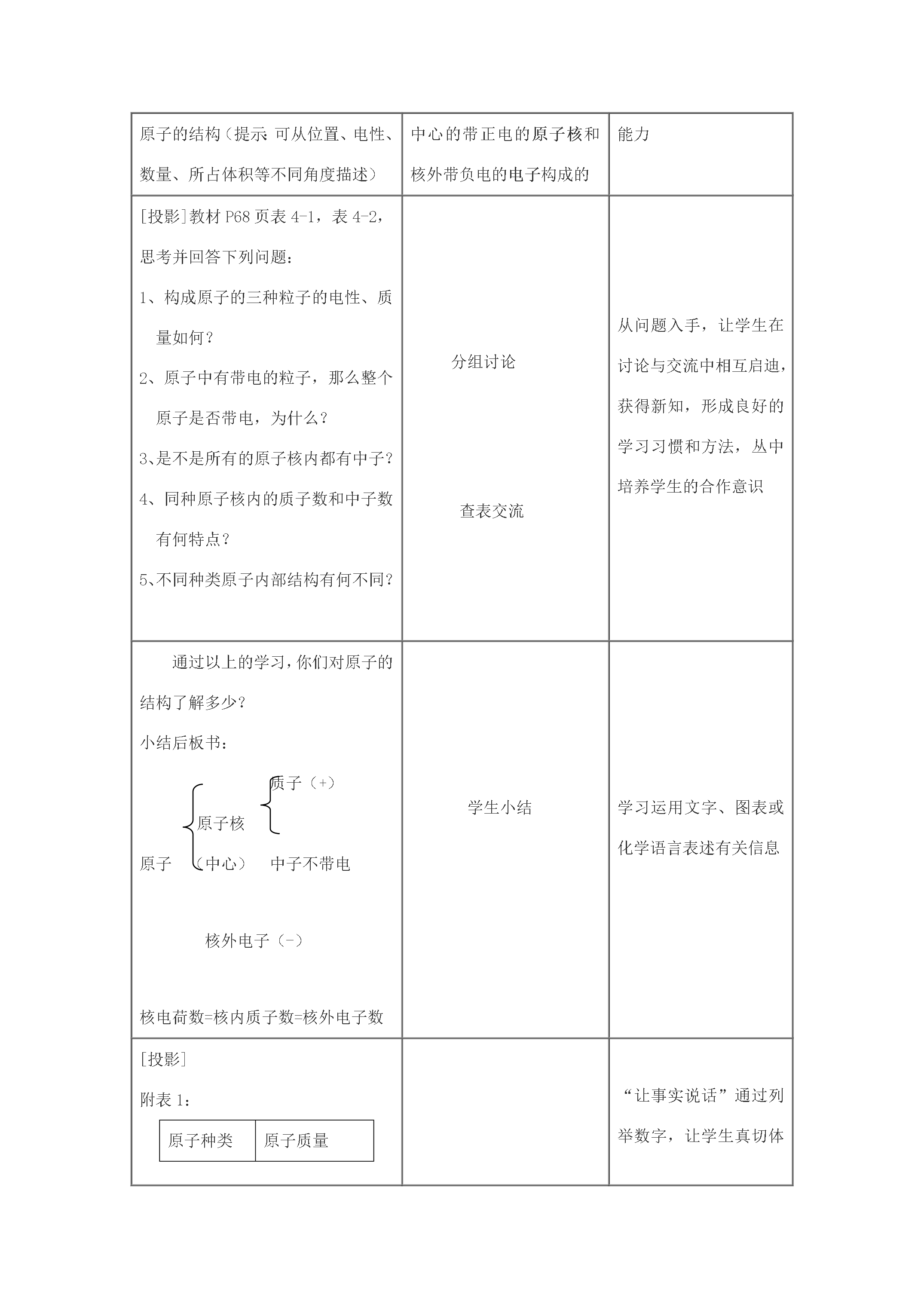
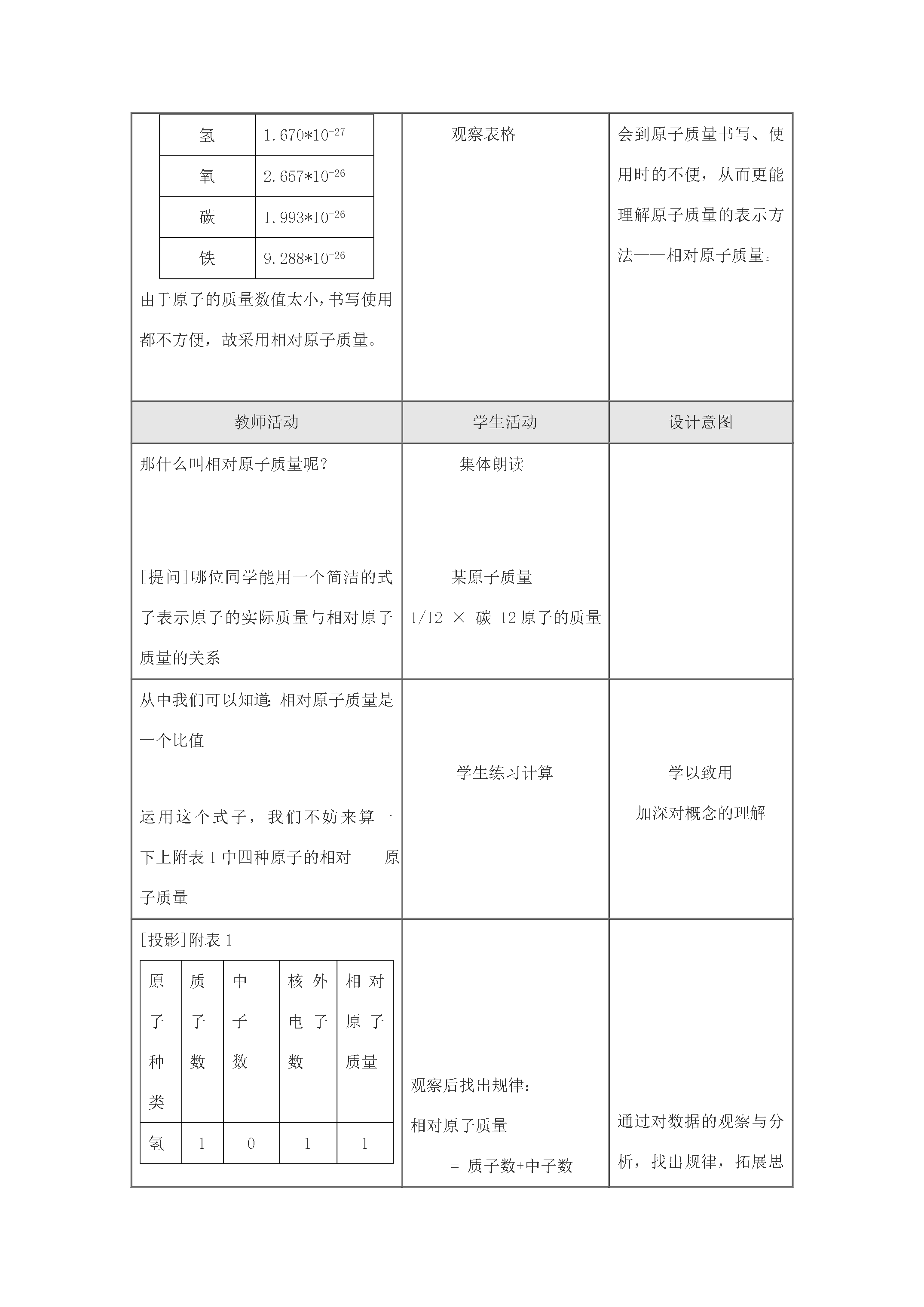
课题1原子的构成一、教学目标知识与技能1、了解原子是由质子、中子和电子构成的2、初步了解相对原子质量的概念并会查相对原子质量表过程与方法1、充分利用教材提供的图表等资料借助模型多媒体等教学手段化抽象为直观初步学会运用类比、想象、归纳、概括等方法获取的信息2、通过讨论与交流启发学生的思维逐步养成良好的学习习惯和学习方法情感态度与价值观1、激发学生对微观世界的探究欲和学习化学的兴趣2、对学生进行世界的物质性、物质的可分性的辨证唯物主义观点的教育

九年级化学上册:4.1原子的构成教案2 人教新课标.doc
九年级化学原子的构成(2)教学目标1.知识与技能(1)了解原子是由质子、中子和电子构成的;(2)初步了解相对原子质量的概念并会查相对原子质量表。2.过程与方法(1)充分利用教材提供的图、表等资料借助模型多媒体等教学手段化抽象为直观初步学会运用类比、想像、归纳、概括等方法对获取的信息进行加工;(2)通过讨论与交流启发学生的思维逐步养成良好的学习习惯和学习方法。3.情感、态度与价值观(1)激发学生对微观世界的探究欲和学习化学的兴趣;

九年级化学上册 4.1 原子的构成教案1 人教新课标版.doc
课题1原子的构成教学目标:1、知识与技能:1)了解原子是由质子、中子和电子构成的;2)初步了解相对原子质量的概念并会查相对原子质量表。2、认识与过程:培养学生观察能力分析综合能力和抽象思维能力。3、情感与价值观:进行世界的物质性、物质的可分性的辨证唯物主义观点的教育结合张青莲教授的卓越贡献资料对学生进行爱国主义教育。重点:原子的构成。难点:相对原子质量的概念形成。教学方法:情境教学法、课堂讨论法。教学手段:多媒体课件教学思路:由于在现阶段的教学条件下原子这种微观粒子既看不见也摸不
