
课件-全国-2015_高效课堂宝典训练2016九年级化学上册 第2单元 课题3 制取氧气课件3 (新版)新人教版.ppt

代瑶****zy









亲,该文档总共20页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

课件-全国-2015_高效课堂宝典训练2016九年级化学上册 第2单元 课题3 制取氧气课件3 (新版)新人教版.ppt
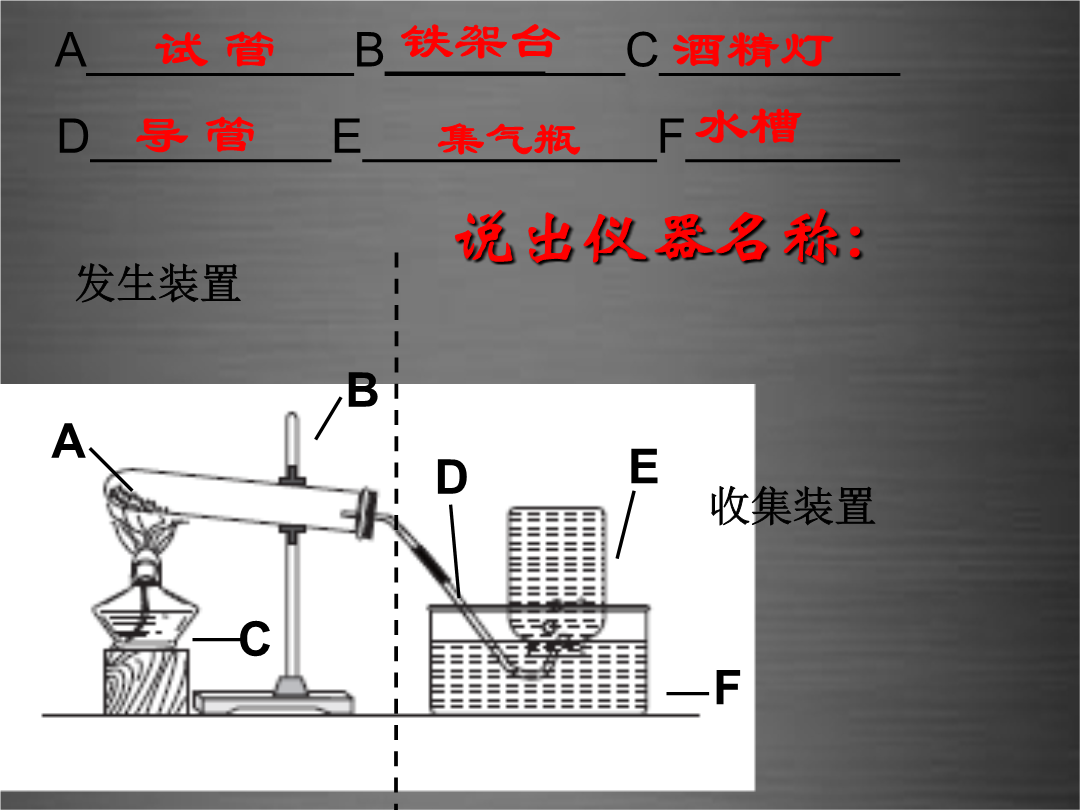
1.了解实验室用氯酸钾制取氧气的主要方法和原理;2.掌握实验室制取氧气的仪器选用、连接、检查装置气密性,实验步骤、注意事项等。3.掌握分解反应及其特征4.氧气的工业制法回忆、复习实验室用加热高锰酸钾制取氧气的仪器装置A__________B_________C_________D_________E___________F________氯酸钾氯化钾+氧气2、发生装置:由于反应物是固体,反应需要加热,所以选择制备气体的装置。3、收集装置:由于氧气不易溶于水,且不与水发生化学反应,所以可以选择

课件-全国-2015_高效课堂宝典训练2016九年级化学上册 第2单元 课题3 制取氧气课件2 (新版)新人教版.ppt
1.了解实验室用过氧化氢制取氧气的主要方法和原理;2.掌握实验室制取氧气的仪器选用、连接、检查装置气密性,实验步骤、注意事项等。3.了解催化剂,知道催化剂的特征,催化剂在化学反应中起催化作用复习实验室用高锰酸钾制取氧气的主要方法和原理;探究:分解过氧化氢溶液制取氧气中二氧化锰的作用现象(2):向上述试管中,加入少量二氧化锰,把带火星的木条伸入试管。观察发生的现象。过氧化氢水+氧气实验步骤:①查:检查装置的______________性。②装:向锥形瓶中装入固体催化剂__________________,塞

课件-全国-2015_高效课堂宝典训练2016九年级化学上册 第2单元 课题3 制取氧气课件1 (新版)新人教版.ppt
情景引入:氧气的用途1.了解实验室用高锰酸钾制取氧气的主要方法和原理;2.掌握实验室制取氧气的仪器选用、连接、检查装置气密性,实验步骤、注意事项等。阻止高锰酸钾固体随氧气气流进入导管,导致导管阻塞。A__________B_________C_________D_________E___________F________2、发生装置:由于反应物是固体,反应需要加热,所以选择制备气体的装置。3、收集装置:由于氧气不易溶于水,且不与水发生化学反应,所以可以选择收集气体的装置。由于氧气的密度比空气大,

课件-全国-2015_高效课堂宝典训练2016九年级化学上册 第2单元 课题2 氧气课件2 (新版)新人教版.ppt
学习目标:1.通过实验掌握氧气的化学性质学会观察描述实验现象2.化合反应和氧化反应知识点1:氧气的性质实验编号1、反应物是两种,生成物是一种。氧化反应原理:铁粉和空气中氧气缓慢反应,持续放热。缓慢氧化——铁生铁食物腐烂产生的黄曲霉素是一种致癌物质森林火灾产生的原因之一:由于阳光的辐射强烈,植物枯败或泥炭层发生高热自燃课堂小结:【例1】:(2015年天津)下列说法正确的是()A.木炭燃烧后生成红色固体B.镁条在空气中燃烧发出耀眼白光C.红磷在空气中燃烧产生大量白雾D.铁丝伸入盛有氧气的集气瓶中剧

课件-全国-2015_高效课堂宝典训练2016九年级化学上册 第2单元 课题2 氧气课件1 (新版)新人教版.ppt
说是宝,真是宝,动物植物离不了;看不见。摸不着.越往高处越稀少——打一化学物质名称。学习目标:1、认识氧气主要的物理性质2、观察和描述木炭、铁丝、硫等在空气中或氧气中燃烧的现象,从中归纳出氧气的化学性质1、空气中氧气的体积分数是______;2、物理性质包括:________________________________________________________________________________________________。知识点1:氧气的物理性质:氧气贮存在天蓝色
