
(新课标Ⅲ)高考化学 专题二十 化学实验基本方法课件-人教版高三全册化学课件.pptx

和裕****az





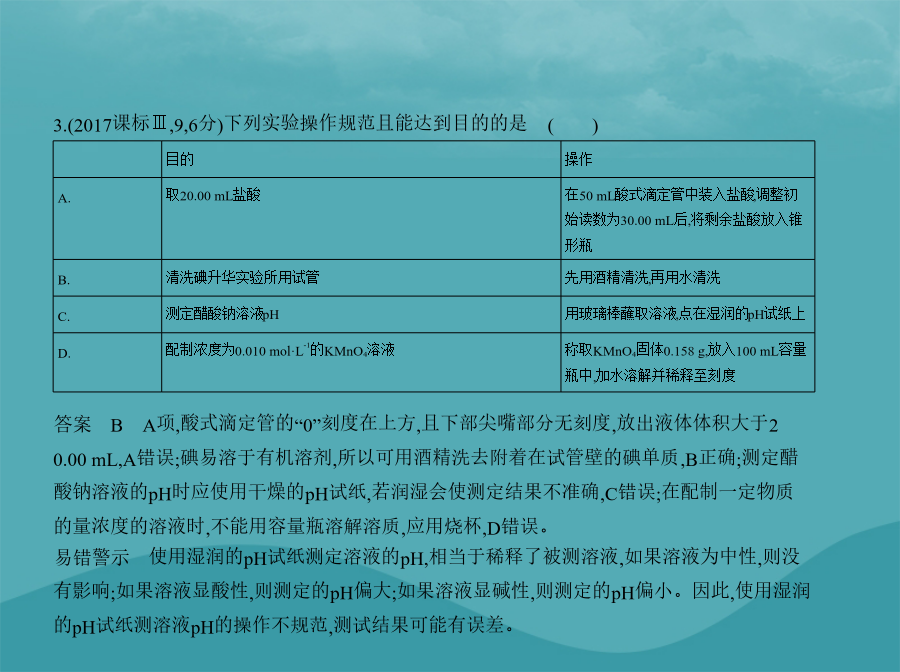

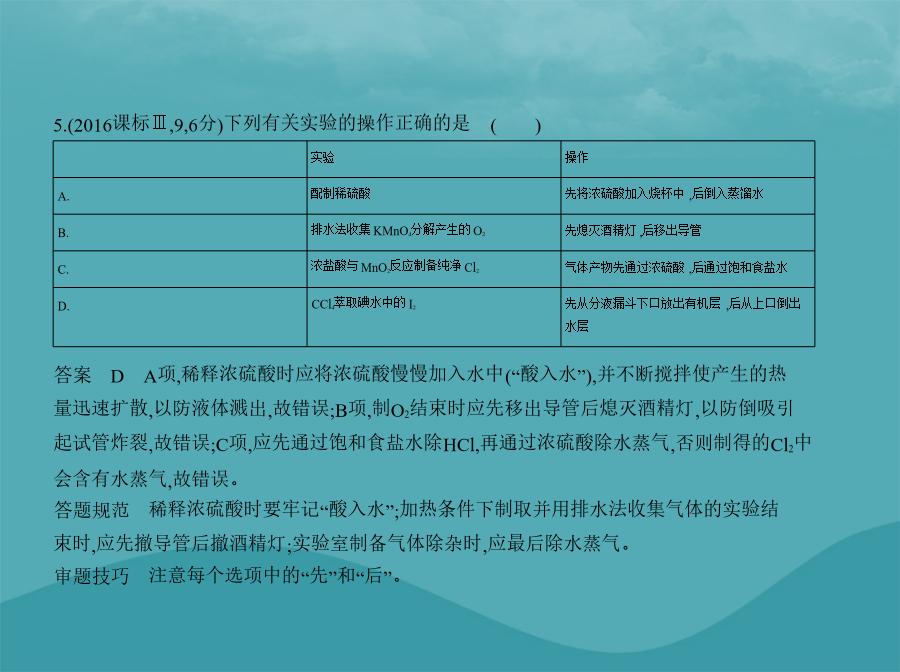
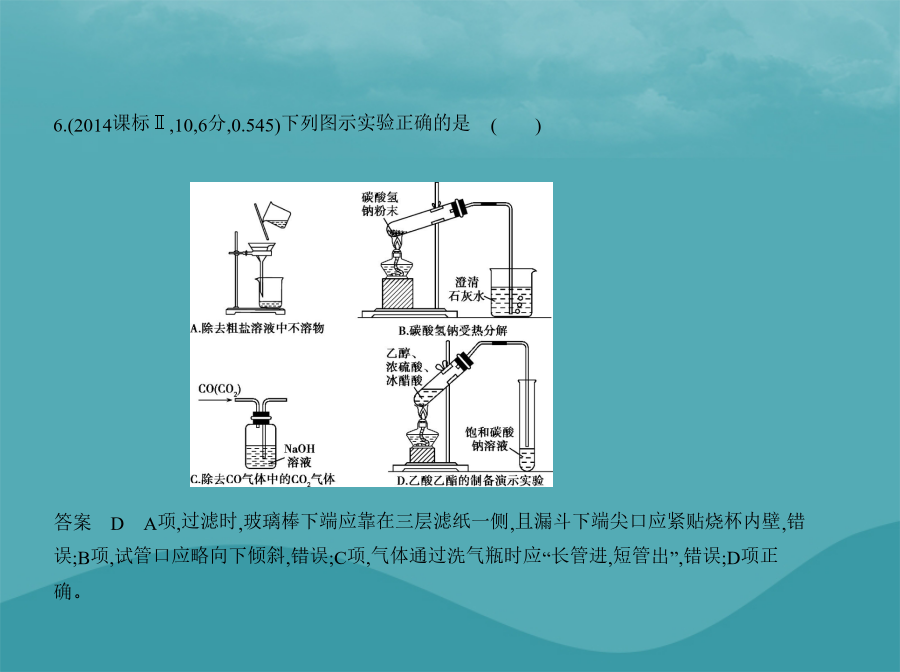

亲,该文档总共84页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

(新课标Ⅲ)高考化学 专题二十 化学实验基本方法课件-人教版高三全册化学课件.pptx
专题二十化学实验基本方法A组统一命题·课标卷题组考点一常见仪器的使用(2014课标Ⅰ126分0.747)下列有关仪器使用方法或实验操作正确的是 ()A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干B.酸式滴定管装标准溶液前必须先用该溶液润洗C.酸碱滴定实验中用待滴定溶液润洗锥形瓶以减小实验误差D.用容量瓶配溶液时若加水超过刻度线立即用滴管吸出多余液体易错警示配制一定物质的量浓度的溶液在定容完成后不可以再做其他的任何补加液体或吸出液体的操作如果发现有多加的情况只能重新配制。考点二化学实验基本操作1.

(新课标Ⅲ)高考化学 专题二十 化学实验基本方法课件-人教版高三全册化学课件.pptx
专题二十化学实验基本方法A组统一命题·课标卷题组考点一常见仪器的使用(2014课标Ⅰ,12,6分,0.747)下列有关仪器使用方法或实验操作正确的是 ()A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干B.酸式滴定管装标准溶液前,必须先用该溶液润洗C.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差D.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体易错警示配制一定物质的量浓度的溶液,在定容完成后,不可以再做其他的任何补加液体或吸出液体的操作,如果发现有多加的情况,只能重新配制。考点二化学实验基本

(新课标Ⅲ)高考化学 专题二十 化学实验基本方法课件-人教版高三全册化学课件.pptx
专题二十化学实验基本方法A组统一命题·课标卷题组考点一常见仪器的使用(2014课标Ⅰ126分0.747)下列有关仪器使用方法或实验操作正确的是 ()A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干B.酸式滴定管装标准溶液前必须先用该溶液润洗C.酸碱滴定实验中用待滴定溶液润洗锥形瓶以减小实验误差D.用容量瓶配溶液时若加水超过刻度线立即用滴管吸出多余液体易错警示配制一定物质的量浓度的溶液在定容完成后不可以再做其他的任何补加液体或吸出液体的操作如果发现有多加的情况只能重新配制。考点二化学实验基本操作1.

(新课标Ⅰ)高考化学一轮复习 专题二十 化学实验基本方法课件-人教版高三全册化学课件.ppt
专题二十化学实验基本方法考点一常见仪器的使用1.(2014课标Ⅰ126分0.747)下列有关仪器使用方法或实验操作正确的是 ()A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干B.酸式滴定管装标准溶液前必须先用该溶液润洗C.酸碱滴定实验中用待滴定溶液润洗锥形瓶以减小实验误差D.用容量瓶配溶液时若加水超过刻度线立即用滴管吸出多余液体易错警示配制一定物质的量浓度的溶液在定容完成后不可以再做其他的任何补加液体或吸出液体的操作如果发现有多加的情况只能重新配制。考点二化学实验的基本操作2.(2018课标Ⅲ1

(新课标Ⅱ)高考化学一轮复习 专题二十 化学实验基本方法课件-人教版高三全册化学课件.ppt
专题二十化学实验基本方法考点一常见仪器的使用(2014课标Ⅰ126分0.747)下列有关仪器使用方法或实验操作正确的是 ()A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干B.酸式滴定管装标准溶液前必须先用该溶液润洗C.酸碱滴定实验中用待滴定溶液润洗锥形瓶以减小实验误差D.用容量瓶配溶液时若加水超过刻度线立即用滴管吸出多余液体答案B容量瓶不能放在烘箱中烘干否则其容积可能受温度的影响而发生改变A错误;滴定管在盛放溶液前必须用所盛溶液润洗2~3次B正确;中和滴定时若用待滴定溶液润洗锥形瓶必然导致标
