
乙酰乙酸乙酯的制备.docx

快乐****蜜蜂








在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

乙酰乙酸乙酯的制备.docx
乙酰乙酸乙酯的制备实验目的了解乙酰乙酸乙酯的制备原理和方法掌握无水操作及减压蒸馏实验原理含a-活泼氢的酯在强碱性试剂(如Na.NaNAH2.三苯甲基钠或格式试剂)存在下,能与另一分子酯发生claisen酯缩合反应,生成ß-羰基酸酯。乙酰乙酸乙酯就是通过这一反应制备的。虽然反应中使用金属钠作缩合剂,但真正的催化剂是钠与乙酸乙酯中残留的乙醇作用产生的乙醇钠仪器与试剂主要仪器:100ml圆底烧瓶,干燥管,冷凝管,分液漏斗,加热装置,减压蒸馏装置主要试剂:乙酸乙酯12.5g(13.8ml0.19mol)金属钠1.
乙酰乙酸乙酯的制备.pdf
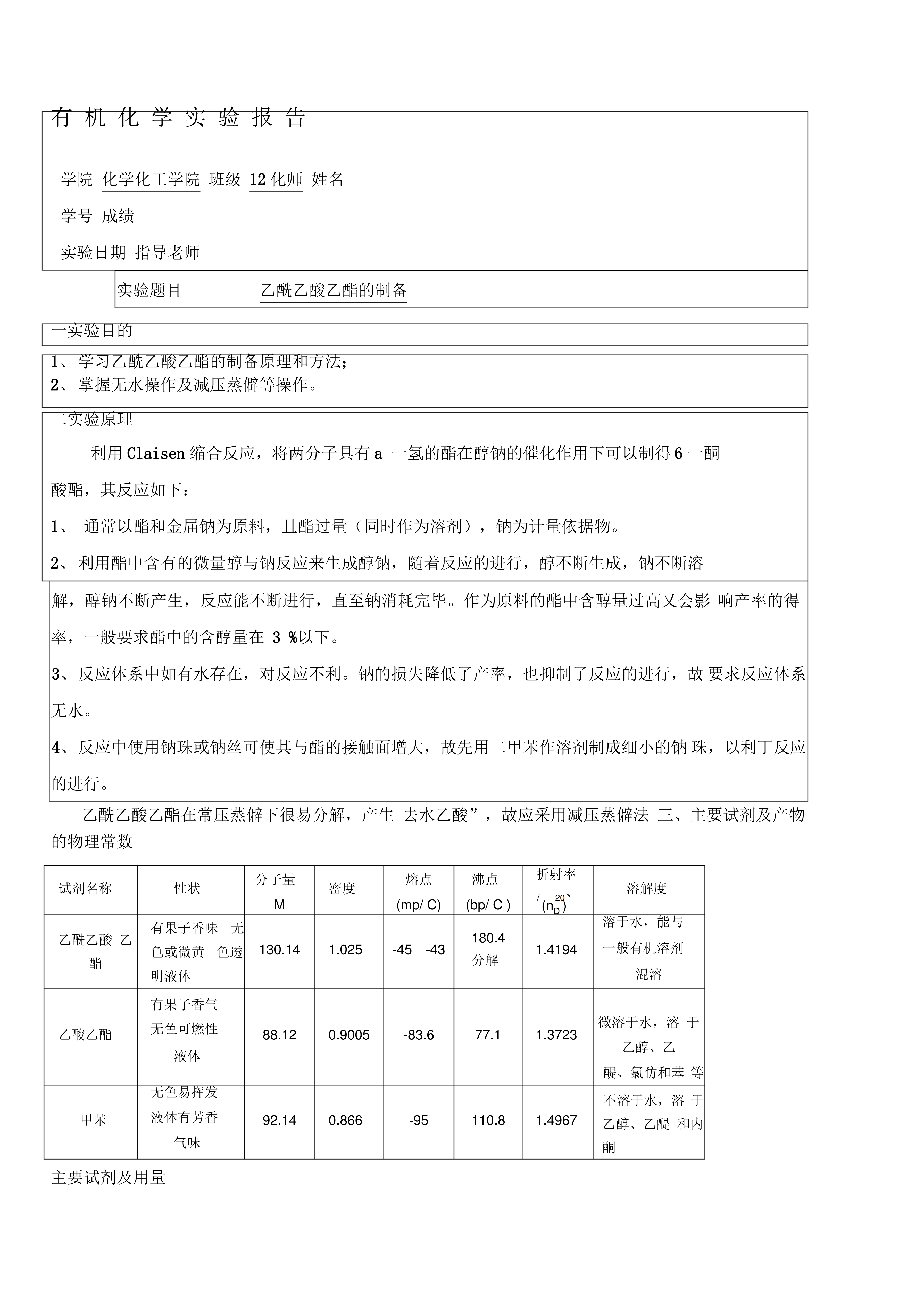
有机化学实验报告学院化学化工学院班级12化师姓名学号成绩实验日期指导老师实验题目________乙酰乙酸乙酯的制备___________________________一实验目的1、学习乙酰乙酸乙酯的制备原理和方法;2、掌握无水操作及减压蒸僻等操作。二实验原理利用Claisen缩合反应将两分子具有a一氢的酯在醇钠的催化作用下可以制得

乙酰乙酸乙酯制备.docx
乙酰乙酸乙酯的制备摘要:本实验是为了了解Claisen酯缩合反应的机理和应用,熟悉在酯缩合反应中金属钠的应用和操作注释,复习液体干燥和减压蒸馏操作,并且了解乙酰乙酸乙酯的性质及用途。关键词:乙酰乙酸乙酯、制备、Claisen酯缩合反应前言:乙酰乙酸乙酯是无色至淡黄色澄清液体,微溶于水,易溶于乙醚、乙醇有刺激性气味。可燃,遇明火、高温或接触氧化剂有发生燃烧的危险有醚样和苹果似的香气。广泛应用于食品香精中,主要用于调配苹果、杏、桃等食用香精。制药工业用于制造氨基比林、维生素B等。染料工业用于合成染料的原料和用

乙酰乙酸乙酯的制备.docx
有机化学实验报告学院化学化工学院班级12化师姓名学号成绩实验日期指导老师实验题目乙酰乙酸乙酯的制备一实验目的1、学习乙酰乙酸乙酯的制备原理和方法;2、掌握无水操作及减压蒸馏等操作。二实验原理利用Claisen缩合反应,将两分子具有α-氢的酯在醇钠的催化作用下可以制得β-酮酸酯,其反应如下:1、通常以酯和金属钠为原料,且酯过量(同时作为溶剂),钠为计量依据物。2、利用酯中含有的微量醇与钠反应来生成醇钠,随着反应的进行,醇不断生成,钠不断溶解,醇钠不断产生,反应能不断进行,直至钠消耗完毕。作为原料的酯中含醇量

乙酰乙酸乙酯的制备.ppt
实验4减压蒸馏一、实验目的二、实验原理三、主要仪器与试剂减压蒸馏装置由蒸馏瓶、克氏蒸馏头、毛细管、温度计及冷凝管、接受器等组成。四、实验步骤3、加料、抽真空、加热蒸馏检查仪器不漏气后,加入待蒸的液体,量不要超过蒸馏瓶的一半,关好安全瓶上的活塞,开动油泵,调节毛细管导入的空气量,以能冒出一连串小气泡为宜。当压力稳定后,开始加热。液体沸腾后,应注意控制温度,并观察沸点变化情况。待沸点稳定时,转动多尾接液管接受馏分,蒸馏速度以0.5~1滴/秒为宜。4、结束蒸馏蒸馏完毕,除去热源,慢慢旋开夹在毛细管上的橡皮管的螺
