
-相平衡和相图.ppt

lj****88







亲,该文档总共217页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

相平衡和相图.ppt
第六章相平衡和相图合金相图是表示合金在热力学平衡条件下相或状态与温度、成分之间关系的图形,又称为状态图或平衡图。合金相图的用途:①利用相图可以知道各种成分的合金在不同温度下有哪些相及各相的相对含量和成分,以及温度变化时发生的相的变化。这种相与相之间的转变称为相变。②利用相图可以分析平衡状态下合金的组织,并进而预测性能。③合金相图还是制订合金熔炼、铸造、锻造、焊接和热处理工艺的重要依据。6.1相平衡及其研究方法一、相平衡的基本概念1、系统通常,我们把选择的研究对象称为系统。而系统以外的一切物质都称为环境。当

-相平衡和相图.ppt
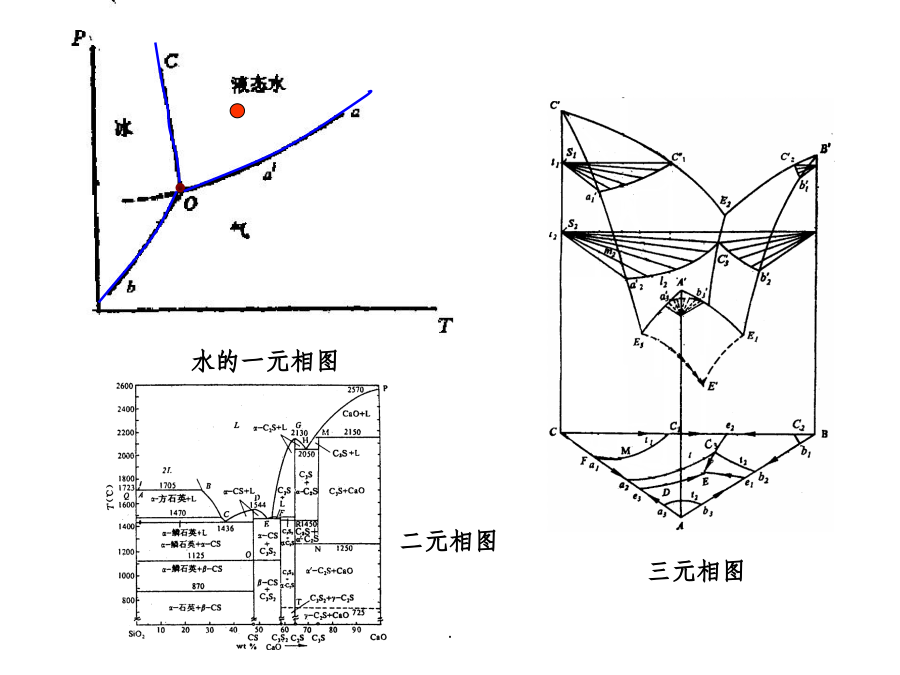
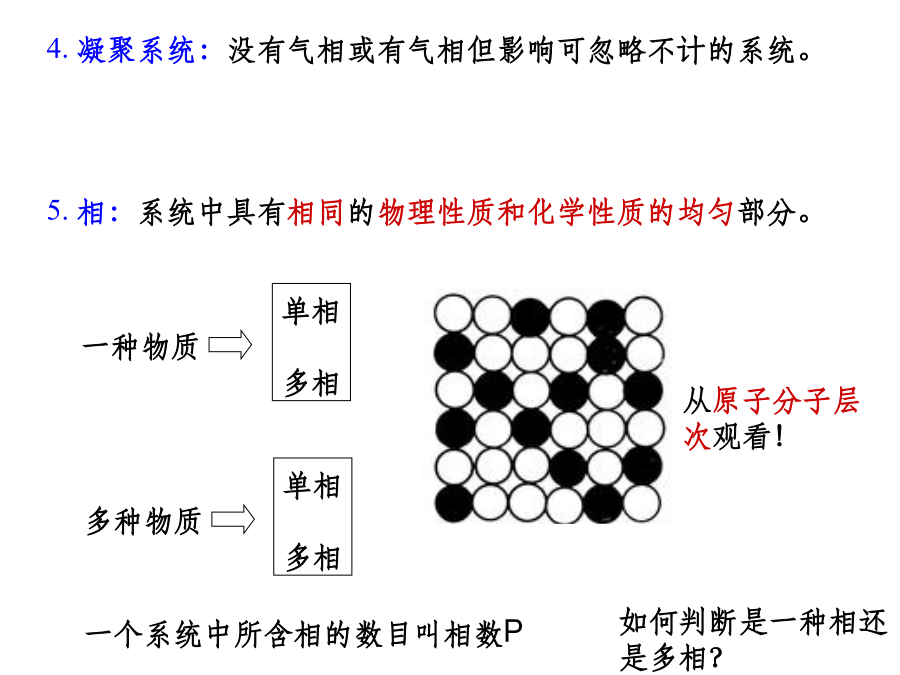
第六章相平衡和相图浮冰二元相图6.1相平衡及其研究方法一、相平衡基本概念1.系统:研究的对象,其他为环境2.平衡态:一定条件下,系统的各种性质不随时间而改变,处于热力学平衡状态。3.介稳态:非平衡态,热力学不平衡,但因动力学不满足而存在4.凝聚系统:没有气相或有气相但影响可忽略不计的系统。5.相:系统中具有相同的物理性质和化学性质的均匀部分。常见的几种固体:二、相律假设一系统中有S种化学物质,在平衡条件下形成P种物相,每种相中都有S种化学物质。则总变量数:P(S-1)+2多相平衡时,每种物质在各相中的化学

相平衡和相图.ppt
章相平衡和相图合金相图是表示合金在热力学平衡条件下相或状态与温度、成分之间关系的图形,又称为状态图或平衡图。合金相图的用途:①利用相图可以知道各种成分的合金在不同温度下有哪些相及各相的相对含量和成分,以及温度变化时发生的相的变化。这种相与相之间的转变称为相变。②利用相图可以分析平衡状态下合金的组织,并进而预测性能。③合金相图还是制订合金熔炼、铸造、锻造、焊接和热处理工艺的重要依据。6.1相平衡及其研究方法一、相平衡的基本概念1、系统通常,我们把选择的研究对象称为系统。而系统以外的一切物质都称为环境。当外界

相平衡与相图.ppt
第六章相平衡与相图主要内容★系统阐述相图的基本原理★结合实际介绍相图在无机非金属材料的研究和生产实践中的具体应用。第一节硅酸盐系统相平衡特点一、热力学平衡态和非平衡态1.平衡态相图即平衡相图,反应的是体系所处的热力学平衡状态,即仅指出在一定条件下体系所处的平衡态(其中所包含的相数,各相的状态、数量和组成),与达平衡所需的时间无关。2.介稳态即热力学非平衡态,经常出现于硅酸盐系统中。如:根据吉布斯相律f=c-p+2f-自由度数c-独立组分数p-相数2-温度和压力外界因素硅酸盐系统的相律为:f=c-p+1(i

相平衡与相图.ppt
材料的性能相图8.1相平衡与吉布斯相律2.组元(Component)组元通常是指系统中每一个可以单独分离出来,并能独立存在的化学纯物质,在一个给定的系统中,组元就是构成系统的各种化学元素或化合物。3.相平衡在某一温度下,系统中各个相经过很长时间也不互相转变,处于平衡状态,这种平衡称为相平衡。处于热力学平衡状态的系统中自由度数、组元数、相数和外界影响因素之间的关系定律,通常简称为相律。F=C-P+n只考虑温度和压力对系统平衡状态的影响:F=C-P+2凝聚系统:F=C-P+1式中:F是自由度数;C是组成材料系
