
大化材102原子核外电子运动状态(1).ppt

lj****88







亲,该文档总共32页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

大化材102原子核外电子运动状态(1).ppt
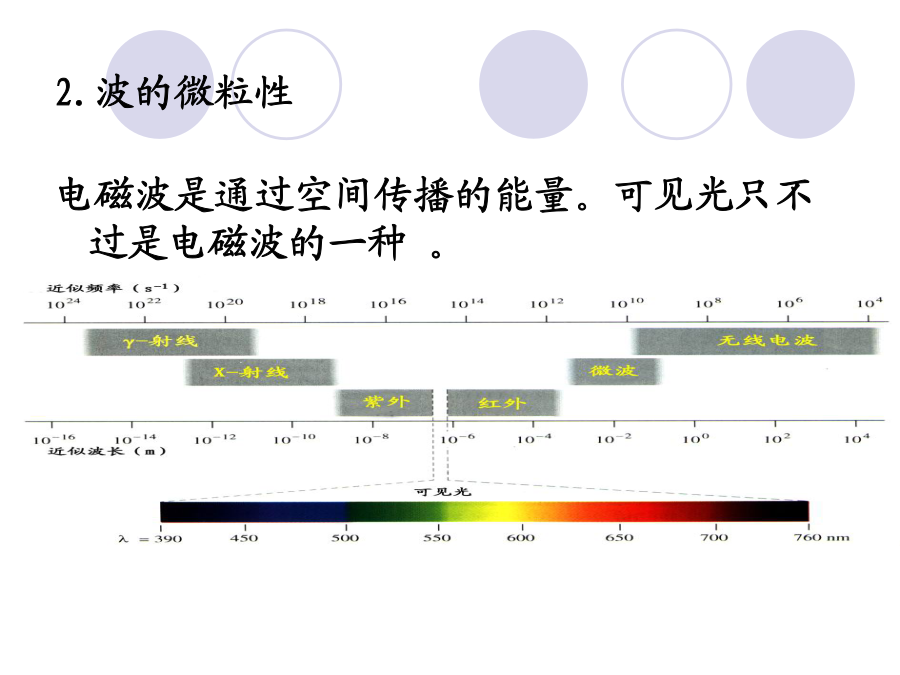
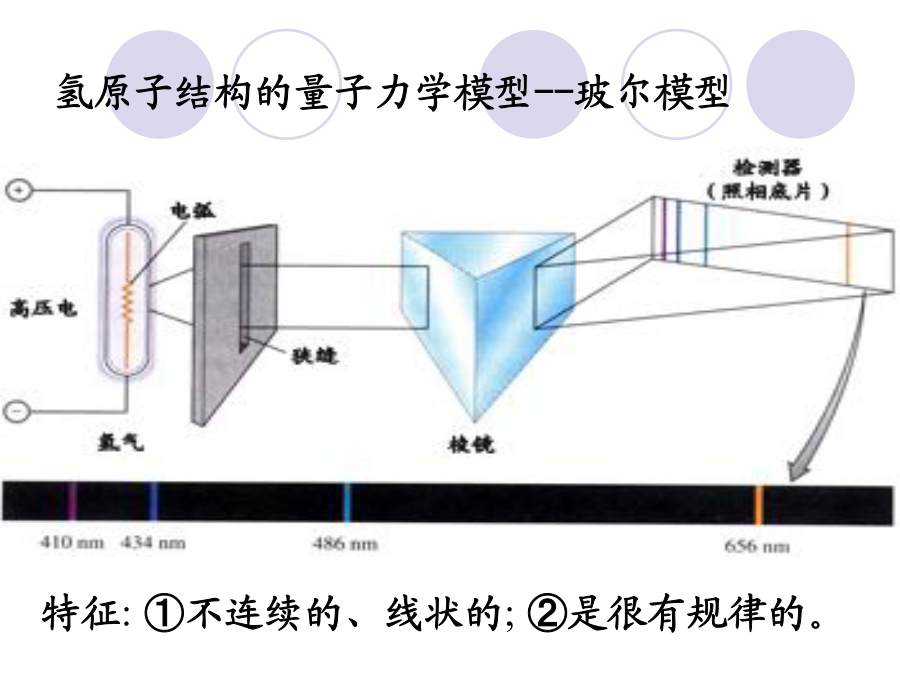
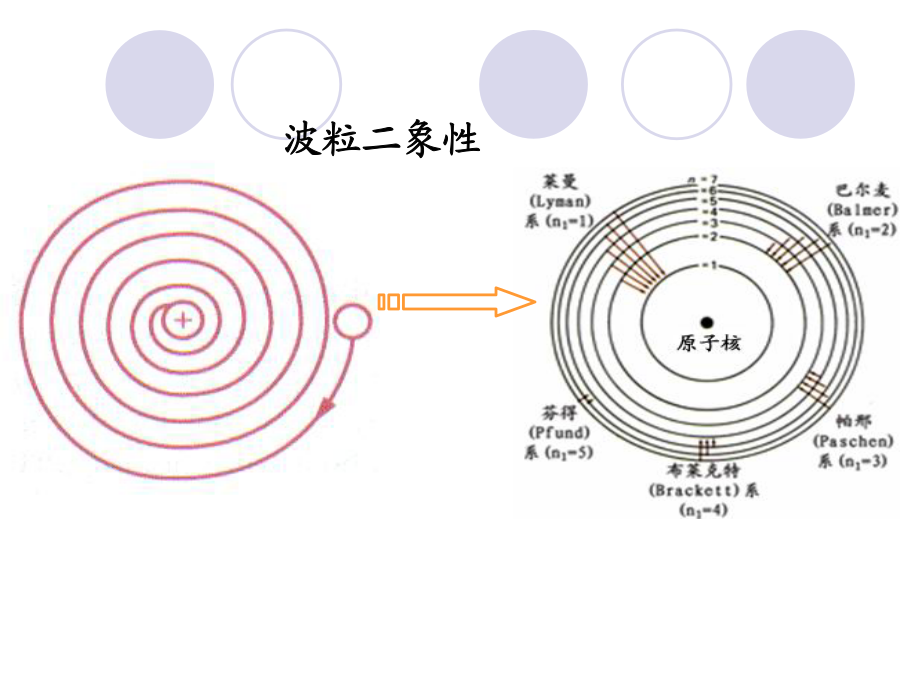
第二章物质的结构和材料的性质一、电子的波粒二象性1.经典物理学的原子结构的概念2.波的微粒性电磁波在有些情况下表现出连续波的性质,另一些情况下则更像单个微粒的集合体,后一种性质叫作波的微粒性。普朗克提出了当时物理学界一种全新的概念普朗克方程:E=hv(黑体辐射时能量密度按频率分布)1905年,爱因斯坦(EinsteinA)成功地将能量量子化概念扩展到光本身,解释了光电效应。3.电子的波粒二象性氢原子结构的量子力学模型--玻尔模型波粒二象性Bohr(1)解释了H及He+、Li2+、B3+的原子光谱(2)不能

大化材102原子核外电子运动状态.ppt
第二章物质的结构和材料的性质一、电子的波粒二象性1.经典物理学的原子结构的概念2.波的微粒性电磁波在有些情况下表现出连续波的性质,另一些情况下则更像单个微粒的集合体,后一种性质叫作波的微粒性。普朗克提出了当时物理学界一种全新的概念普朗克方程:E=hv(黑体辐射时能量密度按频率分布)1905年,爱因斯坦(EinsteinA)成功地将能量量子化概念扩展到光本身,解释了光电效应。3.电子的波粒二象性氢原子结构的量子力学模型--玻尔模型波粒二象性Bohr(1)解释了H及He+、Li2+、B3+的原子光谱(2)不能

原子核外电子的运动状态.docx
原子核外电子排布【学习目标】知识与技能了解元素原子核外电子排布的基本规律会用原子结构示意图熟练表示1——18号元素,惰性气体,部分第四,五周期的主族元素的电子排布式,在必修1的基础上,进一步认识卢瑟福和玻尔的原子结构模型,了解原子核外电子的运动状态。在原子核外电子排布基本规律的基础上,进一步了解表述电子运动状态的四个要素,了解电子云,知道1——36号元素的电子排布式,轨道表示式,价电子排式。过程与方法学习运用实验,查阅资料等多种手段获取信息,运用比较、分类、归纳等方法对信息进行加工。情感态度与价值观体会化
量子力学对原子核外电子运动状态的描述.pptx
量子力学对原子核外电子运动状态的描述[基础·初探]教材整理1原子轨道1.电子层2.能级在同一电子层中,电子所具有的能量可能不同,所以同一电子层可分成不同的能级,用s、p、d、f表示。3.原子轨道(1)概念:原子中的单个电子的空间运动状态。(2)n值所对应的能级和原子轨道的情况4.自旋运动状态处于同一原子轨道上的电子自旋运动状态只有两种,分别用符号“↑”和“↓”表示。练习:(1)离核越近的电子,能量越低。()(2)第n电子层共有n个能级,n2个原子轨道。()(3)每个轨道容纳的2个电子自旋方向不固定。()(

量子力学对原子核外电子运动状态的描述.docx
量子力学对原子核外电子运动状态的描述1.下列有关认识正确的是()A.各能级的原子轨道数按s、p、d、f顺序依次为1、3、5、7B.各电子层的能级都是从s能级开始至f能级结束C.各电子层含有的能级数为n-1D.各电子层含有的电子数为2n2个【解析】各电子层的能级数等于其所处的电子层数,即当n=1时,它只有一个s能级,当n=2时,它有两个能级:s能级和p能级,所以B、C均错误;而每个电子层最多容纳的电子数为2n2个。【答案】A2.某元素原子的核外有三个电子层,最外电子层有4个电子,该原子核内的质子数为()A.
