
无机材料科学基础章学习教案.pptx

快乐****蜜蜂








亲,该文档总共115页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

无机材料科学基础章学习教案.pptx
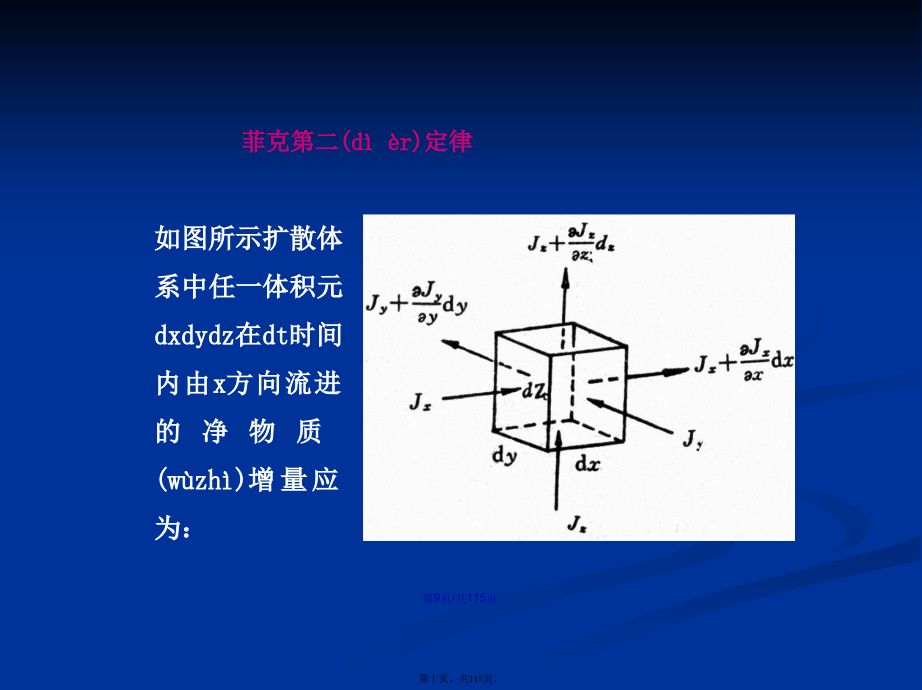
会计学§7-1晶体中扩散的基本(jīběn)特点与宏观动力学方程一、基本(jīběn)特点二、扩散(kuòsàn)动力学方程Dynasticequationofdiffusion1、稳定(wěndìng)扩散和不稳定(wěndìng)扩散2、菲克定律(dìnglǜ)菲克第一(dìyī)定律对于(duìyú)一般非立方对称结构晶体,扩散系数D为二阶张量,上式可写为:对于大部分的玻璃或各向同性的多晶陶瓷材料,可认为(rènwéi)扩散系数D将与扩散方向无关而为一标量菲克第二(dìèr)定律同理在y、z方向流进

无机材料科学基础烧结学习教案.pptx
无机材料科学基础(jīchǔ)烧结234567891011121314151617181920212223242526272829303132333435363738394041424344454647484950515253545556575859606162636465666768697071727374757677787980818283848586878889909192

无机材料科学基础固溶体学习教案.pptx
第一节固溶体的分类(fēnlèi)一、按杂质原子(yuánzǐ)在固溶体中的位置可分为:1、置换式固溶体,亦称替代固溶体,其溶质原子(yuánzǐ)位于点阵结点上,替代(置换)了部分溶剂原子(yuánzǐ)。金属和金属形成的固溶体都是置换式的。如,Cu-Zn系中的α和η固溶体都是置换式固溶体。在金属氧化物中,主要发生在金属离子位置上的置换,如:MgO-CaO,MgO-CoO,PbZrO3-PbTiO3,Al2O3-Cr2O3等。C3S的固溶体C54S16MA2.相当于18个Si中有两个被置换。2、间隙式固

无机材料科学基础表面与界面学习教案.pptx
会计学※固体表面(biǎomiàn)的特征由于固体表面质点排列的周期(zhōuqī)重复性中断,使处于表面边界上的质点力场对称性破坏,表现出剩余的键力,这就是固体表面力场。在晶体内部,质点处在一个对称力场中。但在晶体表面,质点排列的周期(zhōuqī)性重复中断,表面上的质点一方面受到内部质点的作用,另一方面又受到性质不同的另一相中物质分子(原子)的作用,使表面质点的力场对称性被破坏,表现出剩余的键力,这就是固体表面力的来源。表面力可分为:范德华力、长程力、静电力、毛细管表面力、接触力等。456(3)静电

无机材料科学基础结晶学基础学习教案.pptx
无机(wújī)材料科学基础结晶学基础认识晶体/非晶体的过程(guòchéng):自然界存在的外形规则的物体→人工合成晶体非晶体也可以呈现出规则外形;晶体在非理想生长条件下可以呈现出不规则外形晶体现代定义:内部质点以一定周期性方式在三维空间规则排列的物质晶体学包含的主要内容///结晶学基础(jīchǔ)的主要内容主要人工(réngōng)晶体及其用途§1-1晶体(jīngtǐ)的基本概念与性质注意:晶体生长环境对其外形有影响规则(guīzé)的几何外形是内部结构决定的“晶体是物质存在的一种状态”2、空间格
