
紫外吸收光谱法.ppt

lj****88








亲,该文档总共62页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

紫外吸收光谱法.doc
第8章紫外吸收光谱法紫外-可见分子吸收光谱法(ultraviolet-visiblemolecularabsorptionspectrometry,UV-VIS),又称紫外-可见分光光度法(ultraviolet-visiblespectrophotometry)。它是研究分子吸收190~750nm波长范围内的吸收光谱。紫外-可见吸收光谱主要产生与分子价电子在电子能级间的跃迁,是研究物质电子光谱的分析方法。通过测定分子对紫外-可见光的吸收,可以用于鉴定和定量测定大量的无机化合物和有机化合物。在化学和临床实

紫外吸收光谱法.ppt
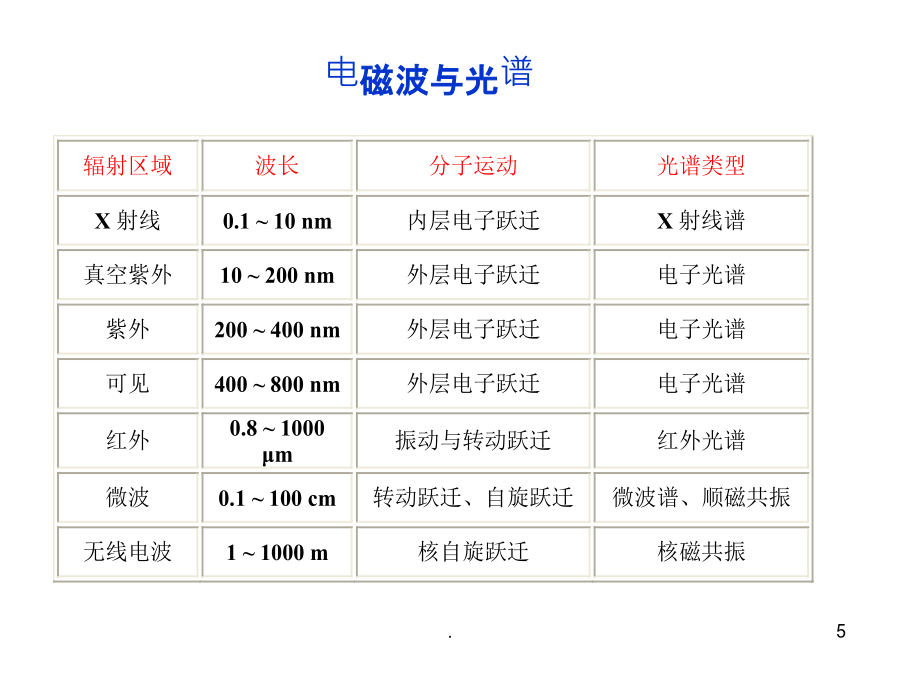
第二章紫外可见吸收光谱法紫外吸收光谱法(ultravioletandVisbleSpectroscopy,UV-Vis)是研究物质在紫外区(10--400nm)和可见光区(400-750nm)的分子吸收光谱法。分子吸收光谱图:二、分子吸收光谱的分类1、分类:远红外光谱、红外光谱和紫外-可见光谱(1)远红外光谱(分子的转动光谱)△E转=0.005-0.05eV当△E=0.005ev时(2)红外光谱(振转光谱)△E振=0.05-1eVλ=25-1.25μm(3)紫外-可见光谱(电子光谱)△E电=20-1eVλ

紫外吸收光谱法.ppt
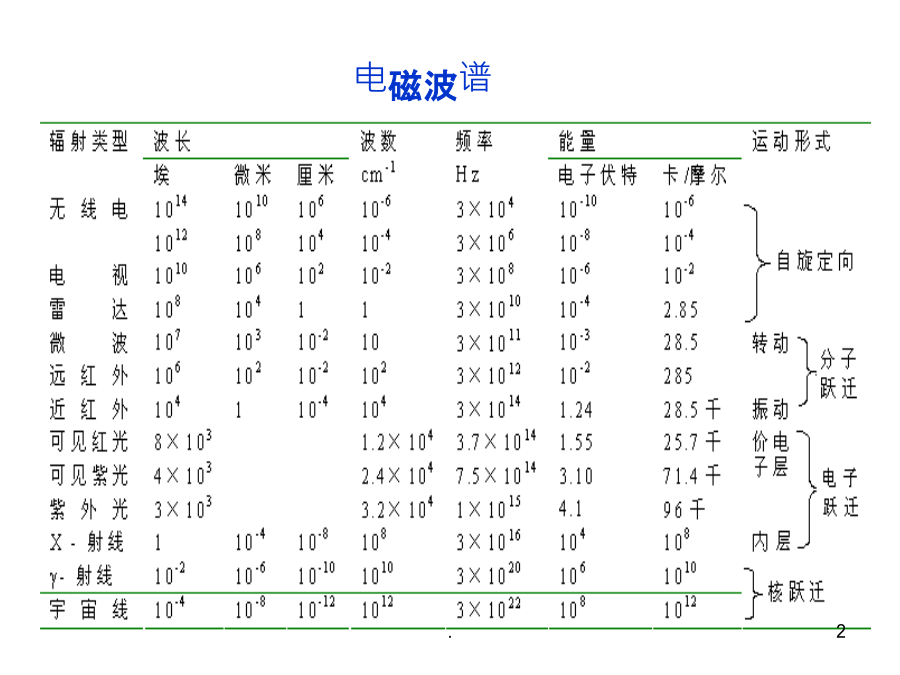
电磁波的范围包括从波长最短的γ射线到波长达数百米的无线电波的整个区域,可见光仅是其中极小的一部分。振动频率(υ),波长(λ)与光速之间的关系:υ=c/λ或c=υ×λ电磁波具有一定的能量,它可以被物质的分子或原子所吸收。电磁波的能量E与波长或频率的关系为:E=hυ=hc/λh:普朗克常数6.626×10-34J、S电磁波谱波长λ与波数υ的关系:υ=1/λ电磁波的有关数据见表2-1(P5)。§2.1-2吸收光谱的产生吸收:电磁波能量向分子或原子转移的作用。发射:处于激发态的原子或离子在外层电子发生能级跃迁时产

紫外可见吸收光谱法.ppt
HEBEINORMALUNIVERSITY,CollegeofChemistry&MaterialScienceHEBEINORMALUNIVERSITY,CollegeofChemistry&MaterialScienceHEBEINORMALUNIVERSITY,CollegeofChemistry&MaterialScienceHEBEINORMALUNIVERSITY,CollegeofChemistry&MaterialScienceHEBEINORMALUNIVERSITY,Collegeof

紫外吸收光谱法0.ppt
第十章紫外-可见分光光度法一、电磁辐射和电磁波谱高能辐射区γ射线能量最高,来源于核能级跃迁χ射线来自内层电子能级的跃迁光学光谱区紫外光来自原子和分子外层电子能级的跃迁可见光红外光来自分子振动和转动能级的跃迁波谱区微波来自分子转动能级及电子自旋能级跃迁无线电波来自原子核自旋能级的跃迁二、光学分析法及其分类续前续前三、光谱法仪器——分光光度计第二节紫外-可见吸收光谱一、紫外-可见吸收光谱的产生续前二、紫外-可见吸收光谱的电子跃迁类型图示电子跃迁类型:图示续前三、相关的基本概念图示续前续前四、吸收带类型和影响因
