
制药工艺用水验证.ppt

sy****28









亲,该文档总共67页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

制药工艺用水验证.pptx
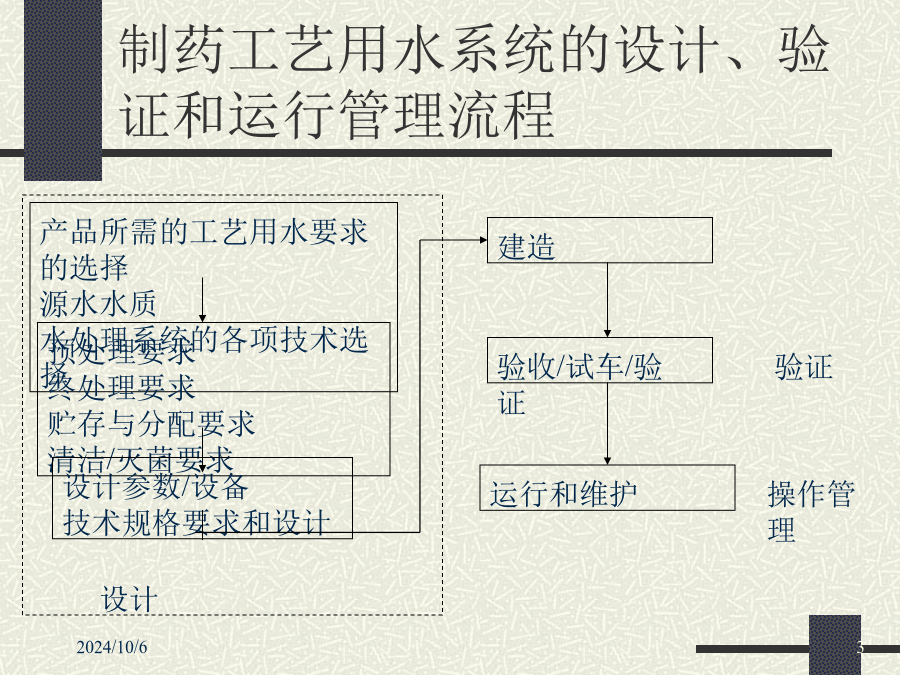
制药工艺用水的设计、验证、运行和维护微生物限度举例(2005版药典)产品所需的工艺用水要求的选择源水水质水处理系统的各项技术选择一。概述1、制药工艺用水的定义(2005版药典)1.1中国药典2005版中注射用水与纯化水的主要区别1.2纯化水和注射用水2005年版1.3中国药典2005版、欧洲药典、美国药典版关于纯化水的标准1.4制药工艺用水的定义(美国药典31版)2、各种工艺用水的用途(98版GMP/2005药典)(1)2、各种工艺用水的用途(98版GMP/2005药典)(2)注射用水:无菌

制药工艺用水验证.pptx
制药工艺用水的设计、验证、运行和维护微生物限度举例(2005版药典)产品所需的工艺用水要求的选择源水水质水处理系统的各项技术选择一。概述1、制药工艺用水的定义〔2005版药典〕1.1中国药典2005版中注射用水与纯化水的主要区别1.2纯化水和注射用水2005年版1.3中国药典2005版、欧洲药典、美国药典版关于纯化水的标准1.4制药工艺用水的定义〔美国药典31版〕2、各种工艺用水的用途(98版GMP/2005药典)〔1〕2、各种工艺用水的用途(98版GMP/2005药典)〔2〕注射用水:无菌原料药:精制工

制药工艺用水验证.ppt
制药工艺用水的设计、验证、运行和维护微生物限度举例(2005版药典)产品所需的工艺用水要求的选择源水水质水处理系统的各项技术选择一。概述1、制药工艺用水的定义(2005版药典)1.1中国药典2005版中注射用水与纯化水的主要区别1.2纯化水和注射用水2005年版1.3中国药典2005版、欧洲药典、美国药典版关于纯化水的标准1.4制药工艺用水的定义(美国药典31版)2、各种工艺用水的用途(98版GMP/2005药典)(1)2、各种工艺用水的用途(98版GMP/2005药典)(2)注射用水:无菌原料药:精制工

制药工艺用水验证.ppt
制药工艺用水的设计、验证、运行和维护微生物限度举例(2005版药典)产品所需的工艺用水要求的选择源水水质水处理系统的各项技术选择一。概述1、制药工艺用水的定义(2005版药典)1.1中国药典2005版中注射用水与纯化水的主要区别1.2纯化水和注射用水2005年版1.3中国药典2005版、欧洲药典、美国药典版关于纯化水的标准1.4制药工艺用水的定义(美国药典31版)2、各种工艺用水的用途(98版GMP/2005药典)(1)2、各种工艺用水的用途(98版GMP/2005药典)(2)注射用水:无菌

制药工艺用水验证专家讲座.pptx
制药工艺用水设计、验证、运行和维护微生物程度举例(版药典)产品所需工艺用水要求选择源水水质水处理系统各项技术选择一。概述1、制药工艺用水定义(版药典)1.1中国药典版中注射用水与纯化水主要区分1.2纯化水和注射用水年版1.3中国药典版、欧洲药典、美国药典版关于纯化水标准1.4制药工艺用水定义(美国药典31版)2、各种工艺用水用途(98版GMP/药典)(1)2、各种工艺用水用途(98版GMP/药典)(2)注射用水:无菌原料药:精制工艺用水(附录四、15)直接接触无菌原料药包装材料最终洗涤用水(附录四、15)
