
试题-全国-2008_2008浙江高三化学模拟试题汇编《探究实验1》.rar

霞英****娘子









亲,该文档总共11页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

试题-全国-2008_2008浙江高三化学模拟试题汇编《探究实验1》.rar
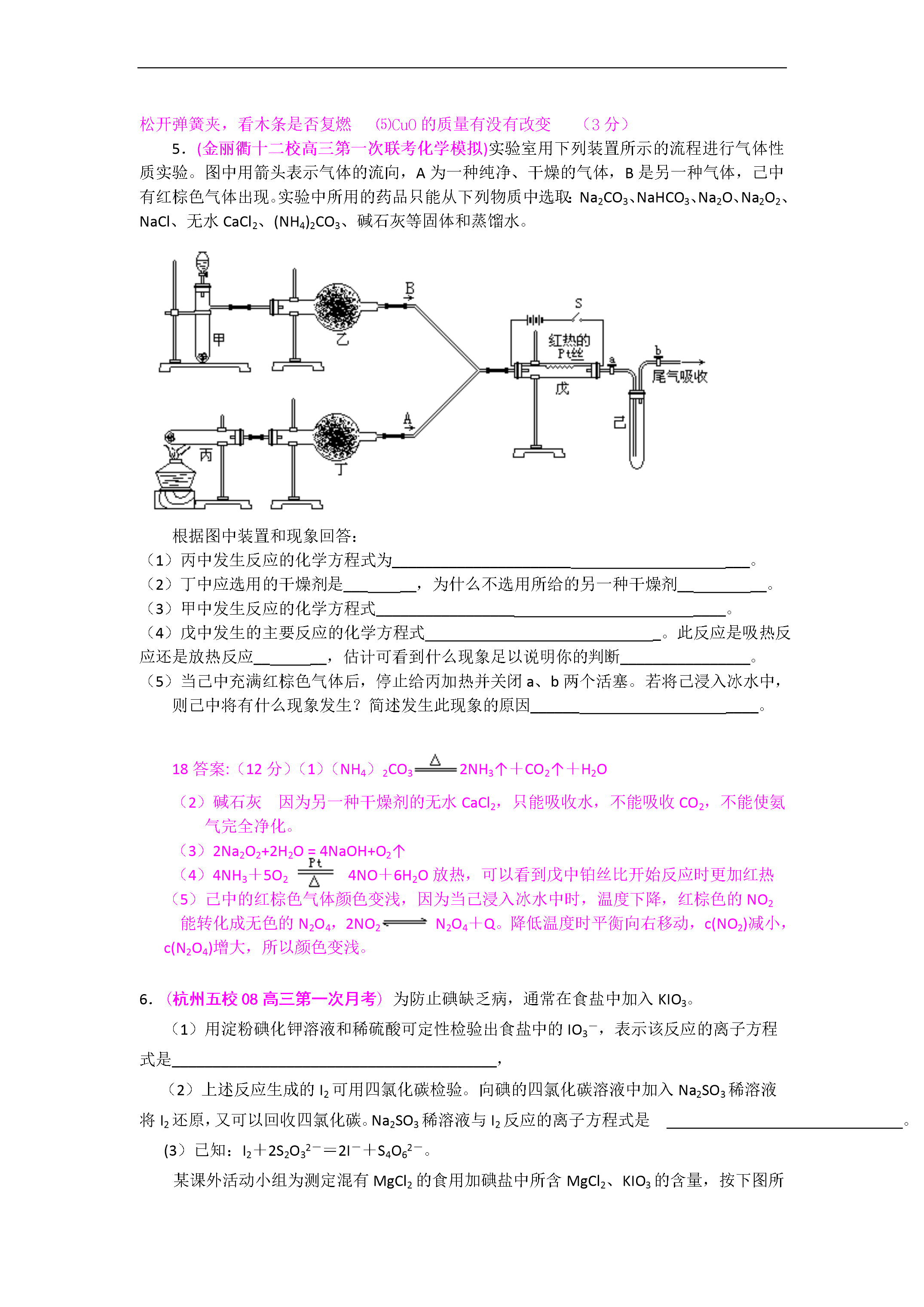
2008浙江高三模拟试题汇编《探究实验1》1.(温州市高三第二次“八校联考”)(Ⅰ)(4分)下列有关化学实验的说法正确的是(填序号)。A.滴定用的锥形瓶和滴定管都要用所盛溶液润洗B.制备(收集)任何气体开始实验前,都要首先检查装置的气密性C.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次D.测定溶液的pH时,应先将pH试纸润湿E.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸F.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭(Ⅱ)(11分)下图甲是旧教材中验证铜与浓

试题-全国-2008_2008浙江高三化学模拟试题汇编《探究实验2》.rar
2008浙江高三模拟试题汇编《探究实验2》1.(严州中学2008第二次模拟)硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2·6H2O,商品名为摩尔盐。硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:温度/℃102030405070(NH4)2SO473.075.478.081.084.591.9FeSO4·7H2O40.048.060.073.3--(NH4)2Fe(SO4)2·6H2O18.121.224.52

试题-全国-2008_2008浙江高三化学模拟试题汇编《化学实验基础》.rar
2008浙江高三模拟试题汇编《化学实验基础》1.(严州中学2008第二次模拟)下列实验中所选用的仪器或操作以及结论不合理的是。A、用托盘天平称量11.7g氯化钠晶体B、用碱式滴定管量取25mL碳酸钠溶液C、不宜用瓷坩埚灼烧氢氧化钠、碳酸钠D、测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较E、用蒸馏水和pH试纸,就可以鉴别pH相等的H2SO4和CH2COOH溶液F、量筒内液体体积正确读数为10.0mL时,全部倒入烧杯内的实际体积10.0mLG、100mL容

试题-全国-2008_2008浙江高三化学模拟试题汇编《电化学》.rar
2008浙江高三模拟试题汇编《电化学》1.(2008年杭州学军中学高考模拟测试5月)镁燃料电池以镁合金作为电池的一极,另一极充入过氧化氢,电解质溶液是酸化的氯化钠溶液,放电时总反应:Mg+2H++H2O2=Mg2++2H2O。关于该电池说法正确的是A.放电时H+在正极反应得电子B.正极方程式为:H2O2+2e-=2OH-C.镁合金为电源负极,发生氧化反应D.放电时正极的pH降低2.(温州市高三第二次“八校联考”)下列叙述不正确的是A.电解饱和食盐水时,用铁作阳极,Cl-发生氧化反应B.电解精炼铜时,纯铜作

试题-全国-2008_2008浙江高三化学模拟试题汇编《电解质溶液1》.rar
2008浙江高三模拟试题汇编《电解质溶液1》1.(温州市高三第二次“八校联考”)常温下,将V1mLc1mol/L的醋酸滴加到V2mLc2mol/L的氢氧化钠溶液中,下列结论正确的是A.若c1·V1=c2·V2,则混合液中c(CH3COO-)=c(Na+)B.若混合液的pH=7,则混合液中c(CH3COO-)>c(Na+)C.若混合液的pH=7,则混合液中c1V1>c2V2D.若混合液的pH>7,且V1=V2,则一定有c1<c22.(浙江淳安县08届高三上学期三校联考)常温时,以下4种溶液PH最小的是(A)
