
高考化学必备专题复习《氯及其化合物》.pdf

17****91










亲,该文档总共14页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

高考化学必备专题复习《氯及其化合物》.pdf
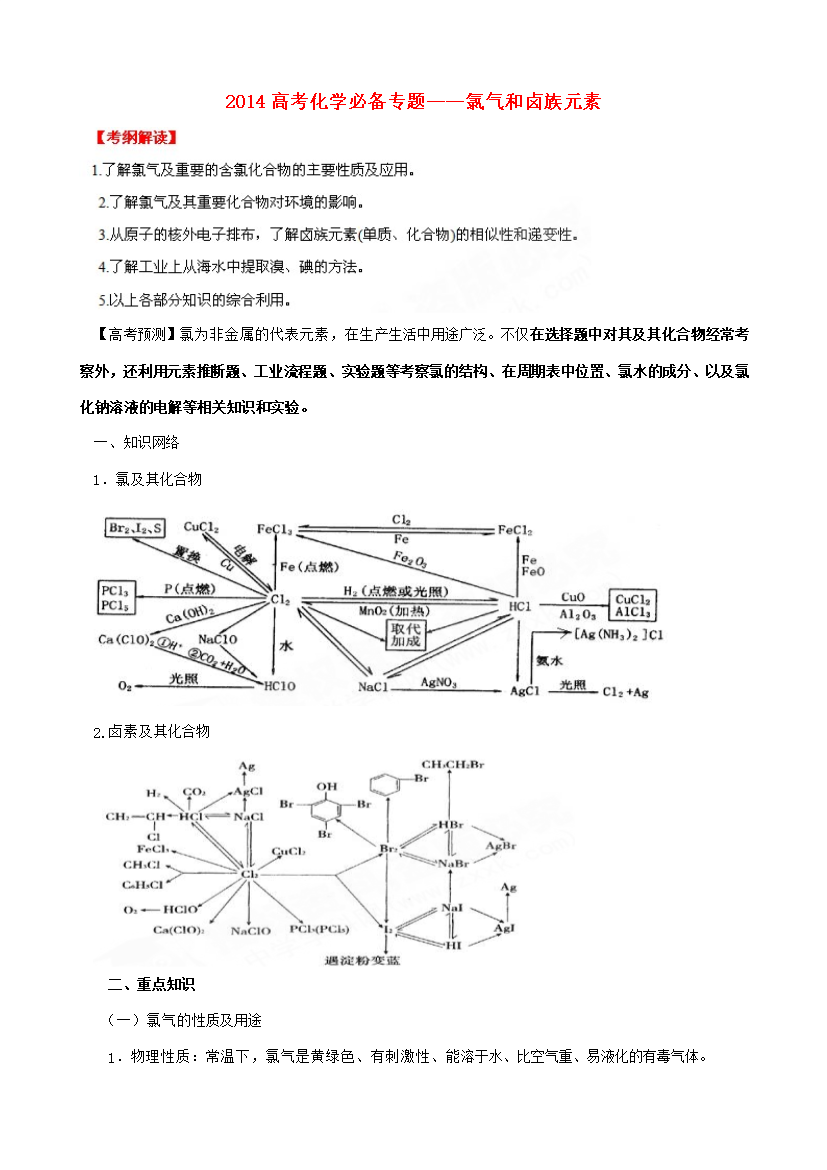
高考化学必备专题——氯气和卤族元素(附参考答案)【高考预测】氯为非金属的代表元素,在生产生活中用途广泛。不仅在选择题中对其及其化合物经常考察外,还利用元素推断题、工业流程题、实验题等考察氯的结构、在周期表中位置、氯水的成分、以及氯化钠溶液的电解等相关知识和实验。一、知识网络1.氯及其化合物2.卤素及其化合物二、重点知识(一)氯气的性质及用途1.物理性质:常温下,氯气是黄绿色、有刺激性、能溶于水、比空气重、易液化的有毒气体。2.化学性质:氯气的化学性质很活泼的非金属单质。(1)与金属反应(与变价金属反应,均

高考化学必备专题复习《氯及其化合物》.pdf
高考化学必备专题——氯气和卤族元素(附参考答案)【高考预测】氯为非金属的代表元素,在生产生活中用途广泛。不仅在选择题中对其及其化合物经常考察外,还利用元素推断题、工业流程题、实验题等考察氯的结构、在周期表中位置、氯水的成分、以及氯化钠溶液的电解等相关知识和实验。一、知识网络1.氯及其化合物2.卤素及其化合物二、重点知识(一)氯气的性质及用途1.物理性质:常温下,氯气是黄绿色、有刺激性、能溶于水、比空气重、易液化的有毒气体。2.化学性质:氯气的化学性质很活泼的非金属单质。(1)与金属反应(与变价金属反应,均

2014年高考化学 氯及其化合物必备专题复习.doc
2014高考化学必备专题——氯气和卤族元素【高考预测】氯为非金属的代表元素,在生产生活中用途广泛。不仅在选择题中对其及其化合物经常考察外,还利用元素推断题、工业流程题、实验题等考察氯的结构、在周期表中位置、氯水的成分、以及氯化钠溶液的电解等相关知识和实验。一、知识网络1.氯及其化合物2.卤素及其化合物二、重点知识(一)氯气的性质及用途1.物理性质:常温下,氯气是黄绿色、有刺激性、能溶于水、比空气重、易液化的有毒气体。2.化学性质:氯气的化学性质很活泼的非金属单质。(1)与金属反应(与变价金属反应,均是金属
2014年高考化学 氯及其化合物必备专题复习.doc
2014高考化学必备专题——氯气和卤族元素【高考预测】氯为非金属的代表元素在生产生活中用途广泛。不仅在选择题中对其及其化合物经常考察外还利用元素推断题、工业流程题、实验题等考察氯的结构、在周期表中位置、氯水的成分、以及氯化钠溶液的电解等相关知识和实验。一、知识网络1.氯及其化合物2.卤素及其化合物二、重点知识(一)氯气的性质及用途1.物理性质:常温下氯气是黄绿色、有刺激性、能溶于水、比空气重、易液化的有毒气体。2.化学性质:氯气的化学性质很活泼的非金属单质。(1)与金属反应(与变价金属反应均是金属氧化

高考化学专题复习 氯及其化合物.doc
用心爱心专心122号编辑高考化学专题复习氯及其化合物【考点指津】⒈了解Cl2的分子结构和物理性质,掌握Cl2的制备和用途;2.掌握Cl2与金属、非金属、水、碱等发生的反应;3.知道次氯酸及其盐的性质和用途。【知识在线】一、氯气的分子结构、性质和用途分子结构电子式为结构式为Cl—Cl性质物理性质黄绿色,刺激性气味有毒气体,易液化,能溶于水(1∶2)化学性质具有强氧化性,能氧化许多金属、非金属及一些还原性化合物,也能在水中或碱溶液中发生歧化反应用途重要的化工原料,可用于制盐酸、漂白粉、含氯有机
