
芳环上的取代反应.ppt

kp****93




亲,该文档总共56页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

芳环上的取代反应.ppt
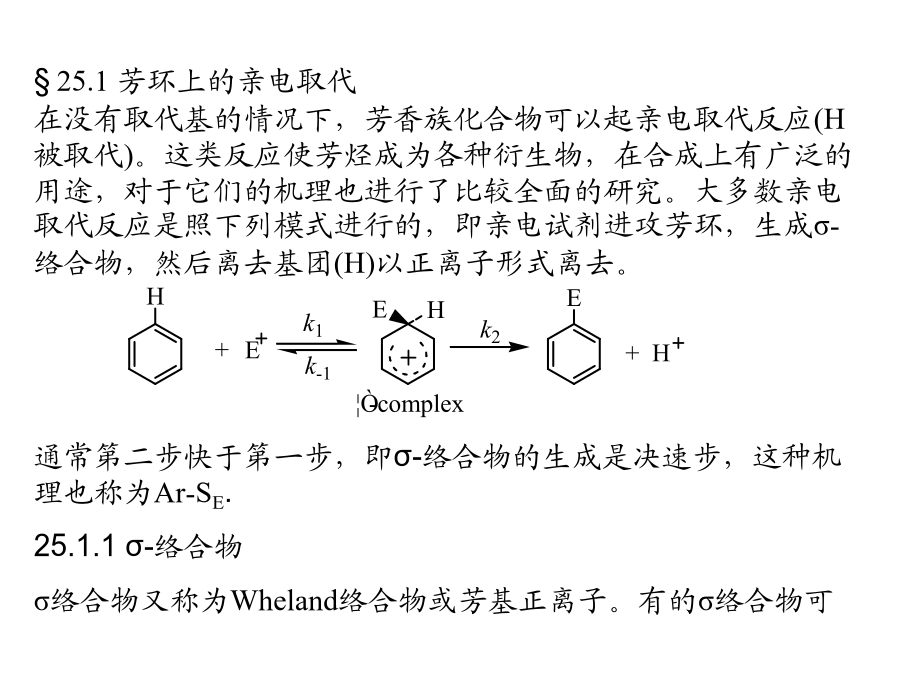
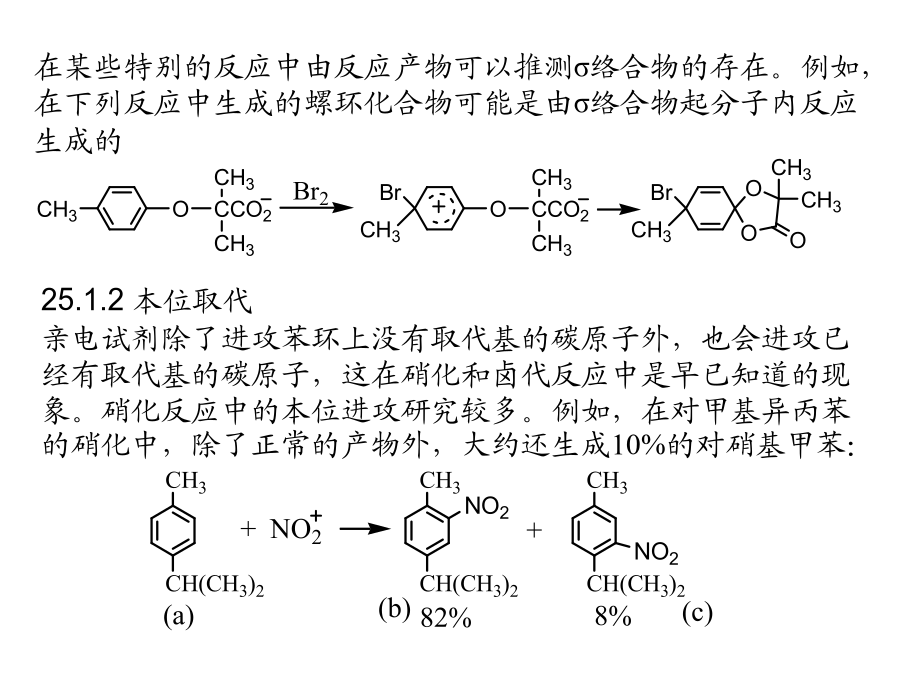
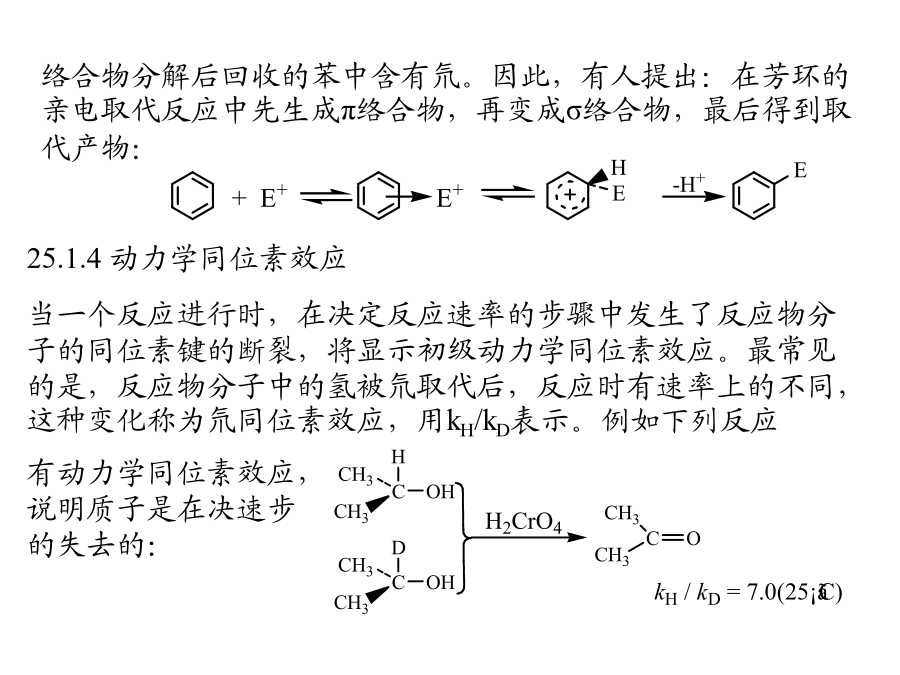
第九章芳环上的取代反应§25.1芳环上的亲电取代在没有取代基的情况下,芳香族化合物可以起亲电取代反应(H被取代)。这类反应使芳烃成为各种衍生物,在合成上有广泛的用途,对于它们的机理也进行了比较全面的研究。大多数亲电取代反应是照下列模式进行的,即亲电试剂进攻芳环,生成σ-络合物,然后离去基团(H)以正离子形式离去。以分离鉴定。例如,2,4,6-三甲基苯与EtF和BF3在低温下反应,生成熔点为-15ºC的固体,加热后分解成乙基化产物:在某些特别的反应中由反应产物可以推测σ络合物的存在。例如,在下列反应中生成的

芳环上的取代氯化反应.ppt
第4章卤化(Halogenation)概述芳环上的取代氯化反应芳环上的取代溴化、碘化和氟化反应脂烃和芳环测链的取代氯化加成卤化置换卤化

理学芳环上的取代反应课件.pptx
会计学溶剂效应螯合效应原位取代(Ipsoattack)()3.取代效应的定量关系a.分速度因数与选择性()b.Hammett方程()一.亲电取代反应卤代反应:实验已经证实芳正离子的存在:第一类定位基:定位效应(Orientation):动力学控制与热力学控制邻位和对位定向比:极化效应:溶剂效应螯合效应:原位取代(Ipso取代):3.取代基的定量关系当f>1时,该位置的活泼性比苯大,否则比苯小。例如:氯苯和苯甲醚进行硝化反应时,分速度因数分别为:2〕Hammett方程当ρ>0时,吸电子基团加速反应;当ρ<0

芳环的亲电取代亲核取代反应芳环取代基的反应.ppt
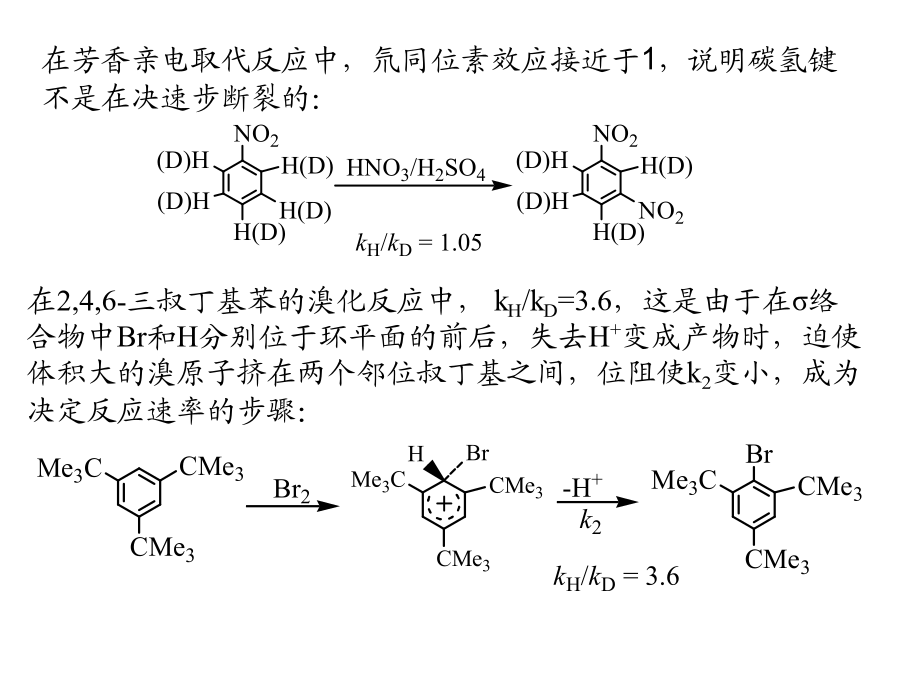
本章主要内容一、芳环的亲电取代反应及机制一、芳环的亲电取代反应及机制亲电试剂的分类2中等强度亲电试剂,能取代致活、不能取代致钝的芳环:3弱亲电试剂,只能取代高活化的芳环:苯环上的电子为芳香取代反应供给了电子,很多亲电试剂能与之反应其范围远比烯、炔加戊反应为广泛。可以用一个统一的反应机理来解释这些取代反应,虽然反应酌动力学、自由能—反应曲线对每一种亲电试剂来说可以是不一样的,但若干中间步骤基本上是相似的.取代反应中发生络合物的证据有好几个方面,用标记同位素方法研究取代速度是其中之一。如果质子的离去关系到亲电

叠氮基取代芳环上仲硝胺基新亲核取代反应的研究.docx
叠氮基取代芳环上仲硝胺基新亲核取代反应的研究叠氮基取代芳环上仲硝胺基新亲核取代反应的研究背景介绍:芳香族化合物是有机化学的重要组成部分,具有广泛的应用和研究价值。其中,芳环上存在着不同的官能团,如叠氮基和仲硝胺基,它们可以参与到不同的有机反应中,并且在合成新化合物中发挥着重要的作用。因此,研究叠氮基取代芳环上仲硝胺基的新亲核取代反应,对于拓展有机反应的领域和合成新型有机化合物具有重要的意义。主要研究内容:在这篇文章中,我们主要研究了叠氮基取代苯环上仲硝胺基的新亲核取代反应,并探究了反应机理和反应条件的影响
