
第二章 晶态和非晶态材料.ppt

kp****93









亲,该文档总共84页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

第二章 晶态和非晶态材料.ppt
第二章晶态和非晶态材料的特性2.1晶体特征及其结构基础晶体以其特有的点阵结构的特殊性,呈现出与其它物质(气、液、非晶态)完全不同的特殊性质。1.晶体的均匀性晶体结构是由相同晶胞周期的并置而成。从宏观上来说,晶体的性质是一个连续的整体,并不随观察的位置而改变。如:相同的密度、化学组成2.晶体的各向异性在晶体中不同的方向上具有不同的物理性质,即为各向异性。主要是由于晶体内的粒子在不同方向上排列、取向不同导致的。例如,在不同的方向具有不同的电导率、膨胀系数、折光率、机械强度等。3.晶体的自范性晶体物质在适宜的外

第二章 晶态和非晶态.ppt
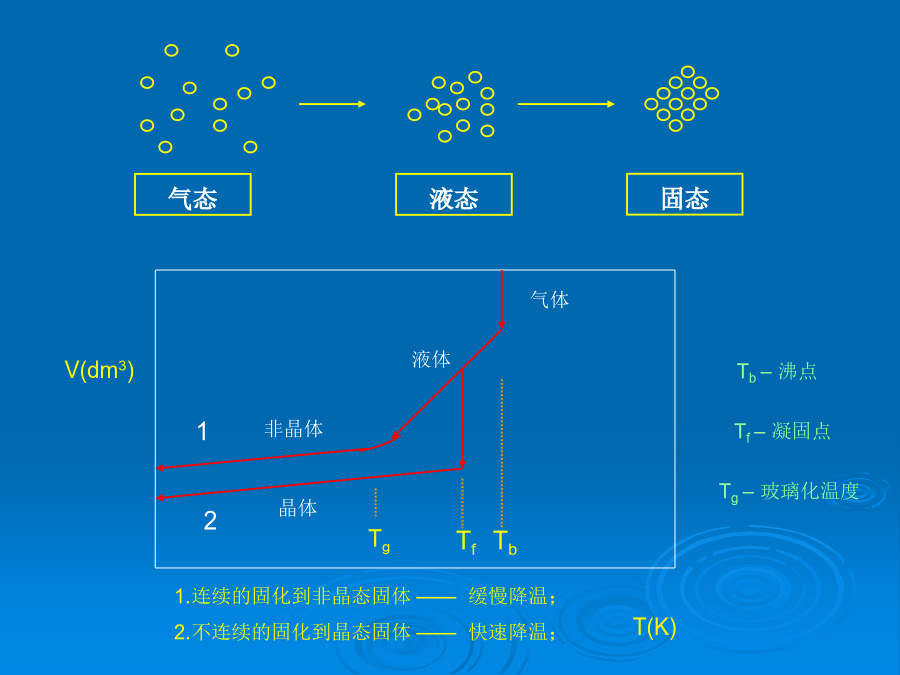
第二章晶态和非晶态材料的特性2.1晶体特征的结构基础1、晶体的均匀性2、晶体的各向异性3、晶体的自范性晶体的外形既受内部结构(点阵排列方式)制约,又在一定程度上受外因(温度、压力、浓度、杂质)的影响。但同一种晶体的每两个相应界面的夹角是不受外界条件的影响,保持恒定不变。这个规律称为“晶面角守恒定律”非晶体如玻璃体在从液相冷却时,形成的固体表面圆滑,没有固定的外形。4、晶体的熔点固体材料的升温和降温曲线5、晶体的对称性2.2非整比化合物材料产生非整比化合物的情况有以下几类:2、层间嵌入某些离子、原子或分子某

非晶态材料的制备.pptx
非晶态材料旳制备一、引言混沌与有序之间的辩证关系二、非晶态材料旳基本概念和基本性质2.非晶态材料旳分类3.非晶态材料旳特征三、非晶态旳形成3.热力学理论4.动力学理论5.构造化学理论四.非晶态材料旳制备原理与措施五.非晶材料旳制备2.气相直接凝聚法3.液体急冷法(1)喷枪法(2)锤砧法(3)离心法(4)压延法(5)单辊法(6)熔体沾出法(7)熔滴法六.大块非晶态材料旳制备2.大块非晶合金旳性能特点3.大块非晶合金旳形成机理4.大块非晶合金旳制备措施(1)电弧熔炼铜模吸铸法(2)水淬法(3)感应加热铜模浇铸

非晶态材料的物理学和应用.pdf
摘要非晶态材料是一类具有无序、非晶和玻璃结构的材料。其物理性质和应用在过去几十年里得到了广泛研究和应用。本文将介绍非晶态材料的基本概念、结构、制备方法、物理性质和应用,同时探讨了其未来的发展方向。引言非晶态材料是指在晶体结构形成之前或由于快速凝固等原因而无法形成有序结构的材料。这种材料具有无序、非晶和玻璃结构,其原子或分子之间的间隙、角度和距离都没有任何规律可言。与晶体材料相比,非晶态材料具有很多优点,如高强度、高韧性、优异的磁性和导电性能、良好的耐蚀性等。因此,非晶态材料在材料科学、物理学和工程领域中具

非晶态0712.ppt
第七章非晶,薄膜,纤维刘杏芹中国科学技术大学,材料科学与工程系2010年6月8日7.1非晶7.2薄膜7.3陶瓷纤维7.1非晶态一、概述自然界的物质通常以气态、液态和固态3种集聚态存在。固体可分为晶体与非晶体两种形式。晶体的结构特点是质点在三维空间作周期性的重复排列,即近程和远程都是有序的;而非晶态固体的结构具有近程有序而远程无序的特点。非晶体固体通常指玻璃体、无定形物质、高聚物(如树脂、橡胶等)。玻璃体则包括有硅酸盐玻璃、硼酸盐玻璃、石英玻璃以及半导体玻璃、金属玻璃等。非晶态材料受到人们的重视是从20世纪
