
液相法制备纳米微粒.ppt

15****92







亲,该文档总共63页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

液相法制备纳米微粒.ppt
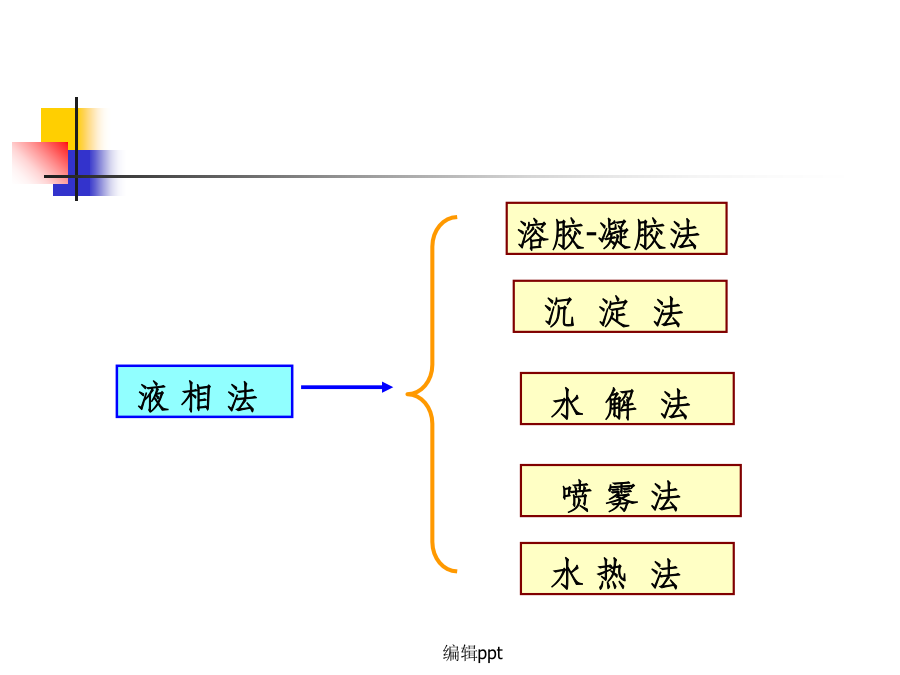
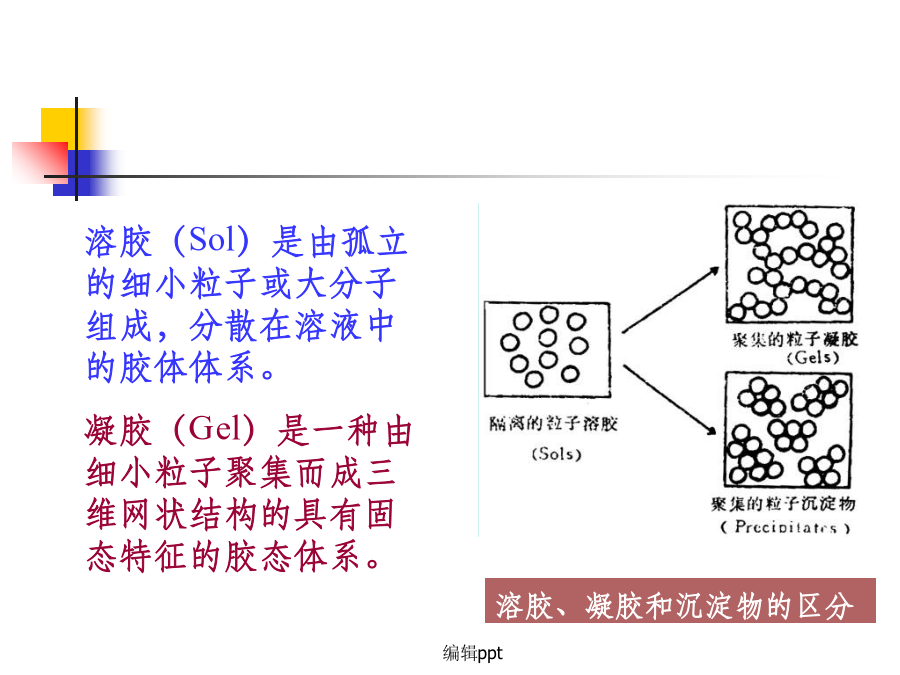
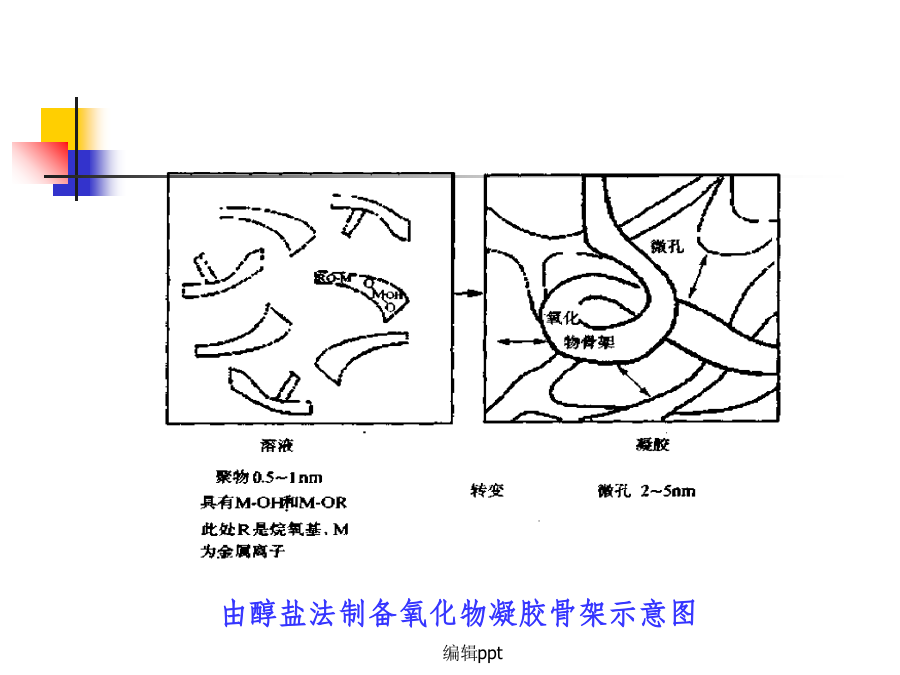
6.2液相法制备纳米微粒溶胶-凝胶法1.溶胶—凝胶法(sol-gel)溶胶—凝胶法是60年代发展起来的一种制备玻璃、陶瓷等无机材料的新工艺。其基本原理是:将金属醇盐或无机盐经水解直接形成溶胶,然后使溶质聚合凝胶化,再将凝胶干燥、焙烧去除有机成分,最后得到无机材料。将一种或几种盐均匀分散在一种溶剂中,使它们成为透明状的胶体,即成溶胶(sol)。将溶胶在一定条件下(温度、酸碱度等)进行老化处理,得到透明状的冻状物即称凝胶(gel)。溶胶、凝胶和沉淀物的区分(1)溶胶的制备有两种方法制备溶胶先将部分或全部组分用

纳米微粒制备-气相法.ppt
纳米微粒的制备-气相法纳米粒子制备方法4.1纳米微粒的气相制备4.1.1低压气体中蒸发法(气体冷凝法)纳米粒子尺寸的影响因素蒸发源的加热方式1)电阻加热:(电阻丝)电阻加热法使用的螺旋纤维或者舟状的电阻发热体。如图金属类:如铬镍系,铁铬系,温度可达1300℃;钼,钨,铂,温度可达1800℃;非金属类:SiC(1500℃),石墨棒(3000℃),MoSi2(1700℃)。.有两种情况不能使用这种方法进行加热和蒸发:①两种材料(发热体与蒸发原料)在高温熔融后形成合金。②蒸发原料的蒸发温度高于发热体的软化温度。

纳米微粒制备-气相法.ppt
纳米微粒的制备-气相法纳米粒子制备方法4.1纳米微粒的气相制备4.1.1低压气体中蒸发法(气体冷凝法)纳米粒子尺寸的影响因素蒸发源的加热方式1)电阻加热:(电阻丝)电阻加热法使用的螺旋纤维或者舟状的电阻发热体。如图金属类:如铬镍系,铁铬系,温度可达1300℃;钼,钨,铂,温度可达1800℃;非金属类:SiC(1500℃),石墨棒(3000℃),MoSi2(1700℃)。有两种情况不能使用这种方法进行加热和蒸发:①两种材料(发热体与蒸发原料)在高温熔融后形成合金。②蒸发原料的蒸发温度高于发热体的软化温度。目

纳米微粒制备气相法.pptx
纳米微粒制备气相法纳米粒子制备方法4.1纳米微粒的气相制备4.1.1低压气体中蒸发法(气体冷凝法)纳米粒子尺寸的影响因素蒸发源的加热方式1)电阻加热:(电阻丝)电阻加热法使用的螺旋纤维或者舟状的电阻发热体。如图金属类:如铬镍系,铁铬系,温度可达1300℃;钼,钨,铂,温度可达1800℃;非金属类:SiC(1500℃),石墨棒(3000℃),MoSi2(1700℃)。/有两种情况不能使用这种方法进行加热和蒸发:①两种材料(发热体与蒸发原料)在高温熔融后形成合金。②蒸发原料的蒸发温度高于发热体的软化温度。目前

固相法制备纳米微粒.pptx
前言物质的微粉化机理大致可分为如下两类,一类是将大块物质极细地分割[尺寸降低过程(SizeReductionProcess)]的方法。另一类是将最小单位(分子或原子)组合[构筑过程(BuildupProcess)]的方法。尺寸降低过程——物质无变化:机械粉碎(用球磨机、喷射磨等进行粉碎),化学处理(溶出法)等。构筑过程——物质发生变化:热分解法(大多是盐的分解),固相反应法(大多数是化合物),火花放电法(用金属铝生产氢氧化铝)等。一.热分解法1.1序言1.2草酸盐的分类1.3草酸盐的热分解机理Ⅰ的反应为:
