
无机材料科学基础.pdf

文库****品店







亲,该文档总共12页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

无机材料科学基础.pdf
第二章晶体结构与晶体结构中的缺陷2-1氯化铯(CsCl)属萤石结构,如果Cs+离子半径为0.170nm,Cl-离子半径为0.181nm,计算球状离子所占据的空间分数(堆积系数)。假设Cs+和Cl-离子沿立方对角线接触。2-2(a)MgO具有NaCl结构。根据O2-半径为0.140nm和Mg2+半径为0.072nm,计算球状离子所占据的空间分数(堆积系数)。(b)计算MgO的密度。2-3氧化锂(Li2O)的晶胞结构构成:O2-离子呈面心立方堆积,Li+离子占据所有四面体空隙。计算:(a)晶胞常数;(b)Li

无机材料科学基础试卷.doc
无机材料科学基础试卷名词解释液相独立析晶:是在转熔过程中发生的,由于冷却速度较快,被回收的晶相有可能会被新析出的固相包裹起来,使转熔过程不能继续进行,从而使液相进行另一个单独的析晶过程,就是液相独立析晶。二次再结晶:少数巨大晶粒在细晶消耗时成核长大过程。晶粒生长:平衡晶粒尺寸在不改变其分布的情况下,连续增大的过程。本征扩散:是指空位来源于晶体结构中本征热缺陷而引起质点的迁移。非本征扩散:空位来源于掺杂而引起的质点迁移。一级相变:体系由一相变为另一相时,如两相的化学势相等但化学势的一级偏微商(一级导数)不相

无机材料科学基础习题.docx
1、已知Mg2+半径为0.072nm,O2-半径为0.140nm,计算MgO晶体结构的堆积系数与密度。解:MgO为NaCl型,O2-做密堆积,Mg2+填充空隙。=0.140nm,=0.072nm,=4,晶胞中质点体积:,,晶胞体积=,堆积系数=晶胞中MgO体积/晶胞体积=68.5%,密度=晶胞中MgO质量/晶胞体积=3.49g/cm3。2、(1)一晶面在x、y、z轴上的截距分别为2a、3b、6c,求出该晶面的米勒指数;(2)一晶面在x、y、z轴上的截距分别为a/3、b/2、c,求出该晶面的米勒指数。解:(

无机材料科学基础答案.docx
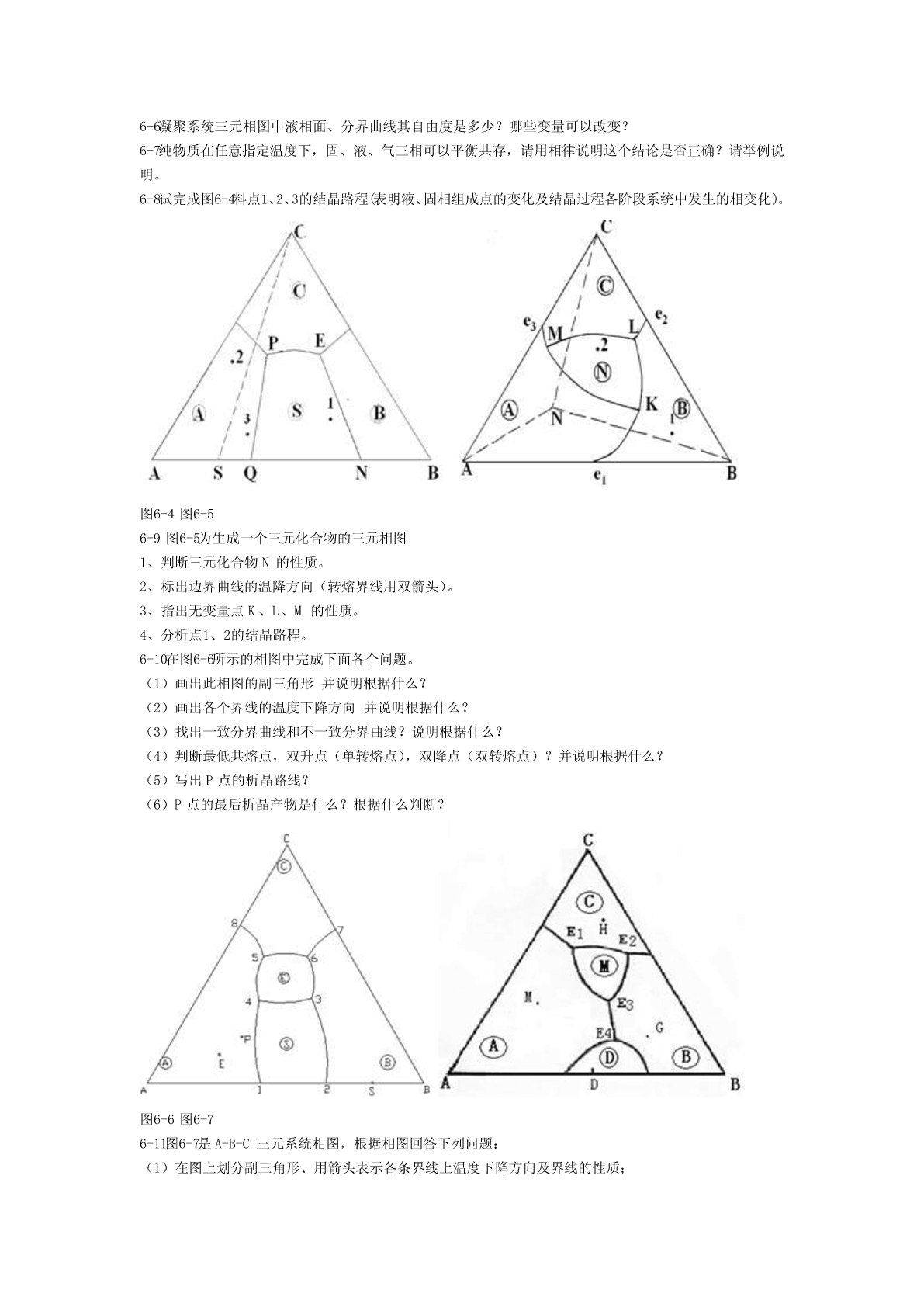
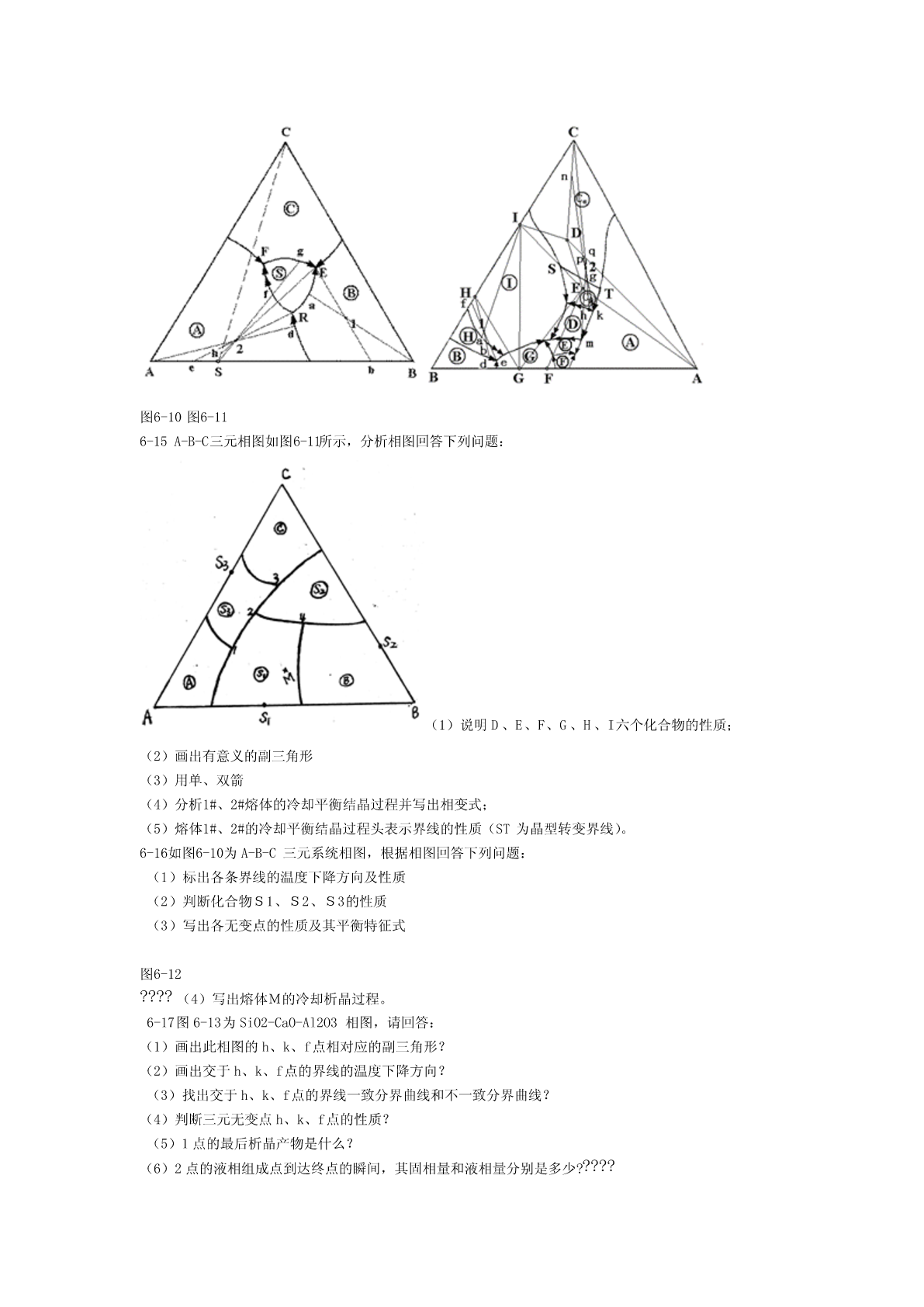
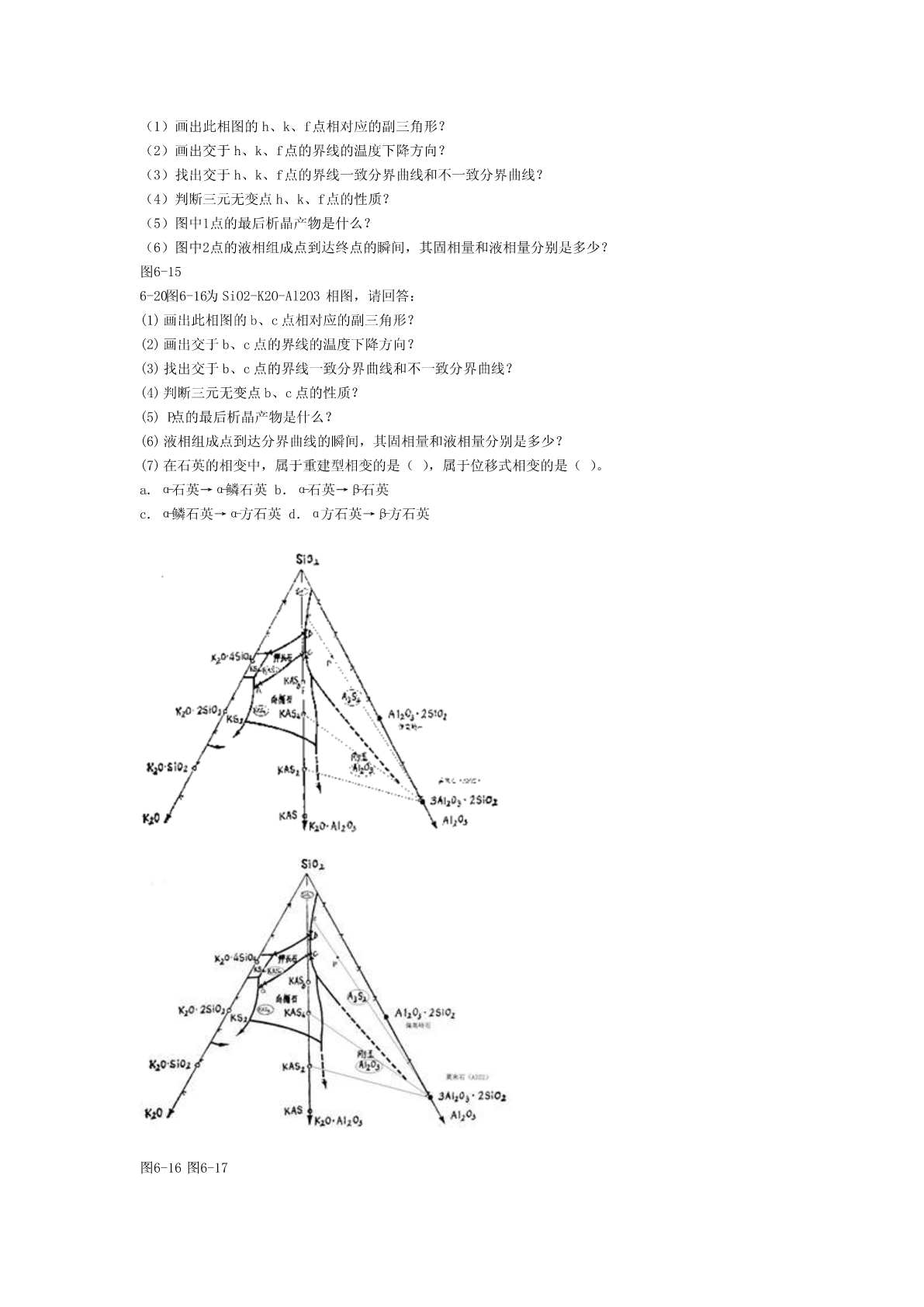
6-1略。6-2什么是吉布斯相律?它有什么实际意义?解:相律是吉布斯根据热力学原理得出的相平衡基本定律,又称吉布斯相律,用于描述达到相平衡时系统中自由度数与组分数和相数之间的关系。一般形式的数学表达式为F=C-P+2。其中F为自由度数,C为组分数,P为相数,2代表温度和压力两个变量。应用相率可以很方便地确定平衡体系的自由度数。6-3固体硫有两种晶型,即单斜硫、斜方硫,因此,硫系统可能有四个相,如果某人实验得到这四个相平衡共存,试判断这个实验有无问题?解:有问题,根据相律,F=C-P+2=1-P+2=3-P

无机材料科学基础教案.docx
《无机材料科学基础》绪论1、材料的发展动向及本课程的重要地位;2、本课程的特色及基本要求。3、无机材料物理化学的科学内涵4、无机材料物理化学的研究方法5、参考文献第一章结晶学基础§1-1—§1-6内容在结晶学课程中讲授§1-7晶体化学基本原理一、结晶化学定律(Goldschmidt——哥希密特定律)1、数量关系2、大小关系3、极化性能二、决定晶体结构的基本因素(一)原子半径和离子半径(二)球体紧密堆积原理1、等径球的最紧密堆积及其空隙(1)六方最紧密堆积1)六方最紧密堆积方式2)六方最紧密堆积特点(2)面
