
一种N-取代脲类化合物及其制备方法和应用.pdf

是你****松呀








亲,该文档总共24页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料
一种N-取代脲类化合物及其制备方法和应用.pdf
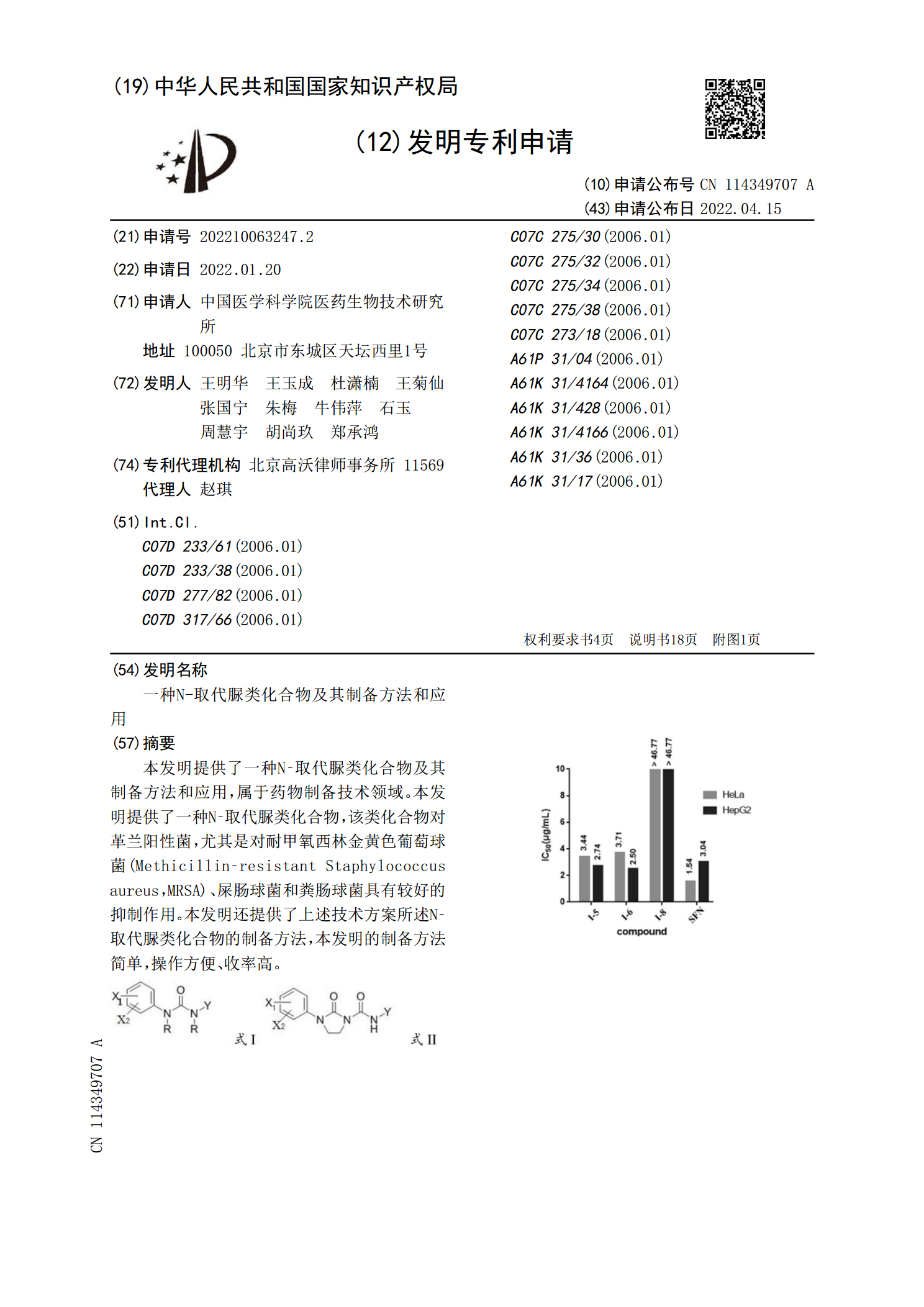
本发明提供了一种N‑取代脲类化合物及其制备方法和应用,属于药物制备技术领域。本发明提供了一种N‑取代脲类化合物,该类化合物对革兰阳性菌,尤其是对耐甲氧西林金黄色葡萄球菌(Methicillin‑resistantStaphylococcusaureus,MRSA)、屎肠球菌和粪肠球菌具有较好的抑制作用。本发明还提供了上述技术方案所述N‑取代脲类化合物的制备方法,本发明的制备方法简单,操作方便、收率高。

取代脲及其制备和使用方法.pdf
本发明涉及取代脲和包含其的组合物,其在某些实施方式中可用于治疗和/或预防对其有需要的对象中的疼痛。

一种取代脲类化合物的制备方法.pdf
本发明提供了一种取代脲类化合物的制备方法,以含氮杂环化合物和四卤甲烷为原料,在催化剂及溶剂条件下经光照催化反应制得取代脲类化合物和卤素单质;本发明的制备方法原料来源广,避免了采用毒性大的光气、三光气等为原料,减少了制备过程对环境的影响,提高了反应的原子利用率;反应条件温和,操作简便、减少了环境污染,降低了反应成本;产品收率高且联产卤素单质,附加值较高,避免了产生大量废弃物,具有较高的原子经济性和环境友好性,有利于推广应用。

一种N‑单取代哌嗪类化合物的制备方法与应用.pdf
本发明公开了一种式(6)所示的N‑单取代哌嗪类化合物的制备方法,由哌嗪单盐酸盐(1)与RX或RCl在溶剂中反应制得单取代哌嗪双酸盐(4)或(5),加碱中和,精馏蒸出产物(6)。本发明为新型药物、合成染料、农药等的研发提供了基础。

一种多取代氨基吡唑类化合物及其制备方法和应用.pdf
本发明提供了一种多取代氨基吡唑类化合物及其制备方法和应用。本发明多取代氨基吡唑类化合物,同时含有氨基、酯基或酰胺键、仲胺等多官能团活性位点,有利于进行进一步有机转化反应,开发出具有抗癌、抗炎、杀菌等活性的杂环吡唑类化合物;本发明的多取代氨基吡唑类化合物的制备方法,以最简底物实现了绿色溶剂体系下三组分便利构建芳胺基吡唑杂环骨架分子,同时,本发明的制备方法,原料廉价易得、使用的催化剂和溶剂安全性高、一锅三组分反应操作简单,此外,针对反应条件进行优化后,反应选择性好,收率高,原子经济性好、产物易于分离,与现存的
