
一种镍负载的多孔碳材料催化剂及其制备方法和用途.pdf

邻家****曼玉








在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

一种镍负载的多孔碳材料催化剂及其制备方法和用途.pdf
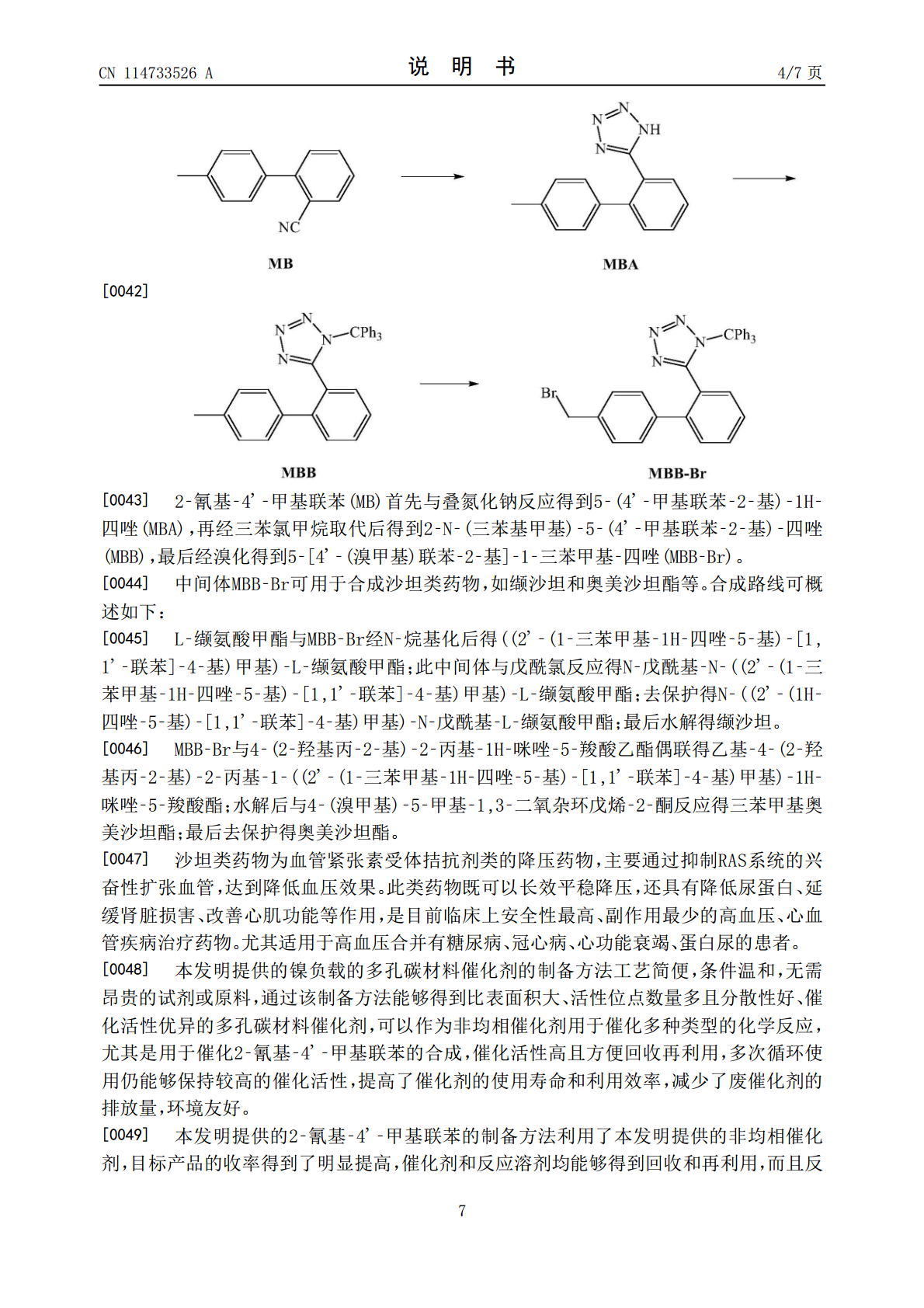
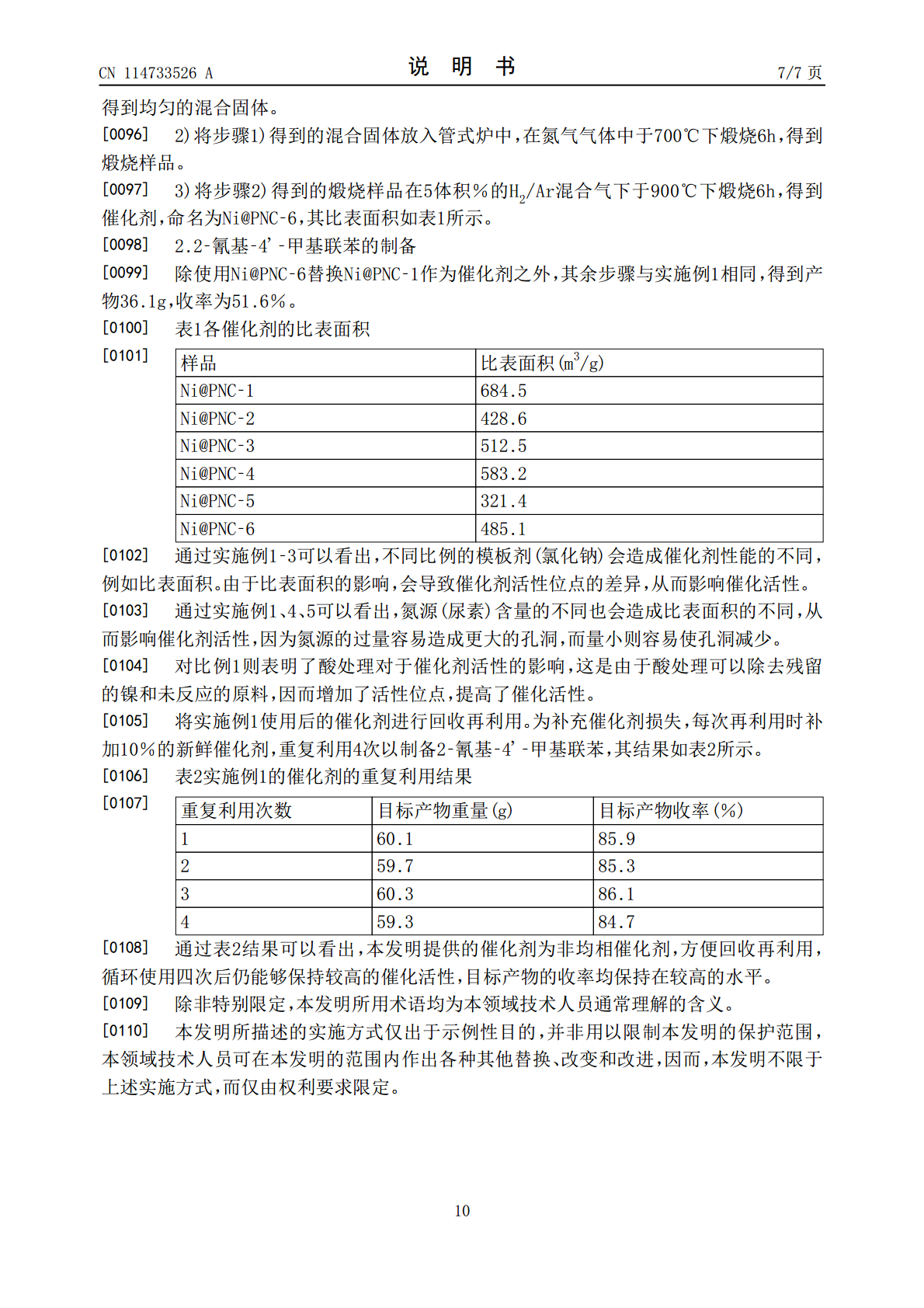
本发明提供了一种镍负载的多孔碳材料催化剂的制备方法以及由此所得的催化剂和其用途。本发明还提供了一种2‑氰基‑4’‑甲基联苯的制备方法。本发明提供的催化剂制备方法工艺简便,条件温和,无需昂贵的试剂或原料,通过该制备方法能够得到比表面积大、活性位点数量多且分散性好、催化活性优异的多孔碳材料催化剂,催化活性高且方便回收再利用,提高了催化剂的使用寿命和利用效率。本发明提供的2‑氰基‑4’‑甲基联苯的制备方法利用了本发明提供的非均相催化剂,目标产品的收率得到了明显提高,能够大幅降低生产成本、提高生产效率,适宜于工业

一种多孔材料负载氧化镍催化剂的制备方法.pdf
本发明公开一种多孔材料负载氧化镍催化剂的制备方法。依次包括如下步骤:将膨润土加入到八烷基三甲基溴化铵溶液中,在恒温搅拌、老化、离心分离,得到八烷基三甲基溴化铵改性的膨润土固体;将(3‑氨基丙基)三乙氧基硅烷、水杨醛和六水合氯化镍按1:1:1(摩尔比)的量加入到乙醇中形成溶液,加入八烷基三甲基溴化铵改性的膨润土固体,搅拌、沉淀分离,形成含镍有机配合物柱撑膨润土;含产物置于管式炉中,在通氮气的情况下,焙烧,再通入空气,最后继续通氮气,然后停止加热冷却至室温,得到氧化硅柱撑的膨润土基多孔材料负载氧化镍催化剂。该

一种多孔碳材料的制备方法及其用途.pdf
本发明提供了一种多孔碳材料的制备方法及其用途,按照下述步骤进行:将乙酸钾放于镍坩埚,置于高温石英管式炉中,在惰性气流保护下,进行高温热解,经过热解后得到产物,用酸溶液洗去产物中的杂质,再将产物浸没于酸溶液中磁力搅拌,然后用大量去离子水将产物洗涤至中性,真空干燥即得到多孔碳材料。制备的材料孔性结构良好,比表面积高、孔体积大,电化学性能良好,并且在其他方面也能得到应用。
一种氮掺杂的多孔碳材料及其制备方法和用途.pdf
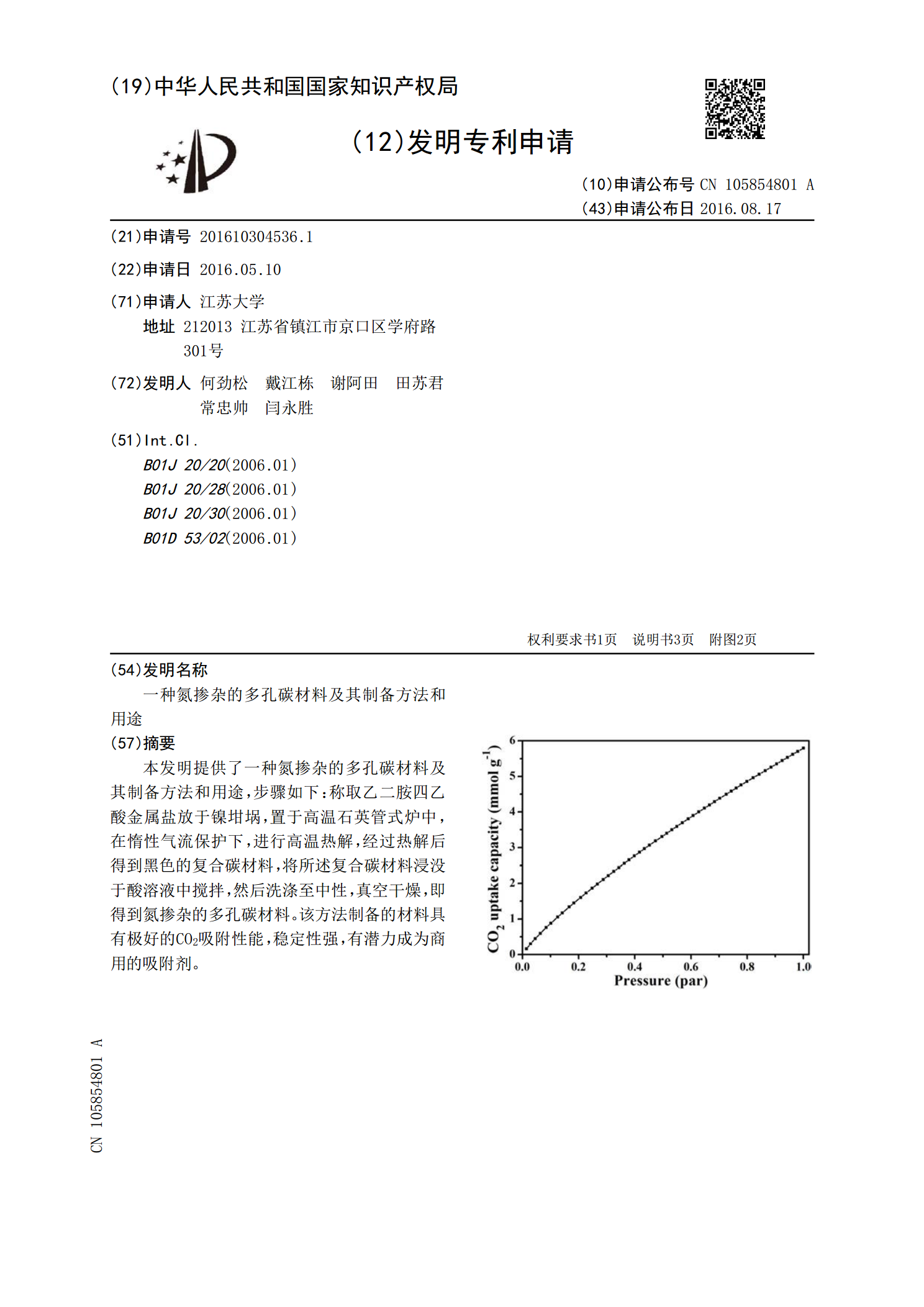
本发明提供了一种氮掺杂的多孔碳材料及其制备方法和用途,步骤如下:称取乙二胺四乙酸金属盐放于镍坩埚,置于高温石英管式炉中,在惰性气流保护下,进行高温热解,经过热解后得到黑色的复合碳材料,将所述复合碳材料浸没于酸溶液中搅拌,然后洗涤至中性,真空干燥,即得到氮掺杂的多孔碳材料。该方法制备的材料具有极好的CO

多孔碳负载镍材料的制备方法及其应用.pdf
本发明涉及一种多孔碳负载镍材料(Ni‑PC)的制备方法及其在催化合成二硫缩醛类化合物中的应用。将均苯三酸和三水硝酸铜溶于乙醇、DMF和去离子水的混合溶液中,在适宜的晶化条件下,合成得到MOF‑199,然后在此基础上负载Ni,制得Ni‑MOF‑199;最后在N
