
高一化学物质的量 学案上科版.doc

明轩****la






在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

高一化学物质的量 学案上科版.doc
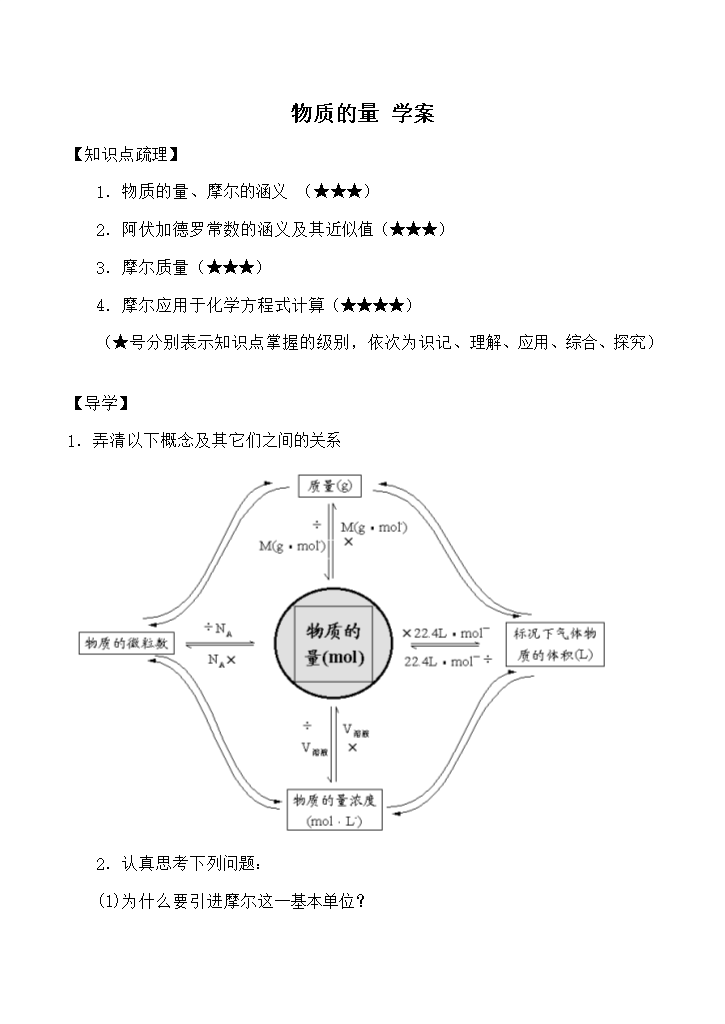
物质的量学案【知识点疏理】1.物质的量、摩尔的涵义(★★★)2.阿伏加德罗常数的涵义及其近似值(★★★)3.摩尔质量(★★★)4.摩尔应用于化学方程式计算(★★★★)(★号分别表示知识点掌握的级别,依次为识记、理解、应用、综合、探究)【导学】1.弄清以下概念及其它们之间的关系2.认真思考下列问题:(1)为什么要引进摩尔这一基本单位?(2)使用摩尔作单位时注意哪些事项?【例题分析】例1.下列说法是否正确,若不正确,请加以改正。(1)水的摩尔质量是18g(2)1分子硫酸的质量是98g(3)1mol氮的质量为2

上科版高一化学物质的量 学案.rar
用心爱心专心物质的量学案考纲要求了解物质的量的单位-摩尔(mol),摩尔质量的涵义。理解阿伏加德罗常数的涵义。掌握物质的量与微粒(原子、分子、离子等)数目之间的相互关系。重点难点物质的量与微粒数目之间关系;阿伏加德罗常数的涵义。一、物质的量及其单位1、物质的量(n):科学上用来研究物质的基本物理量。(1)、物质的量是专有名词,是七个基本物理量之一,(2)、粒子集体是指原子、分子、离子、电子、质子、中子等微观粒子的集体,或表示某些粒子结构的特定组合,如NaCl。2、物质的量的单位-摩尔(mol)(1)“物质
高一化学物质的量 学案上科版.doc
物质的量学案【知识点疏理】1.物质的量、摩尔的涵义(★★★)2.阿伏加德罗常数的涵义及其近似值(★★★)3.摩尔质量(★★★)4.摩尔应用于化学方程式计算(★★★★)(★号分别表示知识点掌握的级别依次为识记、理解、应用、综合、探究)【导学】1.弄清以下概念及其它们之间的关系2.认真思考下列问题:(1)为什么要引进摩尔这一基本单位?(2)使用摩尔作单位时注意哪些事项?【例题分析】例1.下列说法是否正确若不正确请加以改正。(1)水的摩尔质量是18g(2)1分子硫酸的质量是98g(3)1mol

高一化学物质的量浓度 学案上科版.doc
物质的量浓度【知识点疏理】1.物质的量浓度的定义及数学表达式(★★★★)2.物质的量溶液的配制方法及误差分析(★★★)3.应用物质的量浓度进行计算的常见方法(★★★★)4.物质的量浓度和质量分数的换算(★★★★★)5.物质的量溶液中溶质的微粒数(★★★★)(★号分别表示知识点掌握的级别,依次为识记、理解、应用、综合、探究)【导学】溶质的质量分数、物质的量浓度的联系和区别配制溶液时的混合规律一定量溶剂(或溶液)里溶解溶质的质量不超过定温下的极限值。可溶性氧化物溶于水,溶质是跟水反应后的生成物;结晶水合物溶于

高一化学物质的量浓度 学案上科版.doc
物质的量浓度【知识点疏理】1.物质的量浓度的定义及数学表达式(★★★★)2.物质的量溶液的配制方法及误差分析(★★★)3.应用物质的量浓度进行计算的常见方法(★★★★)4.物质的量浓度和质量分数的换算(★★★★★)5.物质的量溶液中溶质的微粒数(★★★★)(★号分别表示知识点掌握的级别依次为识记、理解、应用、综合、探究)【导学】溶质的质量分数、物质的量浓度的联系和区别配制溶液时的混合规律一定量溶剂(或溶液)里溶解溶质的质量不超过定温下的极限值。可溶性氧化物溶于水溶质是跟水反应后的生成物;结晶水合
