
版高考化学一轮复习 课时分层提升练十七 化学键(含解析)新人教版-新人教版高三全册化学试题.doc

是湛****21









亲,该文档总共12页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

版高考化学一轮复习 课时分层提升练十七 化学键(含解析)新人教版-新人教版高三全册化学试题.doc
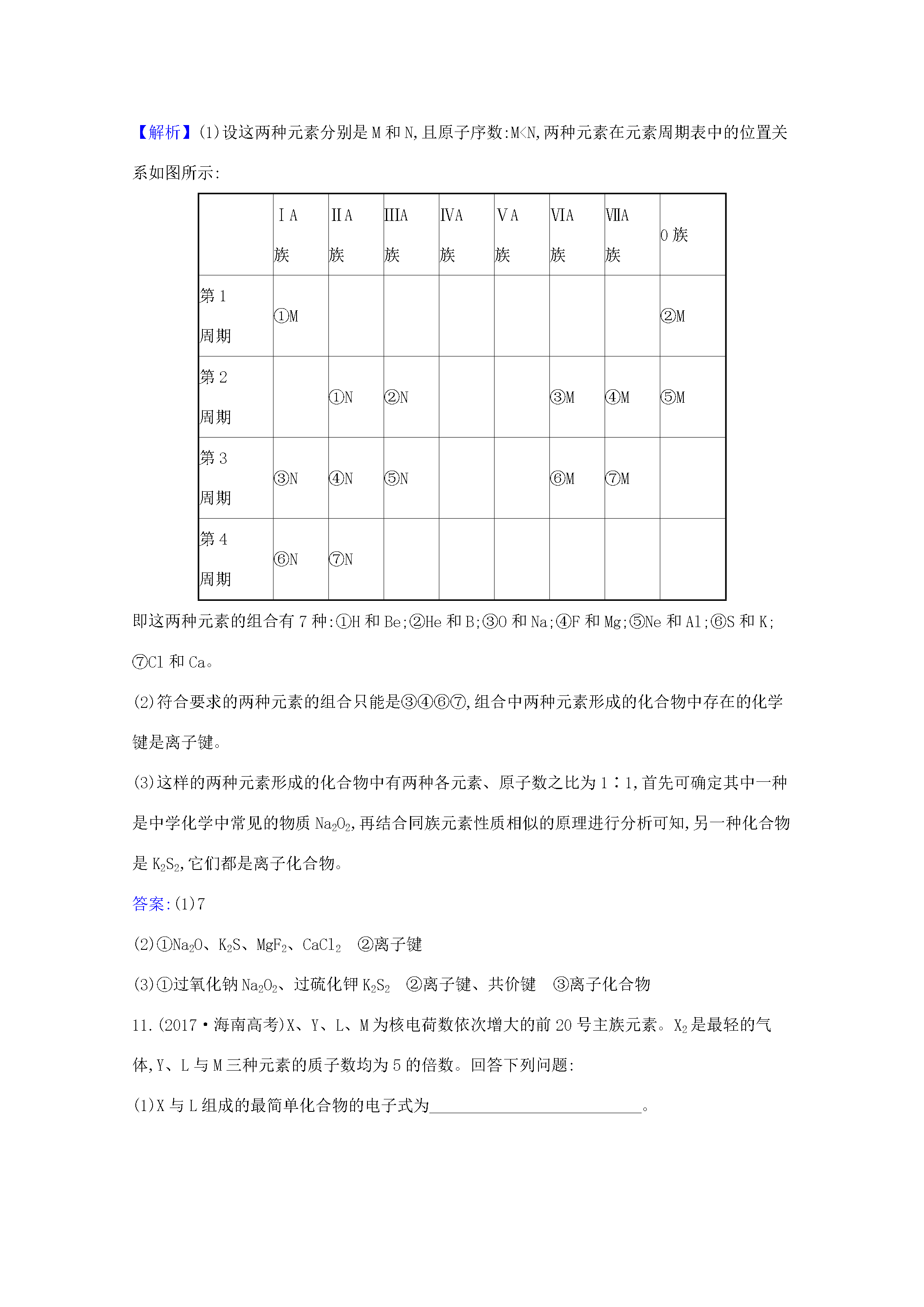
化学键一、选择题1.下列说法中错误的是()A.Na2O2既含离子键又含非极性键B.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素C.除氦外的稀有气体原子的最外层电子数都是8D.位于ⅠA的元素与位于ⅦA的元素组成的化合物都是离子化合物【解析】选D。过氧化钠是钠离子和过氧根离子构成形成的化学键为离子键过氧根离子中为氧原子间形成的非极性共价键故A正确;元素周期表中从ⅢB族到ⅡB族为7个副族一个第ⅤⅢ族为过渡元素都是金属元素故B正确;稀有气体原子结构特征分析除氦外的稀有气体原子的最外层电子数都是8故

2021版高考化学一轮复习 课时分层提升练十七 化学键(含解析)新人教版.doc
化学键一、选择题1.下列说法中错误的是()A.Na2O2既含离子键又含非极性键B.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素C.除氦外的稀有气体原子的最外层电子数都是8D.位于ⅠA的元素与位于ⅦA的元素组成的化合物都是离子化合物【解析】选D。过氧化钠是钠离子和过氧根离子构成,形成的化学键为离子键,过氧根离子中为氧原子间形成的非极性共价键,故A正确;元素周期表中从ⅢB族到ⅡB族为7个副族,一个第ⅤⅢ族,为过渡元素,都是金属元素,故B正确;稀有气体原子结构特征分析除氦外的稀有气体原子的最外层电子

2021版高考化学一轮复习 课时分层提升练十七 化学键(含解析)新人教版.doc
-11-化学键一、选择题1.下列说法中错误的是()A.Na2O2既含离子键又含非极性键B.元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素C.除氦外的稀有气体原子的最外层电子数都是8D.位于ⅠA的元素与位于ⅦA的元素组成的化合物都是离子化合物【解析】选D。过氧化钠是钠离子和过氧根离子构成,形成的化学键为离子键,过氧根离子中为氧原子间形成的非极性共价键,故A正确;元素周期表中从ⅢB族到ⅡB族为7个副族,一个第ⅤⅢ族,为过渡元素,都是金属元素,故B正确;稀有气体原子结构特征分析除氦外的稀有气体原子的最
版高考化学一轮复习 课时分层提升练三 物质的分类(含解析)新人教版-新人教版高三全册化学试题.doc
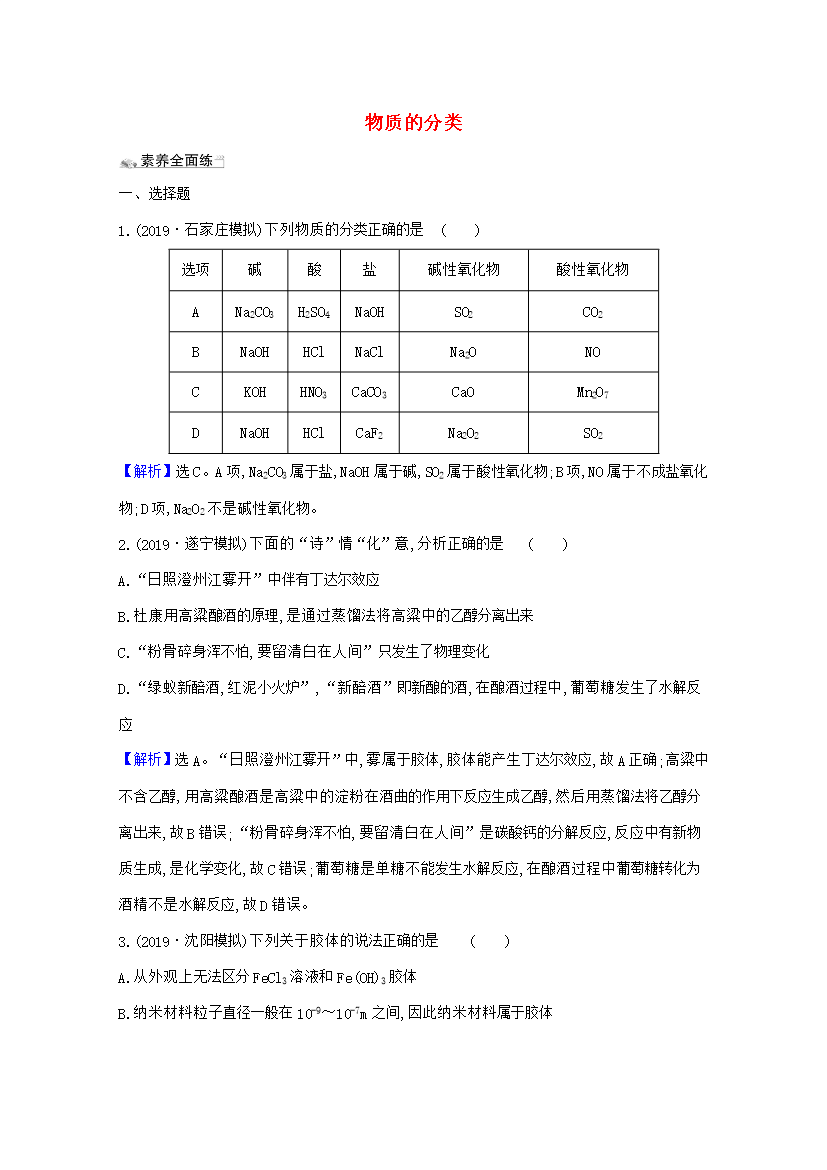
物质的分类一、选择题1.(2019·石家庄模拟)下列物质的分类正确的是()选项碱酸盐碱性氧化物酸性氧化物ANa2CO3H2SO4NaOHSO2CO2BNaOHHClNaClNa2ONOCKOHHNO3CaCO3CaOMn2O7DNaOHHClCaF2Na2O2SO2【解析】选C。A项Na2CO3属于盐NaOH属于碱SO2属于酸性氧化物;B项NO属于不成盐氧化物;D项Na2O2不是碱性氧化物。2.(2019·遂宁模拟)下面的“诗”情“化”意分析正确的是()A.“日照澄州江雾开”中伴有丁达尔效应B.杜

版高考化学一轮复习 课时分层提升练五 氧化还原反应(含解析)新人教版-新人教版高三全册化学试题.doc
氧化还原反应一、选择题1.(2019·桂林模拟)将燃着的镁条伸入盛有二氧化碳的集气瓶中镁条继续燃烧反应的化学方程式为CO2+2MgC+2MgO该反应属于()①化合反应②分解反应③置换反应④复分解反应⑤氧化还原反应⑥离子反应⑦非氧化还原反应A.①③⑦B.②③⑥C.③⑤D.④⑥【解析】选C。根据置换反应的定义可知该反应属于置换反应;碳元素、镁元素化合价反应前后有变化该反应也属于氧化还原反应;没在溶液中进行该反应不属于离子反应。2.明代《天工开物》记载“火法”冶炼锌:“炉甘石十斤
