
2008浙江高三化学模拟试题汇编《探究实验2》.doc

沛芹****ng







在线预览结束,喜欢就下载吧,查找使用更方便
相关资料
2008浙江高三化学模拟试题汇编《探究实验2》.doc
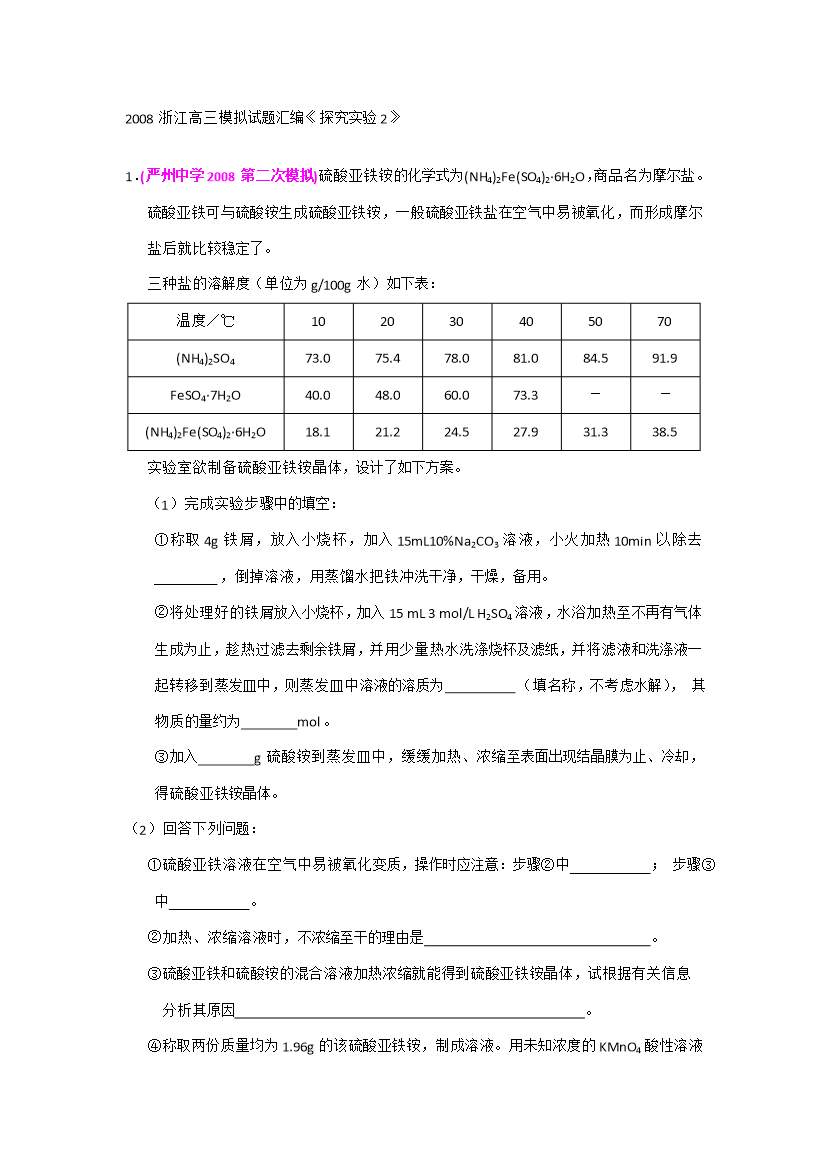
2008浙江高三模拟试题汇编《探究实验2》1.(严州中学2008第二次模拟)硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2·6H2O商品名为摩尔盐。硫酸亚铁可与硫酸铵生成硫酸亚铁铵一般硫酸亚铁盐在空气中易被氧化而形成摩尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:温度/℃102030405070(NH4)2SO473.075.478.081.084.591.9FeSO4·7H2O40.048.060.073.3--(NH4)2Fe(SO4)2·6H2O18.121.224.527.9

2008浙江高三化学模拟试题汇编《探究实验2》.doc
2008浙江高三模拟试题汇编《探究实验2》1.(严州中学2008第二次模拟)硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2·6H2O,商品名为摩尔盐。硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:温度/℃102030405070(NH4)2SO473.075.478.081.084.591.9FeSO4·7H2O40.048.060.073.3--(NH4)2Fe(SO4)2·6H2O18.121.224.52

试题-全国-2008_2008浙江高三化学模拟试题汇编《探究实验2》.rar
2008浙江高三模拟试题汇编《探究实验2》1.(严州中学2008第二次模拟)硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2·6H2O,商品名为摩尔盐。硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:温度/℃102030405070(NH4)2SO473.075.478.081.084.591.9FeSO4·7H2O40.048.060.073.3--(NH4)2Fe(SO4)2·6H2O18.121.224.52

2008浙江高三模拟试题汇编《探究实验2》.doc
2008浙江高三模拟试题汇编《探究实验2》安徽省萧县一中李洪波2352001.(严州中学2008第二次模拟)硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2·6H2O,商品名为摩尔盐。硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:温度/℃102030405070(NH4)2SO473.075.478.081.084.591.9FeSO4·7H2O40.048.060.073.3--(NH4)2Fe(SO4)2·6

2008浙江高三模拟试题汇编《探究实验2》.doc
2008浙江高三模拟试题汇编《探究实验2》安徽省萧县一中李洪波2352001.(严州中学2008第二次模拟)硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2·6H2O商品名为摩尔盐。硫酸亚铁可与硫酸铵生成硫酸亚铁铵一般硫酸亚铁盐在空气中易被氧化而形成摩尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:温度/℃102030405070(NH4)2SO473.075.478.081.084.591.9FeSO4·7H2O40.048.060.073.3--(NH4)2Fe(SO4)2·6H2O
