
新课标人教版选修四市公开课一等奖百校联赛特等奖课件.pptx

人生****奋斗








亲,该文档总共18页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

新课标人教版选修四市公开课一等奖百校联赛特等奖课件.pptx
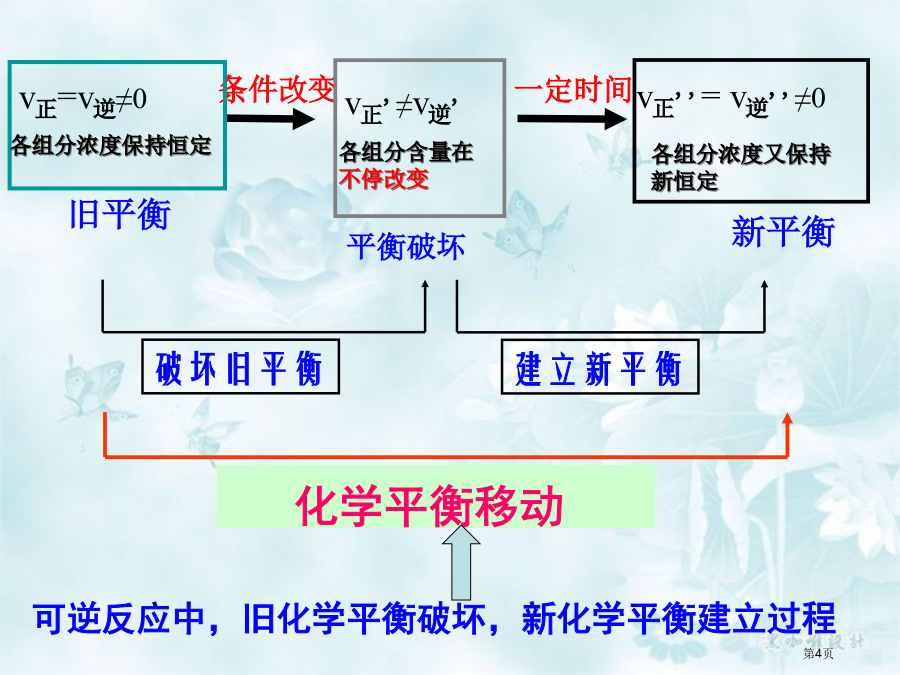
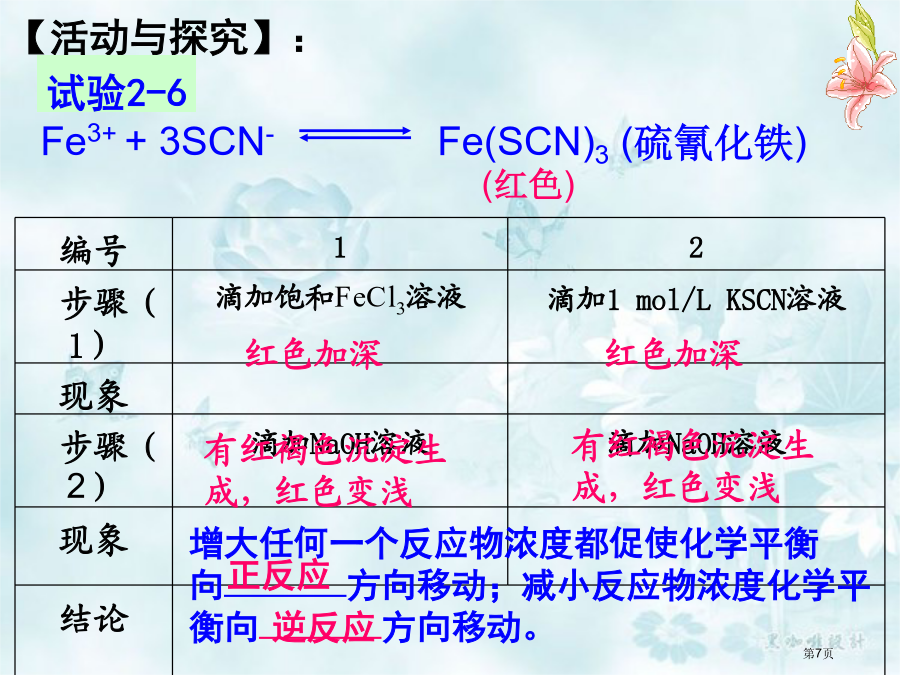
化学反应原理Cr2O72-+3C2H5OH+8H+→2Cr3++3CH3CHO+7H2O橙色绿色一、影响化学反应速率外界原因有哪些?二、化学平衡状态是指在一定条件下可逆反应里,正反应和逆反应速率相等,反应混合物中各组分浓度保持不变状态叫化学平衡状态。条件改变●平衡移动方向与正、逆反应速率关系:一、浓度对化学平衡影响:【活动与探究】:【思索】为何增大任何一个反应物浓度都能促进平衡向正反应方向移动?(试从浓度改变怎样影响正、逆反应速率来解释原因。)二、温度对化学平衡影响:→浓度增大结论:对于气体反应体系来说

新课标人教版市公开课一等奖百校联赛特等奖课件.pptx
教学目标设计试验,预测现象?完成试验Fe(OH)3先有灰白色沉淀,快速变成灰绿色,最终变成红褐色FeCl3溶液改变经过本节课学习总结我们研究和认识一个新化学物质基本思绪?下一节我们会学习铁盐和亚铁盐,思索我们会从哪些角度认识它们?它们可能有哪些化学性质?感激各位领导、同行们光临指导!

新课标人教版课件系列市公开课一等奖百校联赛特等奖课件.pptx
新课标人教版课件系列第一章《地理环境与区域展》教学目标教学重点、难点:1.遥感、全球定位系统、地理信息系统原理,以及数字地球含义。2.遥感、全球定位系统、地理信息系统在区域地理环境研究中应用。课时安排:2课时教具:多媒体课件第2节地理信息技术在区域地理环境研究中应用1.遥感(RS)含义、原理、主要步骤、优点一、遥感技术原理遥感技术优点2.遥感(RS)应用——资源调查、环境监测、自然灾害防御监测补充:遥感影像3种遥感影像地物颜色特征:二、全球定位系统(GPS)--导航、定位1.含义2.组成3.特点4.基本原

新课标人教版系列市公开课一等奖百校联赛特等奖课件.pptx
新课标人教版课件系列9.4《物态改变中能量交换》教学目标固态一、熔化热一、熔化热2.熔化热:一、熔化热晶体熔化过程中,当温度到达熔点时,吸收热量全部用来破坏空间点阵,增加分子势能,而分子平均动能却保持不变,所以晶体有固定熔点。非晶体没有空间点阵,熔化时不需要去破坏空间点阵,吸收热量主要转化为分子动能,不停吸热,温度就不停上升。因为在不一样温度下物质由固态变成液态时吸收热量不一样,而晶体有固定熔点,所以有固定熔化热,非晶体没有固定熔点,也就没有固定熔化热。二、汽化热2.汽化热一定质量物质,在一定温度和压强下

新课标人教版化学必修Ⅱ市公开课一等奖百校联赛特等奖课件.pptx
新课标人教版化学必修Ⅱ复习:二、化学能与热能相互转化怎样设计试验来了解反应中热量改变情况?[试验探究2—1]铝片与盐酸反应试验2-1试验2-1[试验2—2探究]:Ba(OH)2·8H2O与NH4Cl反应试验2-2试验探究2-3试验2-3【思索与交流】中和热测定装置随堂练习2.以下反应既属于氧化还原反应,又属于吸热反应是()3、如右图所表示,把试管放入盛有25℃时饱和石灰水烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答以下问题:(1)试验中观察到现象是(2)产生上述现象原因是(3)
