
(浙江版)2021高考化学一轮复习 专题一 物质的组成、性质和分类课件.pptx

Th****s3







亲,该文档总共19页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

(浙江版)2021高考化学一轮复习 专题一 物质的组成、性质和分类课件.pptx
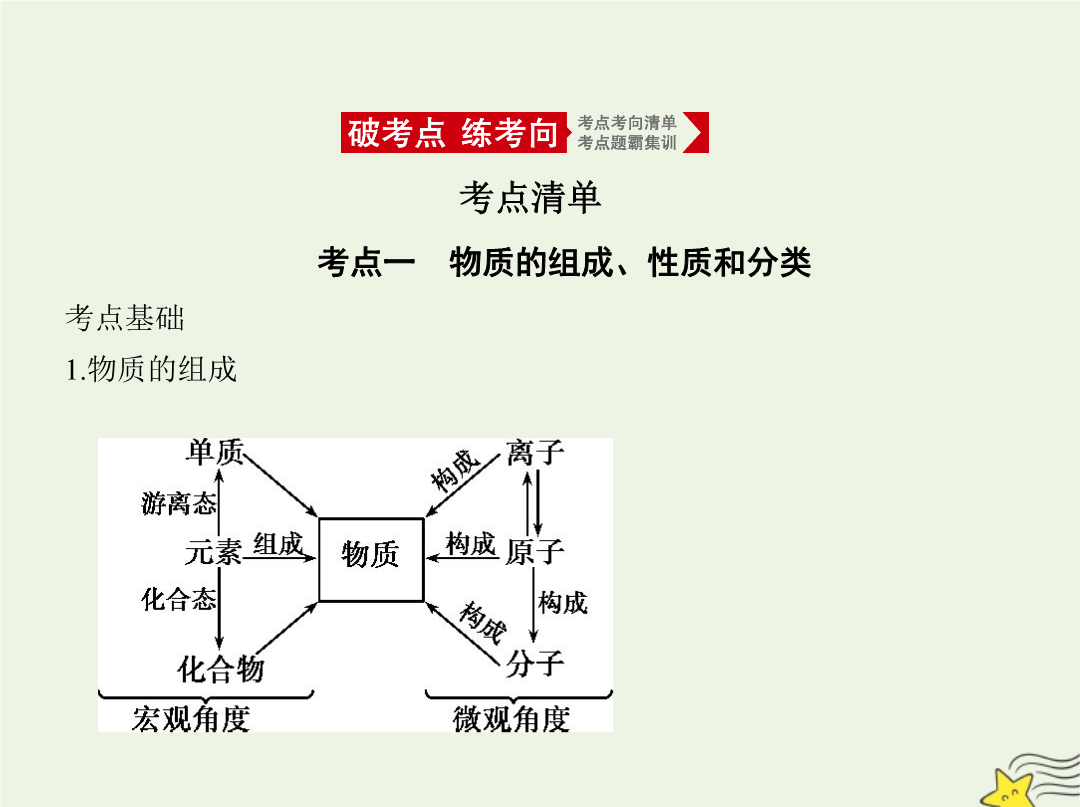
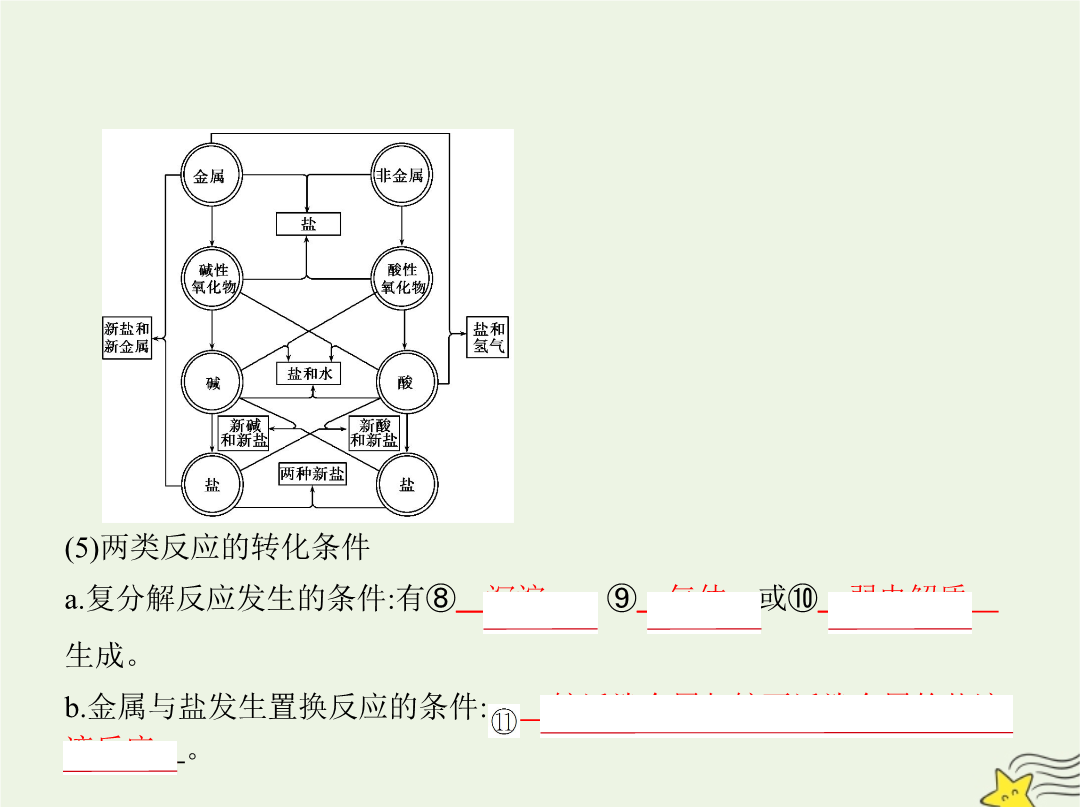
考点一物质的组成、性质和分类考点基础1.物质的组成 (1)宏观上,物质由①元素组成。(2)微观上,物质由②分子、原子或离子构成。2.物质的性质与变化(2)物质的变化a.物理变化:物质仅发生状态或外形的改变,而没有生成⑤新的物质的变化。b.化学变化:物质发生变化时有⑥新的物质生成的变化。在化学变化中常伴随有发光、放热、变色、放出气体、生成沉淀等现象。化学变化不仅有物质的变化,同时还伴随能量的变化,其实质是⑦旧化学键的断裂和新化学键的形成。(3)化学反应的分类 (4)单质、氧化物、酸、碱、盐等物质之间的相互转

2021高考化学一轮复习 专题一 物质的组成、性质和分类课件.pptx
考点一物质的组成、性质和分类二、分类的方法1.单一分类法单一分类法就是对被分类的对象只用一种标准进行分别归类的分类方法,如:3.树状分类法所谓树状分类法,简单地说,是根据被分类对象的整体与分出的类别间的关系及其陈列式的形状(像树)来定义的,如下图: 核心精讲一、物质分类中易混淆的概念1.酸的元数不一定等于酸分子中的H原子数。如亚磷酸(H3PO3)是二元酸,次磷酸(H3PO2)是一元酸,因为它们的结构分别是 、 。2.无氧酸不一定是非金属元素的氢化物,如氢氰酸(HCN)等。3.酸的氧化性与氧化性酸不同。酸的

(湖南版)2021高考化学一轮复习 专题1 物质的组成、性质和分类课件.pptx
考点清单考点一物质的组成、性质和分类一、物质的组成1.宏观上物质由①元素组成,元素在自然界有两种存在形式,以单质形式存在的称为元素的②游离态,以化合物形式存在的称为元素的③化合态。厘清概念:(1)元素:具有相同核电荷数的一类原子的总称。(2)单质:同种元素组成的纯净物。(3)化合物:不同种元素组成的纯净物。(4)纯净物:由同种单质或化合物组成的物质。(5)混合物:由几种不同的单质或化合物组成的物质。2.微观上质子、中子、④电子是构成原子的三种基本粒子,分子、原子、⑤离子是构成物质的三种基本微粒。厘清概念:

(北京版)2021高考化学一轮复习 专题二 物质的组成、性质和分类课件.pptx
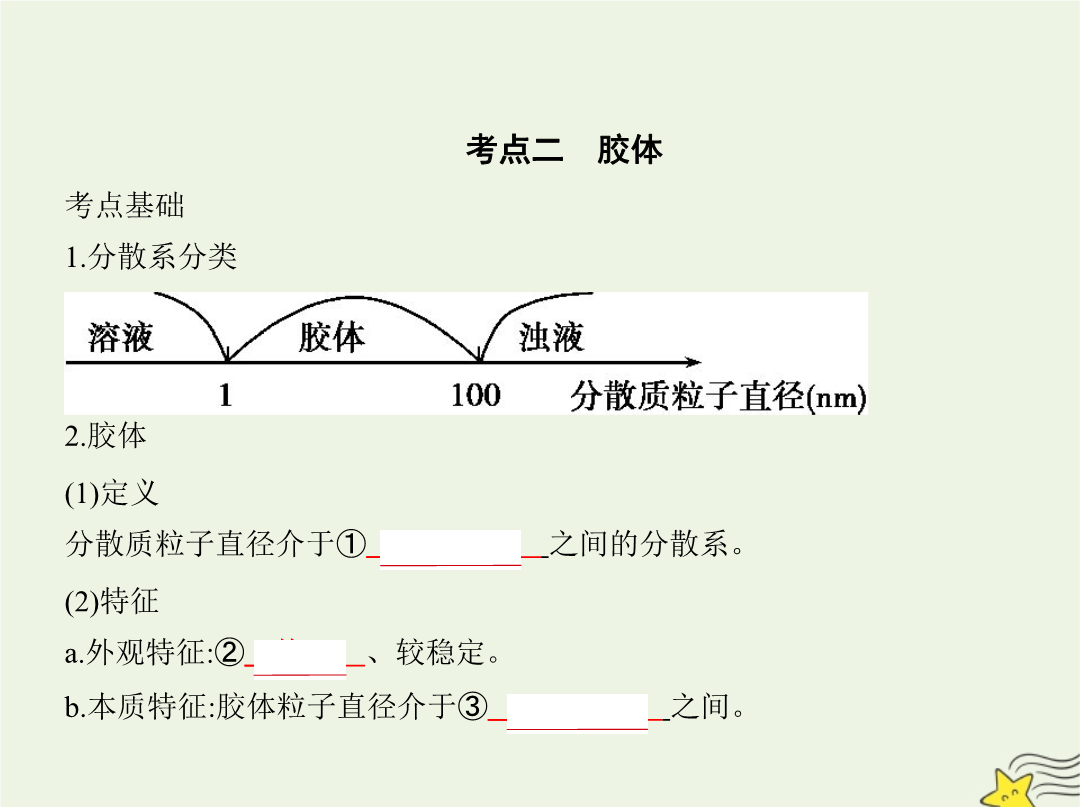
考点清单2.物质的性质(1)化学变化不仅有物质的变化,同时还伴随有能量变化,实质是旧化学键的断裂和新化学键的形成。(2)化学性质是指物质发生化学变化时所表现出的性质,它包括金属性和非金属性、氧化性和还原性、酸性和碱性等。3.物质的分类方法(1)单一分类法单一分类法就是将被分类的对象只用一种标准进行分别归类的方法,此法所依据的标准有一定的局限性,所提供的信息较少。(2)交叉分类法交叉分类法就是将被分类的对象用多种不同的分类标准进行分类的方法,如: 考点基础1.分散系分类 (4)性质及其应用(5)Fe(OH)

(课标版)2021高考化学一轮复习 专题一 物质的组成、性质和分类课件.pptx
考点一物质的组成、性质和分类二、分类的方法1.交叉分类法交叉分类法就是将被分类的对象用多种不同的分类标准进行分类,如: 2.树状分类法所谓树状分类法,简单地说,是根据被分类对象的整体与分出的类别间的关系及其陈列式的形状(像树)来定义的,如下图:重点突破一、物质分类中易混淆的概念1.名称中有“酸”的物质不一定是酸,如石炭酸(C6H5OH)是酚,不是酸。2.酸的元数不一定等于酸分子中的H原子数。如亚磷酸(H3PO3)是二元酸,次磷酸(H3PO2)是一元酸,因为它们的结构分别是 、 。3.无氧酸不一定是非金属元
