
溶液的酸碱性-ppt课件.ppt

知识****SA





亲,该文档总共42页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

溶液的酸碱性ppt课件.ppt
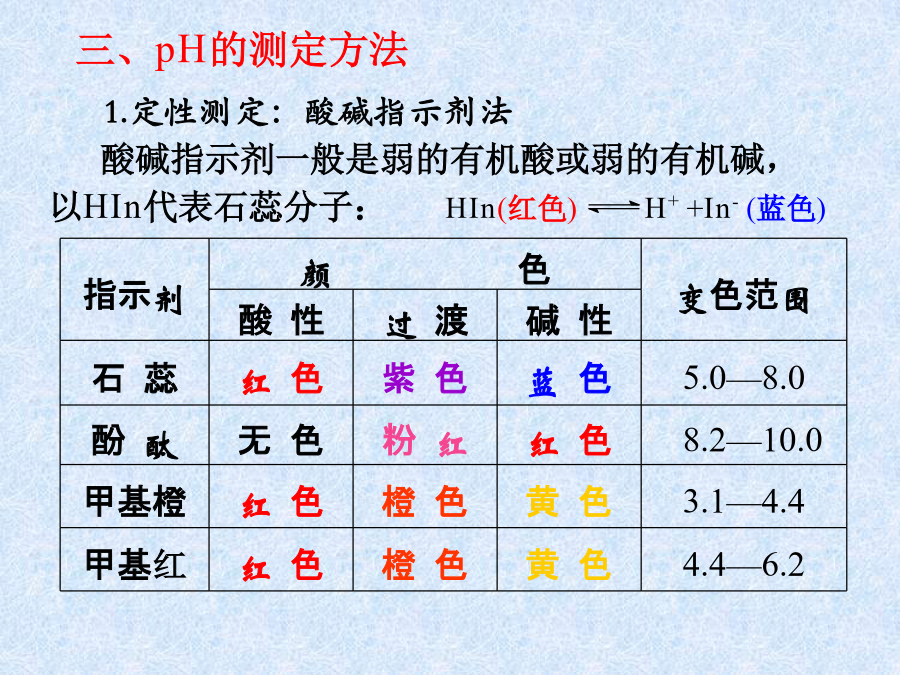
8.1溶液的酸碱性酸“摸起来滑滑的”区分酸性溶液和碱性溶液交流实验结果,归纳出指示剂变色情况与溶液酸碱性的关系,结果列表如下能跟酸性溶液或碱性溶液起作用而显不同颜色的物质叫做酸碱指示剂,简称指示剂。石蕊和酚酞是常见的指示剂。检验溶液酸碱性强弱的程度溶液的酸碱度常用pH来表示,pH范围通常在0~14之间。pH<7溶液呈酸性pH>7溶液呈碱性pH=7溶液呈中性检验溶液酸碱性强弱的程度注意:(1)不能直接把pH试纸浸入待测溶液中,以免带入杂质,污染试液。(2)不能先用水将pH试纸润湿,再进行测试,因为用水润湿后

溶液的酸碱性-ppt课件.ppt
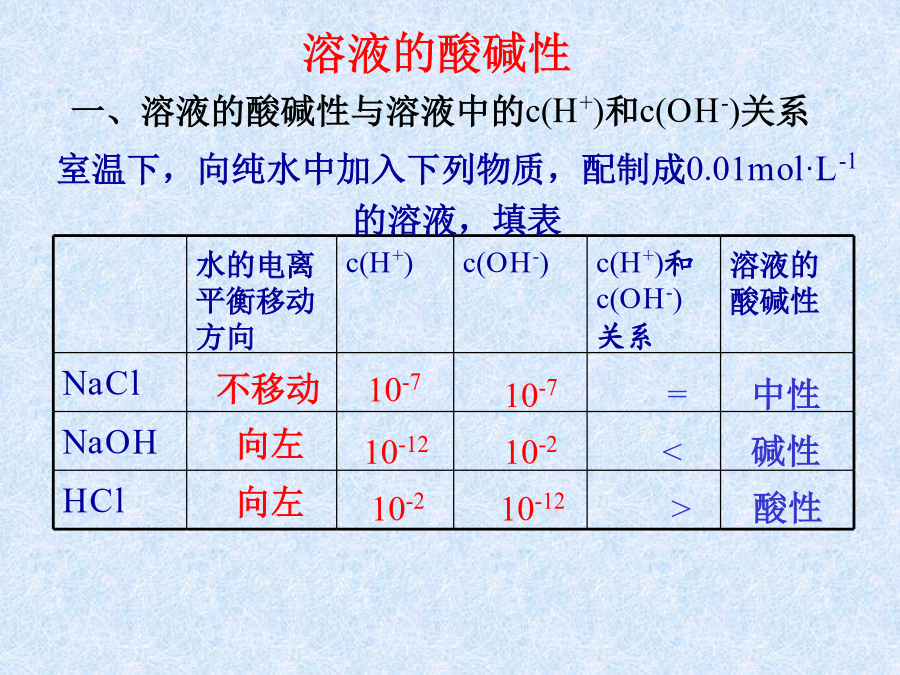
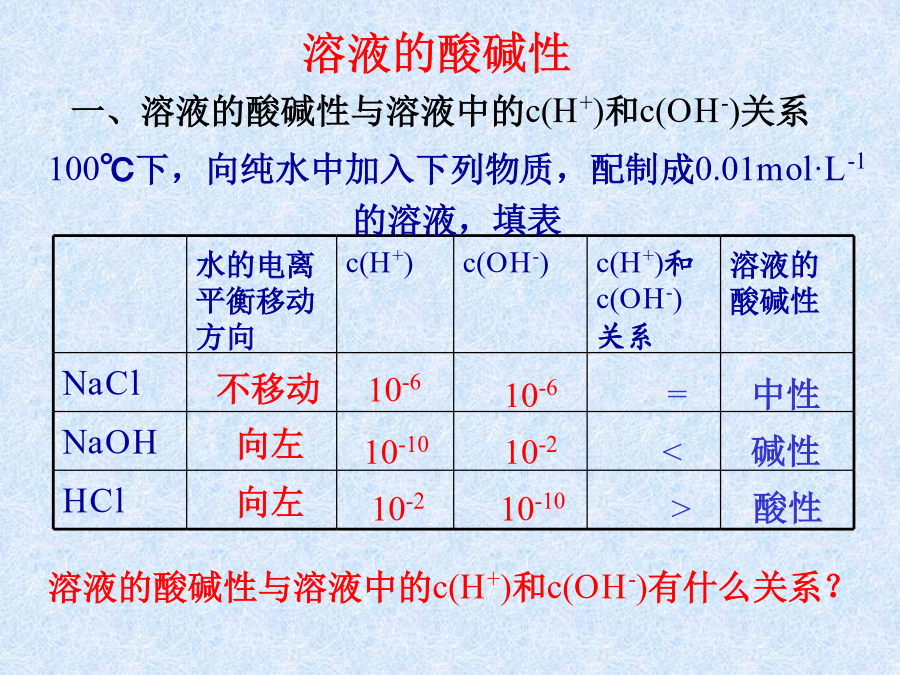
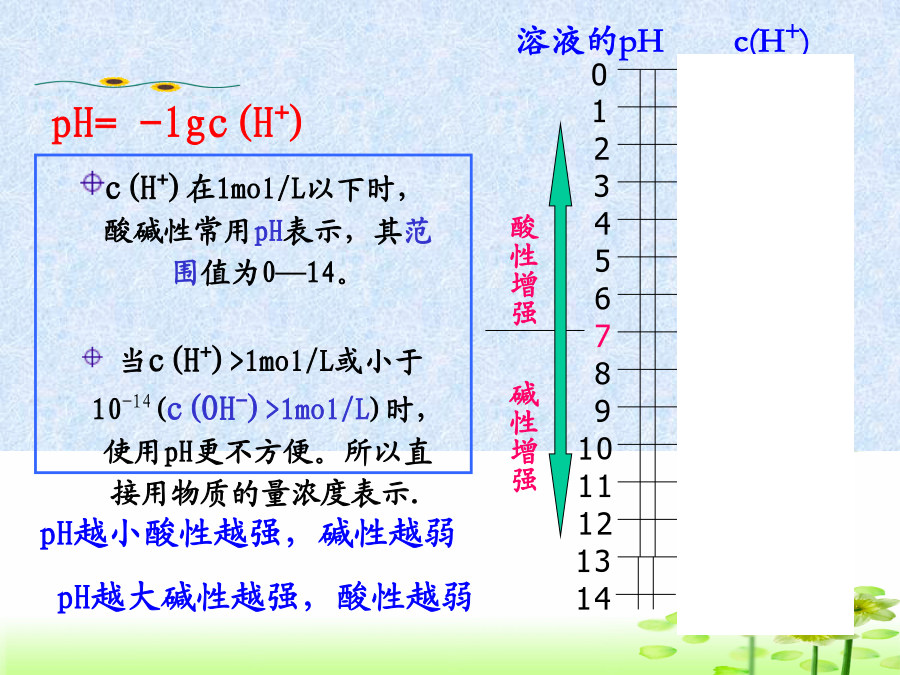
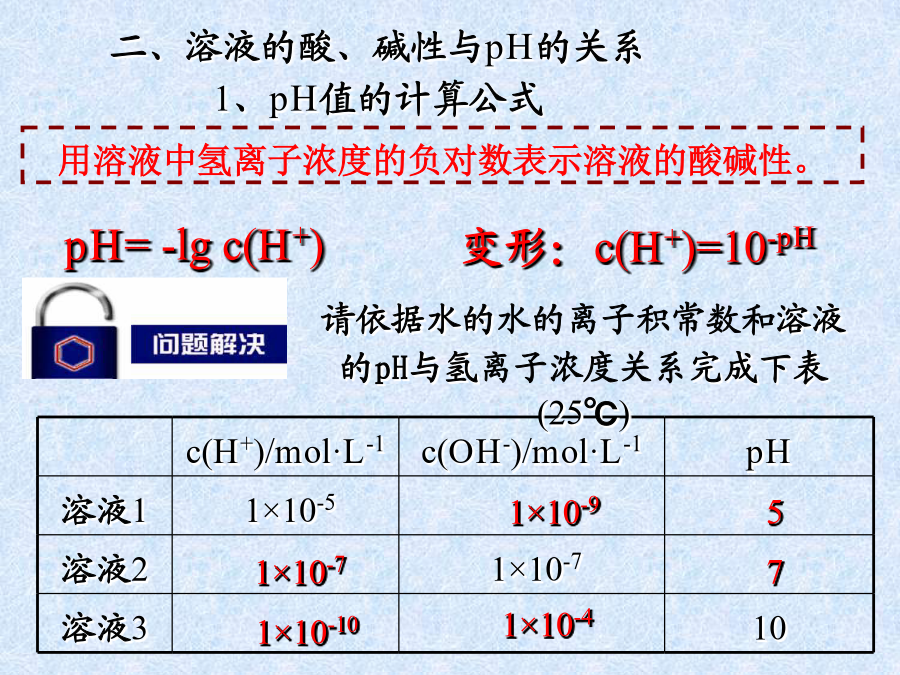
专题3溶液中的离子反应健康人的体液pH必须维持在一定范围内。溶液的酸碱性溶液的酸碱性溶液的酸碱性取决于c(H+)和c(OH-)的相对大小溶液的pHc(H+)二、溶液的酸、碱性与pH的关系1、pH值的计算公式三、pH的测定方法对于一元强酸与一元强碱中和反应则:c(H+)V酸=c(OH-)V碱酸式滴定管、碱式滴定管、(移液管)铁架台、滴定管夹、锥形瓶等。玻璃活塞滴定管与量筒区别(1)酸式滴定用的是玻璃活塞,碱式滴定管用的是橡皮管。(思考为什么?)左手指示剂的选择和滴定终点的判断(1)滴定前准备a检查滴定管:酸

溶液的酸碱性-ppt课件.ppt
21530

新溶液的酸碱性ppt课件.ppt
通常禁止对实验室中的化学试剂采用“尝味试验法”了解其味道。那我们怎么确定该物质是否有酸味或酸性呢?回忆:将二氧化碳通入滴有紫色石蕊试液的水中,看到现象:。遇酸性溶液紫色石蕊试液遇中性溶液遇碱性注意现有两瓶失去标签的无色溶液,一瓶是稀盐酸,一瓶是氢氧化钠溶液,请你通过鉴别,贴上标签。检验酸碱溶液的操作步骤:石蕊试纸的使用方法:酸性溶液使蓝色石蕊试纸,碱性溶液使红色石蕊试纸。观察下图,并完成下列填空:1、溶液的酸碱性:pH=7,溶液呈性;pH<7,溶液呈性;pH>7,溶液呈性。2、溶液的pH与酸碱性强弱的关系

溶液的酸碱性说课稿ppt课件.ppt
《化学反应原理》专题3溶液的酸碱性二、学情分析六、教学过程3、学习溶液酸碱性与pH3、学习溶液酸碱性与pH(25℃)1、酸碱指示剂:判断溶液的酸碱性范围此课件下载可自行编辑修改,供参考!感谢您的支持,我们努力做得更好!
