
新药研发流程专家讲座.pptx

王子****青蛙








亲,该文档总共12页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

新药研发流程专家讲座.pptx
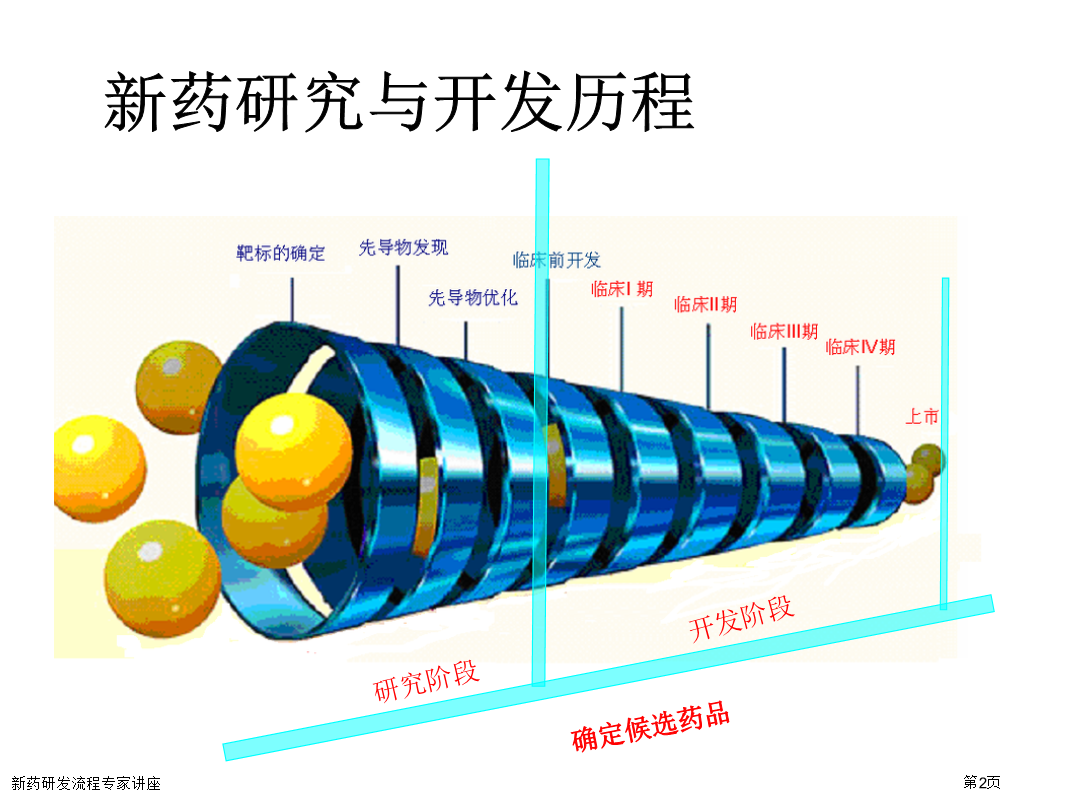
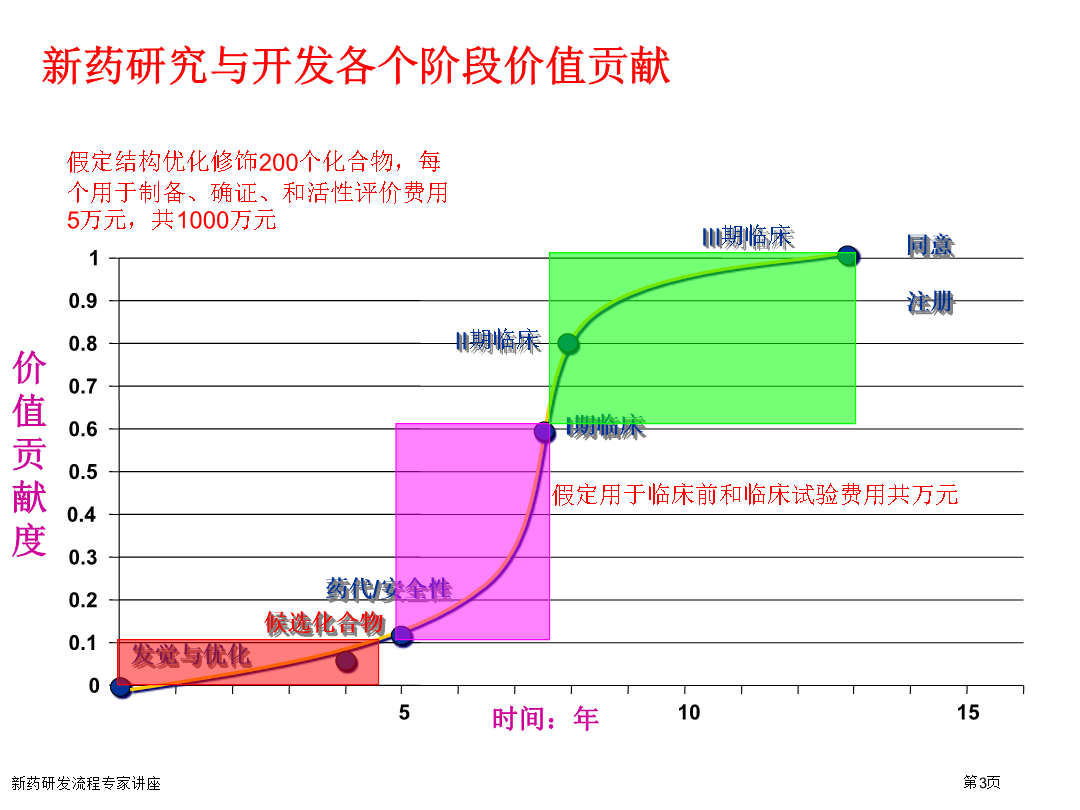
新药研究与开发历程0五、新药申请(NDA)六、上市及监测

新药研发流程专家讲座.pptx
新药研究与开发历程0五、新药申请(NDA)六、上市及监测

现代新药研发的思考专家讲座.pptx
当代新药研发思索一研发特点二存在问题三必备条件四总体思路五基本做法六关键部分七总体展望一、研发特点一、研发特点年全球年销售额40亿美元以上药品年全球年销售额40亿美元以上药品年全球制药企业销售60亿美元以上名单(一)年全球制药企业销售60亿美元以上名单(二)全球主要制药企业R&D投入比较(一)全球主要制药企业R&D投入比较(二)全球主要制药企业R&D投入比较(三)世界十大药业巨头拳头产品一览表(一)世界十大药业巨头拳头产品一览表(二)世界十大药业巨头拳头产品一览表(三)世界十大药业巨头拳头产品一览表(四)

新药研发注册申报资料详解专家讲座.pptx
新药注册申报资料讲解广州蓝韵医药研究有限企业专注中药新药和保健食品研发技术外包服务《药品注册管理方法》法规要求:对于注册分类1品种,临床试验完成后应依据临床期间进行各项研究结果,重新整理报送资料项目1~30全部资料同时申请注册属于注册分类3原料药和属于注册分类6制剂,其原料药注册申请应该符合申报生产要求。申请注册已经有国家标准药品:按照《申报资料项目表》要求报送资料项目1~16和28~30。需进行临床试验,在临床试验完成后报送资料项目28~32以及其它变更和补充资料,并按申报资料项目次序排列。分三类:A:

新药研发注册申报资料详解专家讲座.pptx
新药注册申报资料讲解广州蓝韵医药研究有限企业专注中药新药和保健食品研发技术外包服务《药品注册管理方法》法规要求:对于注册分类1品种,临床试验完成后应依据临床期间进行各项研究结果,重新整理报送资料项目1~30全部资料同时申请注册属于注册分类3原料药和属于注册分类6制剂,其原料药注册申请应该符合申报生产要求。申请注册已经有国家标准药品:按照《申报资料项目表》要求报送资料项目1~16和28~30。需进行临床试验,在临床试验完成后报送资料项目28~32以及其它变更和补充资料,并按申报资料项目次序排列。分三类:A:
