
大气圈及大气污染.ppt

小沛****文章









亲,该文档总共102页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

大气圈及大气污染.ppt
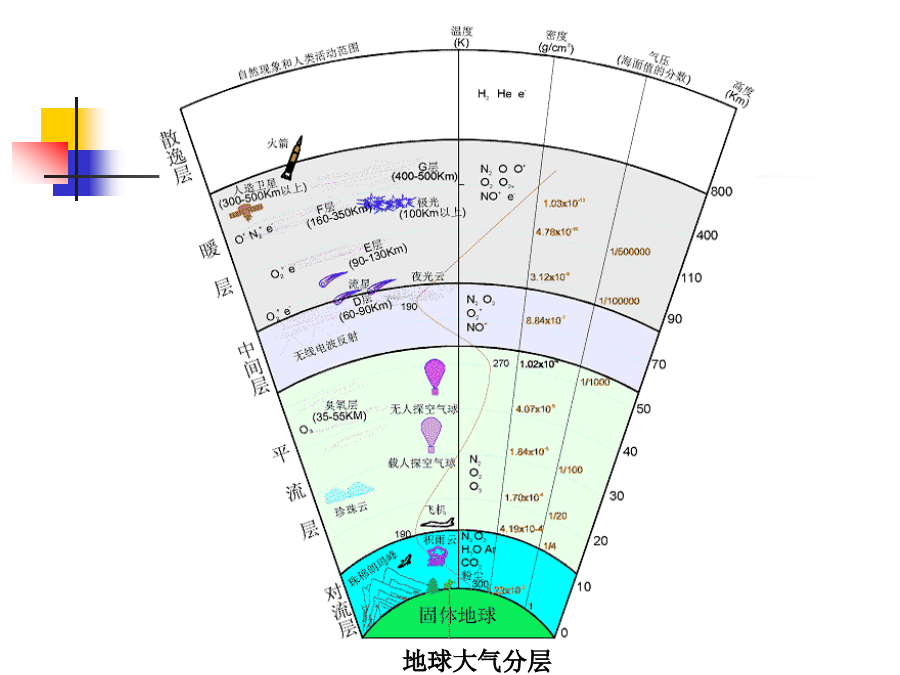
第二章大气圈及大气污染2.1大气圈地球大气分层2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈地球大气组成2.2大气污染(二)大气污染源按污染源存在的形式划分为:(1)固定污染源如工厂的排烟与排气。(2)移动污染源如汽车、机车等。按污染源排放方式划分为:(1)高架源如污染物通过烟囱排放。(2)面源如采矿工作面排出的气体。(3)线源如汽车、机车行驶排出气体。2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.

大气圈及大气污染.ppt
第二章大气圈及大气污染2.1大气圈地球大气分层2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈地球大气组成2.2大气污染(二)大气污染源按污染源存在的形式划分为:(1)固定污染源如工厂的排烟与排气。(2)移动污染源如汽车、机车等。按污染源排放方式划分为:(1)高架源如污染物通过烟囱排放。(2)面源如采矿工作面排出的气体。(3)线源如汽车、机车行驶排出气体。2.2大气污染2.

大气圈及大气污染.ppt
第二章大气圈及大气污染2.1大气圈地球大气分层2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈2.1大气圈地球大气组成2.2大气污染(二)大气污染源按污染源存在的形式划分为:(1)固定污染源如工厂的排烟与排气。(2)移动污染源如汽车、机车等。按污染源排放方式划分为:(1)高架源如污染物通过烟囱排放。(2)面源如采矿工作面排出的气体。(3)线源如汽车、机车行驶排出气体。2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.2大气污染2.

大气圈与天气.ppt
风2.3大气的运动地面注意地面冷热不均【走近生活】海陆风海陆风想一想:A地面图17地面地面(百帕)1000100510102.地转偏向力在气压梯度力和地转偏向力共同作用下的风(北半球高空)近地面风的形成过程(北半球)理想风的风向规律(等压线平行)小结:画风向的步骤想一想:

大气圈的组成与结构.ppt
第二节大气圈与天气、气候一、大气圈的组成与结构组成成分(二)、大气圈的结构高度Km大气的垂直分层大气的垂直分层大气的垂直分层分层①图中正确表示大气层气温垂直变化的曲线是()A.①B.②C.③D.④②对短波通信具有重要意义的电离层位于()A.Ⅰ层顶部B.Ⅱ层底部C.Ⅱ层中部D.Ⅲ层C二、大气的受热过程太阳辐射光谱示意图削弱作用(二)、大气的温室效应?低层大气分层太阳ks5u精品课件
