
辽宁省丹东七中2015九年级化学上册 第十单元 课题1 常见的酸和碱研学案(无答案)(新版)新人教版.doc

书生****ma




在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

辽宁省丹东七中2015九年级化学上册 第十单元 课题1 常见的酸和碱研学案(无答案)(新版)新人教版.doc
4课题1常见的酸和碱第一课时【课前预习】1、向紫色的石蕊中通入CO2会有什么现象产生2、完成化学方程式:(1)盐酸和金属铝反应(2)盐酸除铁锈(3)服用AI(OH)3可中和过多的胃酸(4)写出实验室制取CO2

辽宁省丹东七中2015九年级化学上册 第十单元 课题1 常见的酸和碱研学案(无答案)(新版)新人教版.doc
4课题1常见的酸和碱第一课时【课前预习】1、向紫色的石蕊中通入CO2会有什么现象产生2、完成化学方程式:(1)盐酸和金属铝反应(2)盐酸除铁锈(3)服用AI(OH)3可中和过多的胃酸(4)写出实验室制取CO2

学案-辽宁-2015_辽宁省丹东七中2015九年级化学上册 第十单元 课题1 常见的酸和碱研学案(无答案)(新版)新人教版.rar
1课题1常见的酸和碱第一课时【课前预习】1、向紫色的石蕊中通入CO2会有什么现象产生2、完成化学方程式:(1)盐酸和金属铝反应(2)盐酸除铁锈(3)服用AI(OH)3可中和过多的胃酸(4)写出实验室制取CO2的化学方程式【研学过程】请按照下面的问题提示,在仔细阅读教材的基础上进行自学知识点一:1、酸碱指示剂知识点二:浓酸的性质1、浓盐酸的性质(挥发性)2、浓硫酸的性质(脱水性和吸水性)3、浓硫酸的稀释4、如果浓硫酸弄到皮肤或衣服怎么处理知识点三:稀酸的

辽宁省丹东七中2015九年级化学上册 第十单元 酸和碱复习研学案(无答案)(新版)新人教版.doc
4酸和碱通过旧知复习完成表格内容知识点一:常见的酸和碱浓盐酸浓硫酸颜色状态挥发性吸水性脱水性腐蚀性稀释是否放热氢氧化钠氢氧化钙俗称颜色状态溶解性腐蚀性是否潮解溶解热量变化知识点二:酸和碱的化学性质稀盐酸稀硫酸酸的化学性质指示剂1.使石蕊溶液变色2.使酚酞溶液变色金属Zn+HCl-Fe+H2SO4-金属氧化物Fe2O3+HCl-CuO+H2SO4-碱Fe(OH)3+HCl-Cu(OH)2+H2SO4-碳酸盐C
学案-全国-2019_2019春九年级化学下册 第十单元 酸和碱 课题1 常见的酸和碱学案(无答案)(新版)新人教版.doc
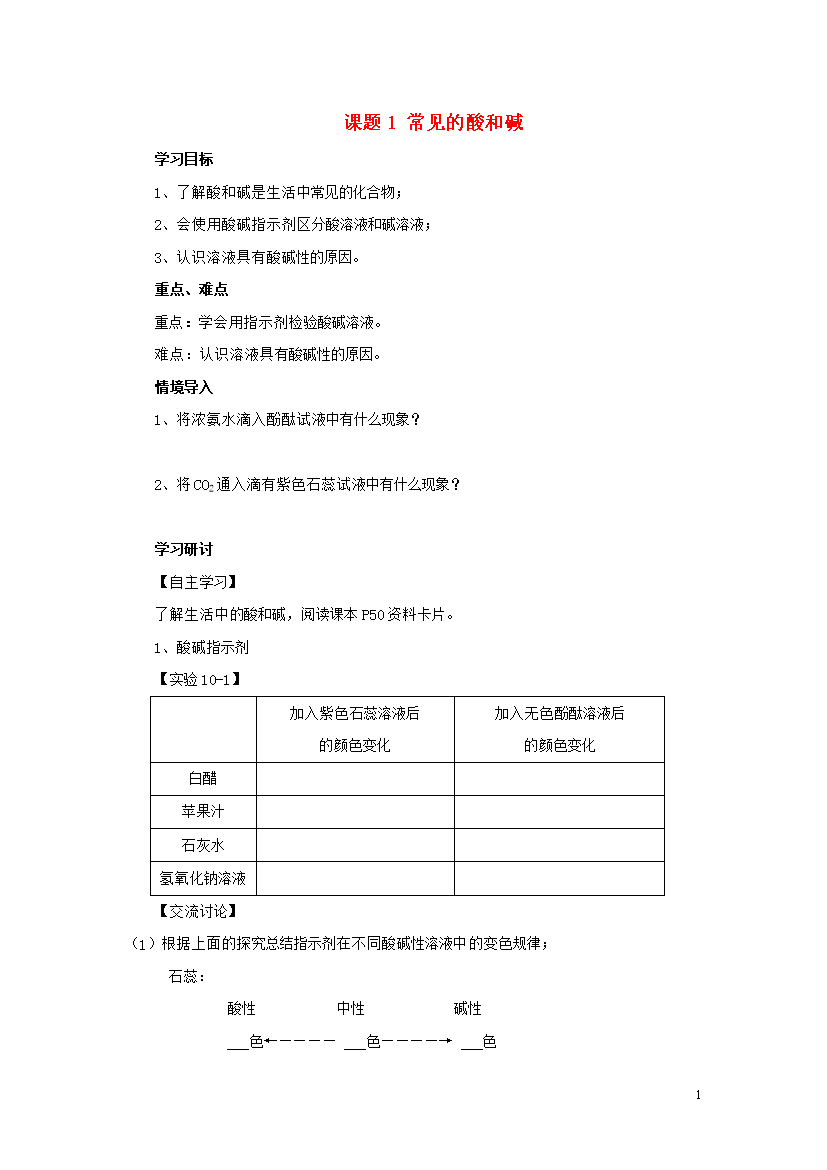
1课题1常见的酸和碱学习目标1、了解酸和碱是生活中常见的化合物;2、会使用酸碱指示剂区分酸溶液和碱溶液;3、认识溶液具有酸碱性的原因。重点、难点重点:学会用指示剂检验酸碱溶液。难点:认识溶液具有酸碱性的原因。情境导入1、将浓氨水滴入酚酞试液中有什么现象?2、将CO2通入滴有紫色石蕊试液中有什么现象?学习研讨【自主学习】了解生活中的酸和碱,阅读课本P50资料卡片。1、酸碱指示剂【实验10-1】加入紫色石蕊溶液后的颜色变化加入无色酚酞溶液后的颜色变化白醋苹果
