
麦克斯韦玻尔兹曼分布.ppt

YY****。。






亲,该文档总共25页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

麦克斯韦玻尔兹曼分布.ppt
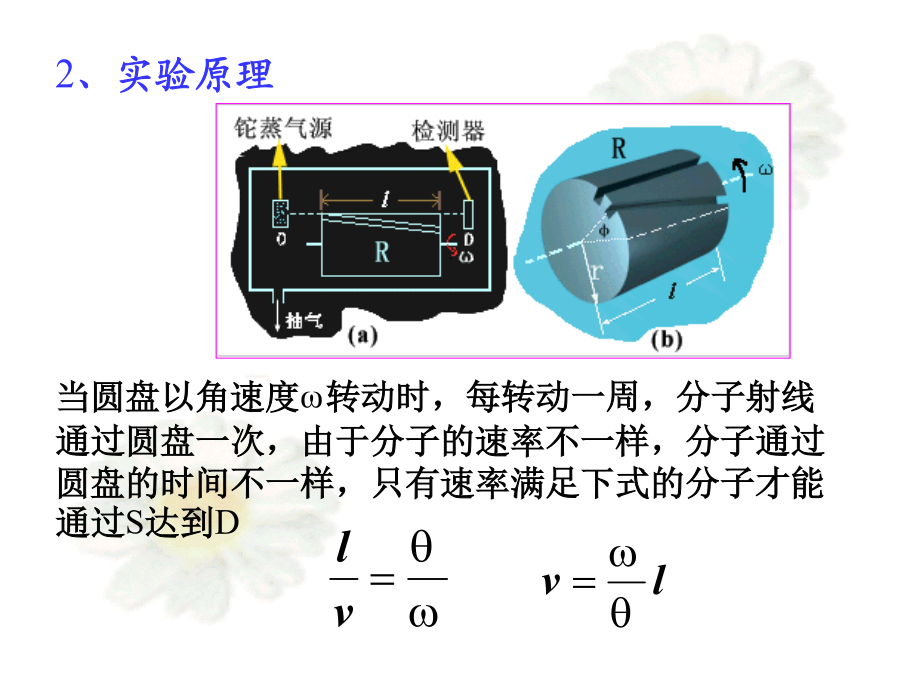
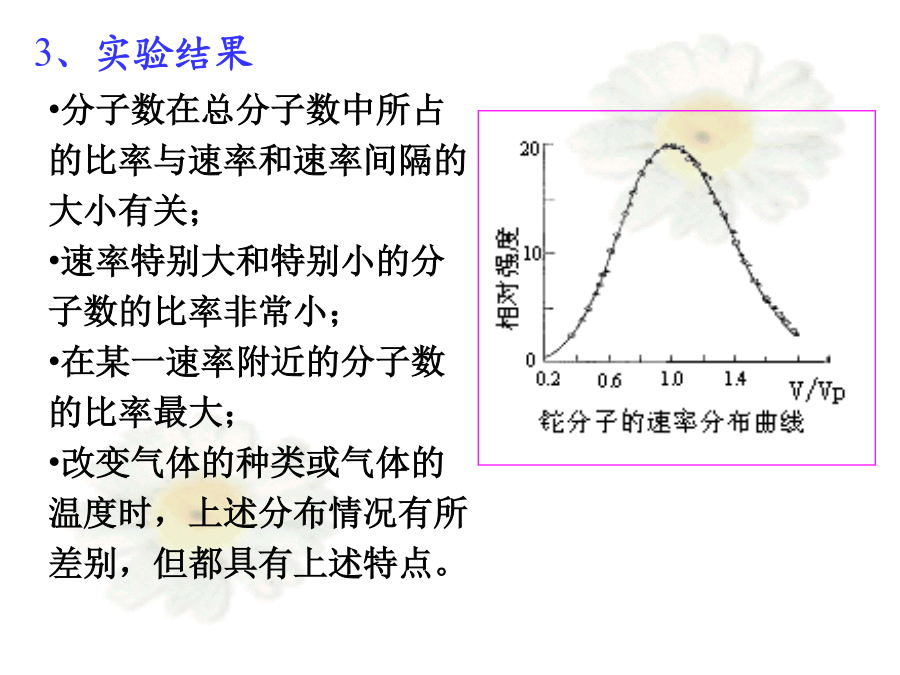
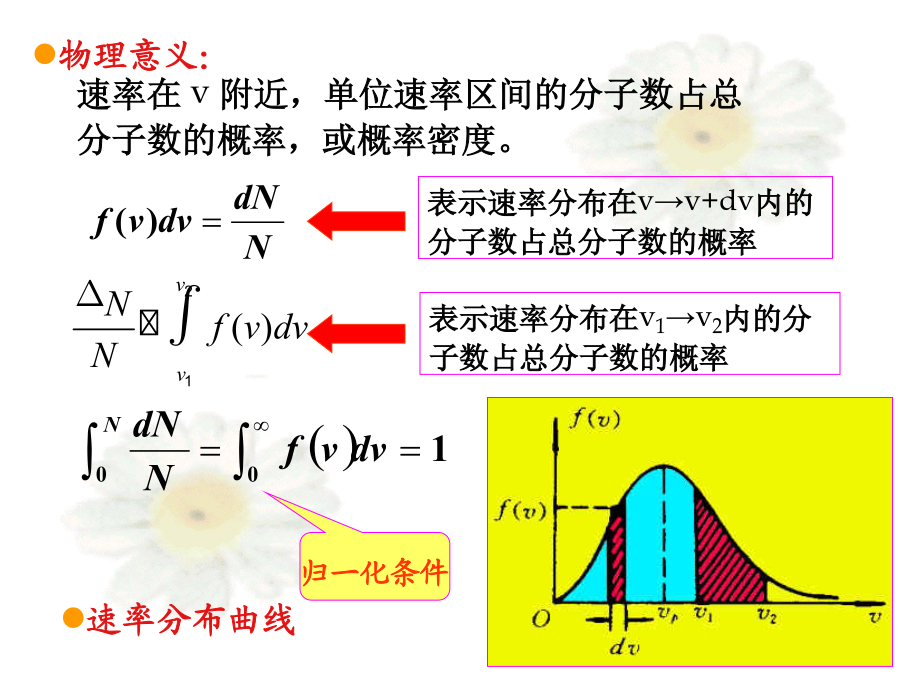
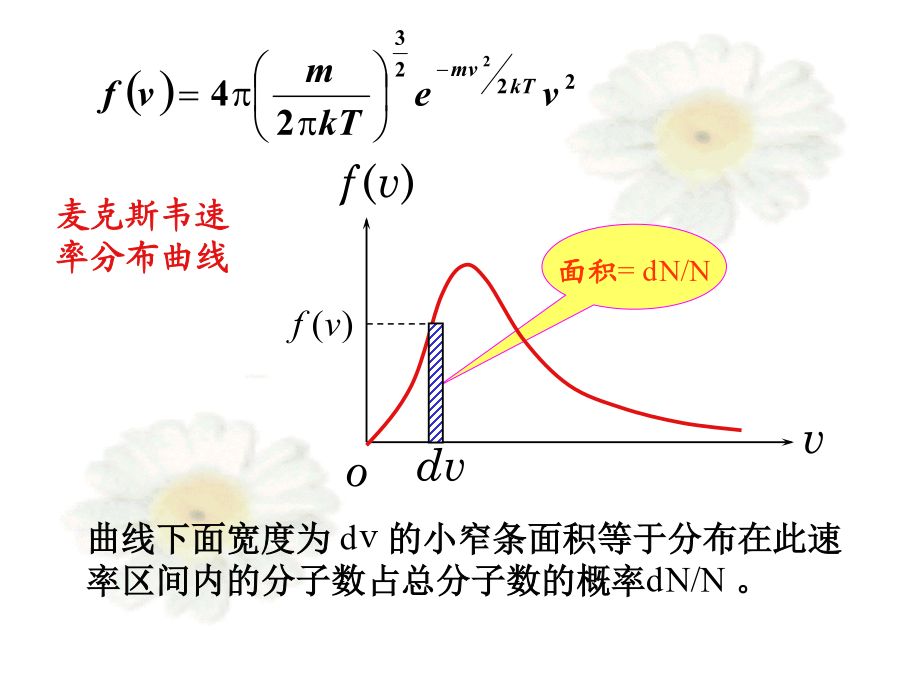
8-4麦克斯韦-玻尔兹曼分布麦克斯韦(JamesClerkMaxwell1831——1879)一、测定气体分子速率的实验2、实验原理3、实验结果二、麦克斯韦气体分子速率分布律物理意义:速率在v附近,单位速率区间的分子数占总分子数的概率,或概率密度。2、麦克斯韦速率分布律在平衡态下,当气体分子间的相互作用可以忽略时,分布在任一速率区间v~v+dv的分子数占总分子数的比率为曲线下面宽度为dv的小窄条面积等于分布在此速率区间内的分子数占总分子数的概率dN/N。定义:与f(v)极大值相对应的速率,称为最概然速率。

麦克斯韦玻尔兹曼统计学习资料.pptx
会计学2024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/232024/10/2320

§4-5-玻尔兹曼分布率.pptx
一、玻尔兹曼分布率玻尔兹曼将麦克斯韦速率分布推广到分子在保守力场中运动时旳情形。零势能处单位体积内具有多种速度旳分子数二、重力场中气体分子高度旳分布在z高度单位体积内旳分子数

thermal6 玻尔兹曼分布律.ppt
§3.1气体分子的速率分布律平衡态理想气体分子热运动Maxwell分布律:#、Maxwell速度分布律(1)泻流气体从薄壁容器很小的小孔中逸出称为泻流。处于平衡态的气体,在dt时间内,从△A面积小孔逸出的分子数△N’具体求出分子束速率分布。dt时间内从dA面积的小孔逸出的分子数可写为,分子束中的速率分布F(v)dv。利用气体分子平均速率公式,分子束速率分布F(v)dv可表示为(1)泻流自由电子经典模型:金属中的自由电子的能量要比金属外空气中的游离电子的能量低W(脱出功)。自由电子脱出金属表面必须做功,所做

麦克斯韦速度分布律.ppt
8.5麦克斯韦分布律8.5.1麦克斯韦速度分布律8.5.2麦克斯韦速率分布律8.5.3平均速率方均根速率高斯积分公式(a为正的常量):速度出现在P(vx,vy,vz)点附近,单位速度空间体积内的分子数占系统分子总数的百分比。归一化条件:2.麦克斯韦速度分布律速度分布函数:麦克斯韦速度分布律速率出现在v附近的单位速率区间的分子数,占系统分子总数的百分比。2.麦克斯韦速率分布律平衡态系统中分子的速率分布函数:速率处于v到v+dv区间的分子数占分子总数的百分比。速度平方的平均值:分子的方均根速率:【例8.8
