
吸收法净化气态污染物.ppt

YY****。。






亲,该文档总共80页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

吸收法净化气态污染物.doc
第九章吸收法净化气态污染物9.1浓度为0.03(摩尔分数)的稀氨水,在30℃时氨的平衡分压为3.924kPa,氨水上方的总压为101.3kPa,其相平衡关系服从亨利定律。稀氨水密度近似取1000kg/m3,试计算亨利系数E、溶解度系数H及相平衡常数。解:由x=p*/E得享利系数:E=p*/x=3.942×103/0.03=1.314×105pa溶解度系数:H===0.423mol/Pa·m3因为y*=P*/P=3.942/101.3=0.039又由y*=mx得相平衡常数:m=y*/x=0.039/0.03

吸收法净化气态污染物.ppt
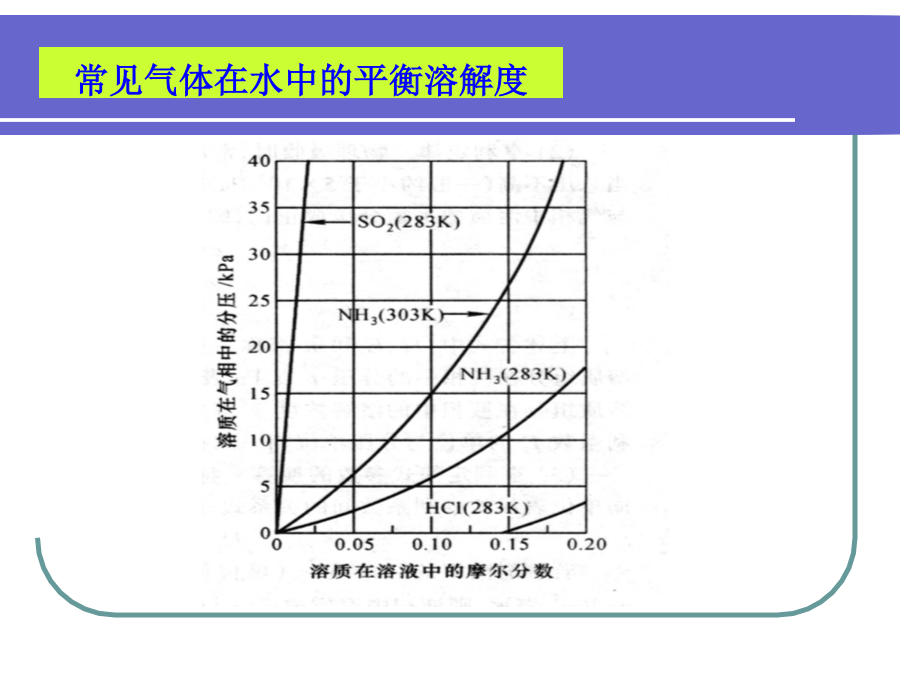
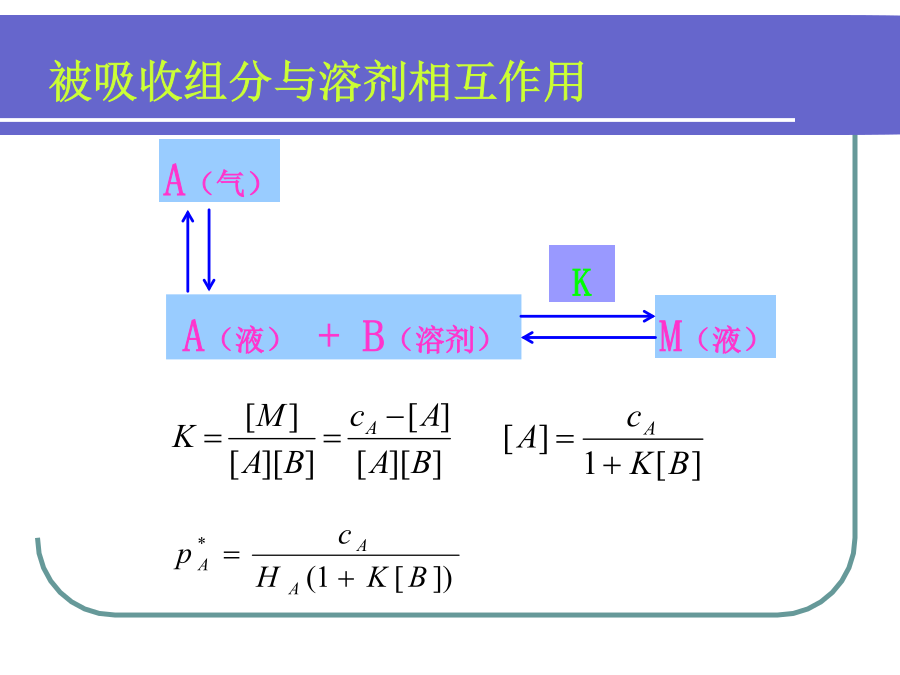
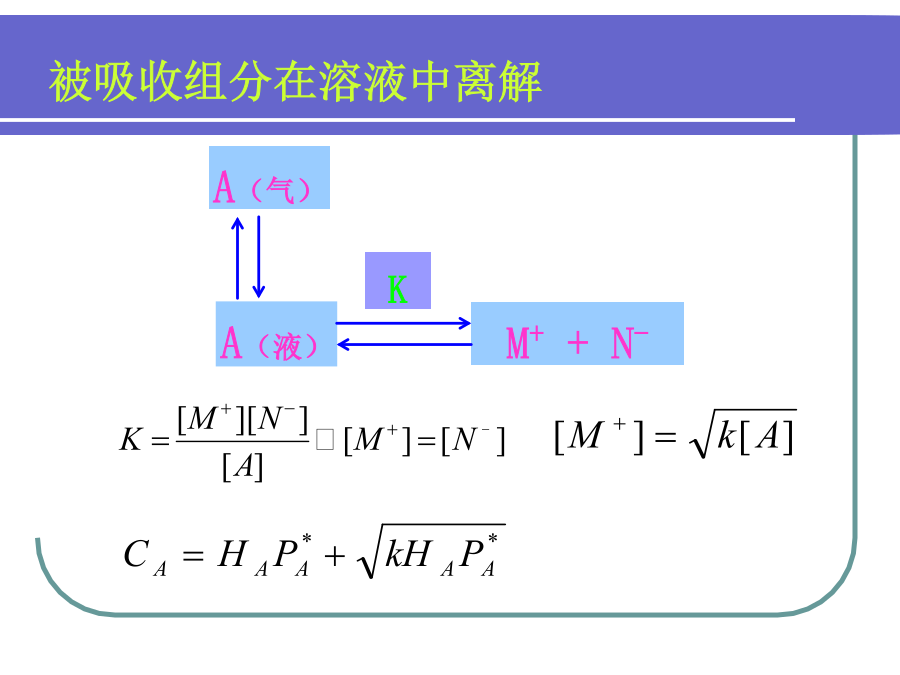
第8章吸收法净化气态污染物吸收是根据气体混合物中各组分在液体溶剂中物理溶解度差异或者化学反应活性的不同,将污染物从气相中分离出来的一种方法。物理吸收:物理溶解度差异吸收剂常见气体在水中的平衡溶解度物理吸收平衡--亨利定律亨利定律的适用条件A(液)+B(溶剂)A(液)A(液)+B(液)8.2吸收机理气态污染物A通过隋性气体B运动,用扩散系数DAB表示:扩散系数随介质的种类、温度、压强及浓度的不同而变化。气体扩散速率实验示意图ρA1-气体A的密度,g/cm3。L1-液体的初始速度,cm;L2-液体的最终速度,

吸收法净化气态污染物.ppt
大气污染控制工程第五章吸收法净化气态污染物第五章吸收法净化气态污染物第五章吸收法净化气态污染物第一节吸收平衡一、物理吸收平衡一、物理吸收平衡二、化学吸收平衡二、化学吸收平衡二、化学吸收平衡由亨利定律有:二、化学吸收平衡第二节吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率吸收设

第5章吸收法净化气态污染物.ppt
大气污染控制工程第五章吸收法净化气态污染物第五章吸收法净化气态污染物第五章吸收法净化气态污染物第一节吸收平衡一、物理吸收平衡一、物理吸收平衡二、化学吸收平衡二、化学吸收平衡二、化学吸收平衡由亨利定律有:二、化学吸收平衡第二节吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率一、物理吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学吸收速率二、化学

11---气态污染物的净化-111-吸收净化.ppt
11气态污染物的净化重点、难点11.1吸收净化一、气态污染物净化过程的特点(1)气体在液体中的溶解度气体的溶解度是在100Kg水中溶解气体的千克数物理吸收三、吸收剂的选择四、吸收设备(三)喷雾塔气体在设备内与液体接触,主要有普通喷雾塔以及文丘里除尘器和冷却器使用,但吸收效率较低。(四)湍球塔以轻质小球作为气液接触的媒体,轻质小球放置在筛板上。它处理气量大,设备体积小,但小球磨损严重。11.2吸附法一、吸附的分类及其原理二、吸附剂三、吸附操作的因素四、吸附剂的再生五、常用的吸附设备11.3催化转化法一、催化
