
中考化学总复习 第5单元 科学探究 第15讲 物质的检验和鉴别、分离和提纯试题(pdf) 试题.pdf

Jo****34



在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

中考化学总复习 第5单元 科学探究 第15讲 物质的检验和鉴别、分离和提纯试题(pdf) 试题.pdf
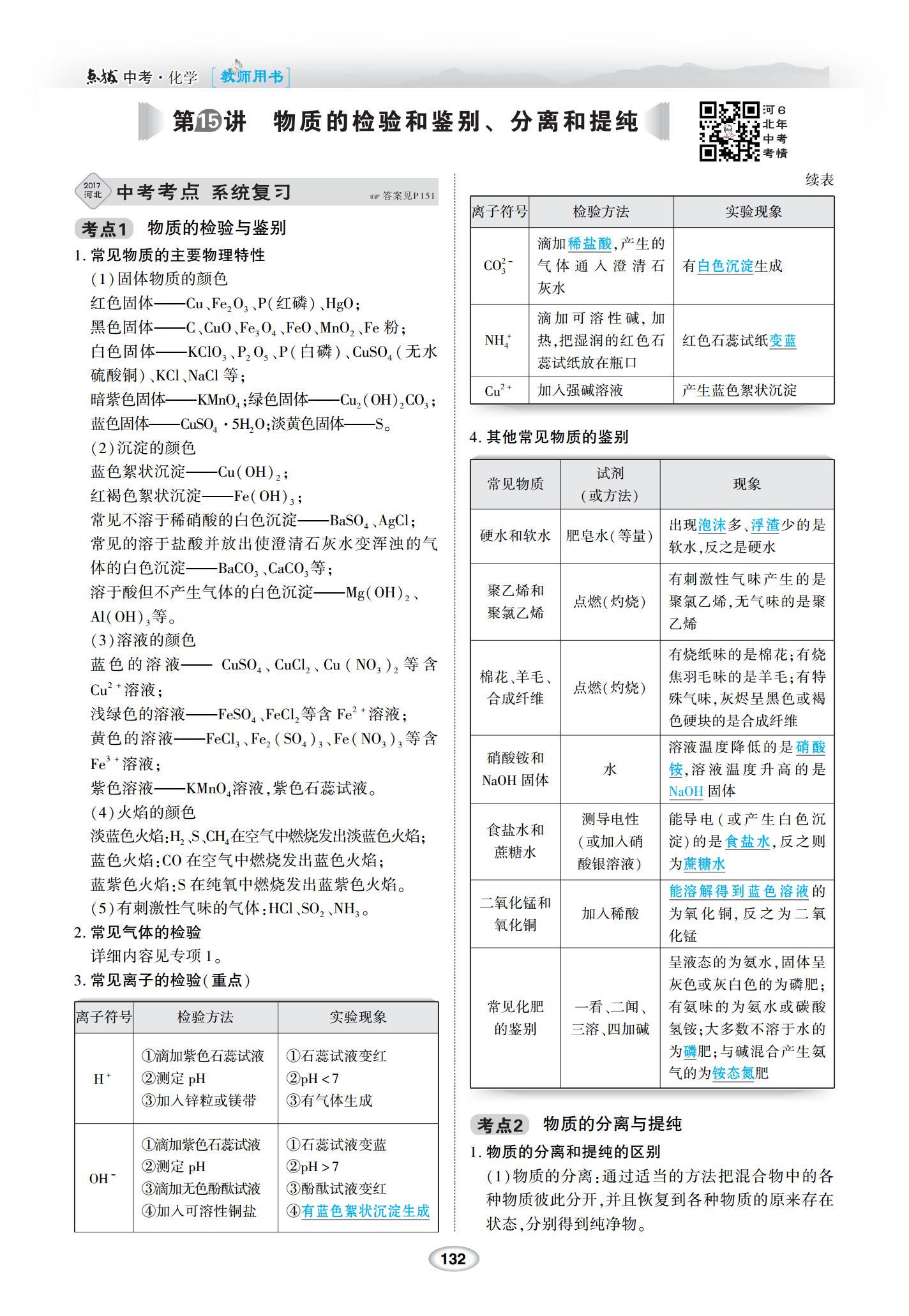
化学教师用书[]ઋઋ续表ઋઋ离子符号检验方法实验现象ઋ物质的检验与鉴别ઋઋ滴加稀盐酸产生的常见物质的主要物理特性ઋꎬ1.ઋ2-气体通入澄清石有白色沉淀生成3固体物质的颜色ઋCO(1)ઋ灰水红色固体红磷ઋ———Cu、Fe2O3、P()、HgOꎻઋ滴加可溶性碱加黑色固体粉ઋꎬ342———C、CuO、FeO、FeO、MnO、Feꎻઋ+热把湿润的红色石红色石蕊试纸变蓝4白色固体白磷无水ઋNHꎬ3254———KClO、PO、P()、CuSO(ઋ蕊试纸放在瓶口硫酸铜等ઋ)、KCl、NaClꎻઋ2+加入强碱溶液产生蓝色
试题-全国-2017_(河北专版)2017年中考化学总复习 第5单元 科学探究 第15讲 物质的检验和鉴别、分离和提纯试题(pdf).pdf
化学教师用书[]续表离子符号检验方法实验现象物质的检验与鉴别滴加稀盐酸产生的常见物质的主要物理特性ꎬ1.2-气体通入澄清石有白色沉淀生成3固体物质的颜色CO(1)灰水红色固体红磷———Cu、Fe2O3、P()、HgOꎻ滴加可溶性碱加黑色固体粉ꎬ342———C、CuO、FeO、FeO、MnO、Feꎻ+热把湿润的红色石红色石蕊试纸变蓝4白色固体白磷无水NHꎬ3254———KClO、PO、P()、CuSO(

课件-全国-2017_(河北专版)2017年中考化学总复习 第5单元 科学探究 第15讲 物质的检验和鉴别、分离和提纯课件.ppt
考点2第1讲(2)沉淀的颜色蓝色絮状沉淀——Cu(OH)2;红褐色絮状沉淀——Fe(OH)3;常见不溶于稀硝酸的白色沉淀——BaSO4、AgCl;常见的溶于盐酸并放出使澄清石灰水变浑浊的气体的白色沉淀——BaCO3、CaCO3等;溶于酸但不产生气体的白色沉淀——Mg(OH)2、Al(OH)3等。(3)溶液的颜色蓝色的溶液——CuSO4、CuCl2、Cu(NO3)2等含Cu2+溶液;浅绿色的溶液——FeSO4、FeCl2等含Fe2+溶液;黄色的溶液——FeCl3、Fe2(SO4)3、Fe(

(河北专版)中考化学总复习 第5单元 科学探究 第15讲 物质的检验和鉴别、分离和提纯课件-人教版初中九年级全册化学课件.ppt
考点2第1讲(2)沉淀的颜色蓝色絮状沉淀——Cu(OH)2;红褐色絮状沉淀——Fe(OH)3;常见不溶于稀硝酸的白色沉淀——BaSO4、AgCl;常见的溶于盐酸并放出使澄清石灰水变浑浊的气体的白色沉淀——BaCO3、CaCO3等;溶于酸但不产生气体的白色沉淀——Mg(OH)2、Al(OH)3等。(3)溶液的颜色蓝色的溶液——CuSO4、CuCl2、Cu(NO3)2等含Cu2+溶液;浅绿色的溶液——FeSO4、FeCl2等含Fe2+溶液;黄色的溶液——FeCl3、Fe2(SO4)3、Fe(NO3)

(河北专版)中考化学总复习 第5单元 科学探究 第15讲 物质的检验和鉴别、分离和提纯课件-人教版初中九年级全册化学课件.ppt
考点2第1讲(2)沉淀的颜色蓝色絮状沉淀——Cu(OH)2;红褐色絮状沉淀——Fe(OH)3;常见不溶于稀硝酸的白色沉淀——BaSO4、AgCl;常见的溶于盐酸并放出使澄清石灰水变浑浊的气体的白色沉淀——BaCO3、CaCO3等;溶于酸但不产生气体的白色沉淀——Mg(OH)2、Al(OH)3等。(3)溶液的颜色蓝色的溶液——CuSO4、CuCl2、Cu(NO3)2等含Cu2+溶液;浅绿色的溶液——FeSO4、FeCl2等含Fe2+溶液;黄色的溶液——FeCl3、Fe2(SO4)3、Fe(NO3)
