
试题-全国-2009_九年级化学溶液总复习人教实验版.rar

是你****盟主





在线预览结束,喜欢就下载吧,查找使用更方便
相关资料

试题-全国-2009_九年级化学溶液总复习人教实验版.rar
用心爱心专心九年级化学溶液总复习人教实验版一、一周知识概述在本周我们全面复习:溶液这一章,内容包括:溶液的形成、深解度、溶质质量分数。二、重点知识归纳及讲解(一)、溶液1、溶液、乳浊液、悬浊液溶液:由溶质和溶剂组成的均一、稳定的混合物;乳浊液:由小液滴分散在液体里形成的混合物;悬浊液:不溶于水的固体小颗粒分散在液体里形成的混合物。2、饱和溶液、不饱和溶液(1)概念:饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时所得到的溶液,叫做这种溶质的饱和溶液。不饱和溶液:在一定温度下,向一定

试题-全国-2009_初中语文总复习人教实验版.rar
初中语文总复习一、复习计划一年一度的中考即将来临,中考语文总复习承担着系统梳理、归纳总结、稳步提高的重任。针对中考语文复习时间短、任务重、范围广、内容多、要求高的特点,如何在短短的几个月内对中学语文进行深入复习,全面提高成绩?这要求我们必须有一定的复习技巧和全面的复习计划。中考语文总复习,是以巩固初中阶段所学语文知识,并重新组合知识系统,有序地进行语文知识及技能训练,提高应用、迁移知识以解决实际问题的能力为目的。如今的应试能力都是建立在扎实的基础、良好的素质之上的。在这样的背景中,我们应当用现代教育理论来

九年级化学溶液总复习人教实验版.doc
九年级化学溶液总复习人教实验版一、一周知识概述在本周我们全面复习:溶液这一章,内容包括:溶液的形成、深解度、溶质质量分数。二、重点知识归纳及讲解(一)、溶液1、溶液、乳浊液、悬浊液溶液:由溶质和溶剂组成的均一、稳定的混合物;乳浊液:由小液滴分散在液体里形成的混合物;悬浊液:不溶于水的固体小颗粒分散在液体里形成的混合物。2、饱和溶液、不饱和溶液(1)概念:饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时所得到的溶液,叫做这种溶质的饱和溶液。不饱和溶液:在一定温度下,向一定量溶剂里加入

试题-全国-2009_九年级化学总复习:化学实验(一)人教实验版知识精讲.rar
用心爱心专心九年级化学总复习:化学实验(一)人教实验版【本讲教育信息】一.教学内容:总复习:化学实验(一)二.重点、难点:1.知道常用的化学实验仪器试管、滴管、酒精灯、烧杯、量筒、集气瓶、漏斗、长颈漏斗、托盘天平、玻璃棒等的名称、性质、用途。2.知道常见药品的保存和使用,实验室安全常识和环保常识。3.学会固体、液体药品的取用,药品的称量,酒精灯的使用与加热,仪器的洗涤,仪器的连接与装配,溶液的配制,装置气密性的检查,溶解、过滤、蒸发等一些重要的实验基本操作。4.学会氧气、
试题-全国-2009_九年级化学总复习:化学实验(二)人教实验版知识精讲.rar
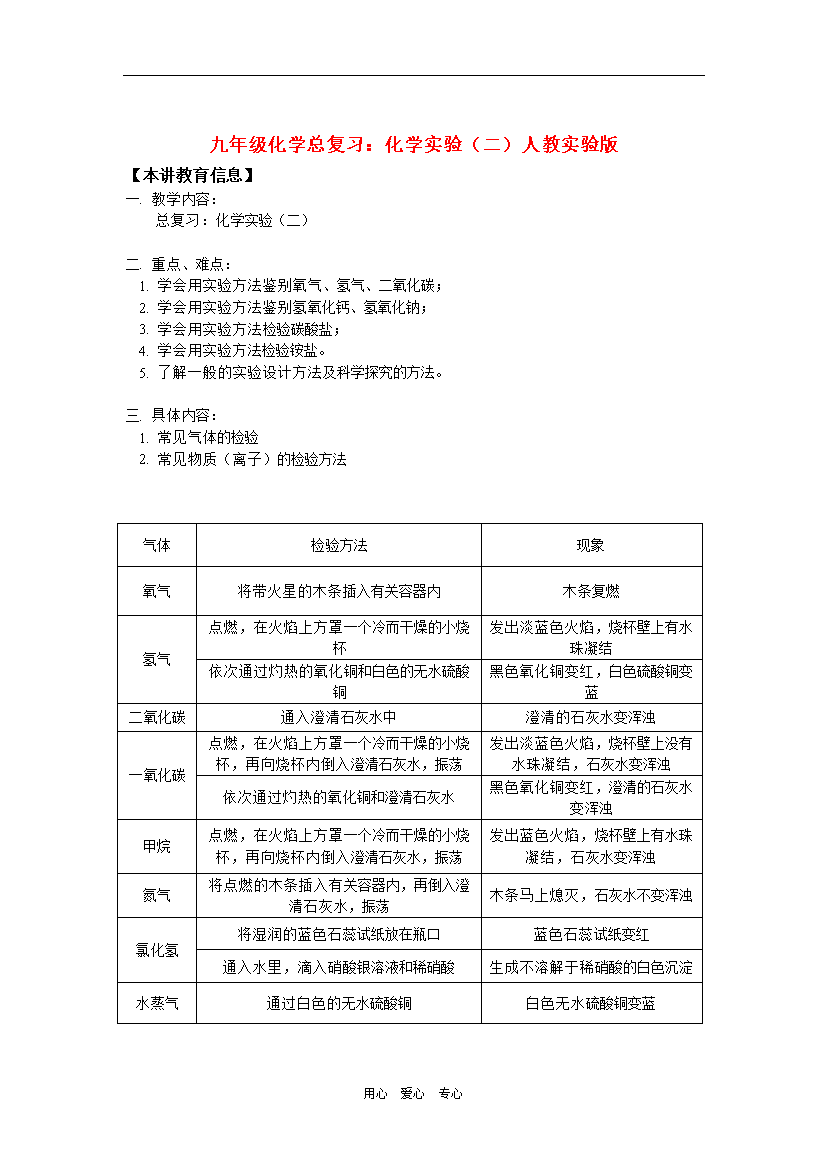
用心爱心专心九年级化学总复习:化学实验(二)人教实验版【本讲教育信息】一.教学内容:总复习:化学实验(二)二.重点、难点:1.学会用实验方法鉴别氧气、氢气、二氧化碳;2.学会用实验方法鉴别氢氧化钙、氢氧化钠;3.学会用实验方法检验碳酸盐;4.学会用实验方法检验铵盐。5.了解一般的实验设计方法及科学探究的方法。三.具体内容:1.常见气体的检验气体检验方法现象氧气将带火星的木条插入有关容器内木条复燃氢气点燃,在火焰上方罩一个冷而干燥的小烧杯发出淡蓝色火焰,烧杯壁上有
