
氢氧化铝沉淀图像ppt课件.ppt

lj****88



亲,该文档总共31页,到这已经超出免费预览范围,如果喜欢就直接下载吧~
相关资料

氢氧化铝沉淀图像ppt课件.ppt
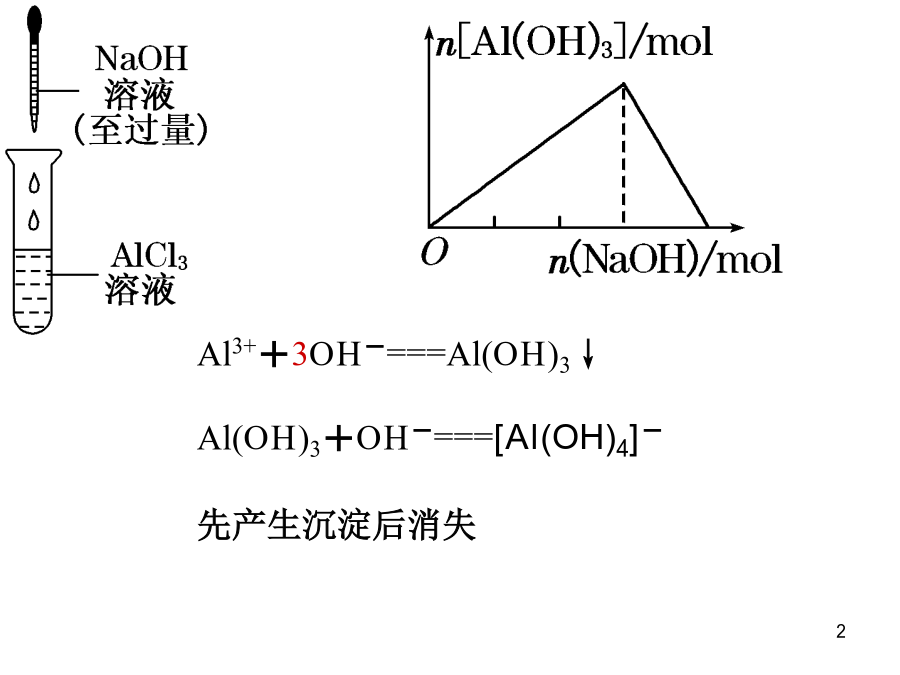
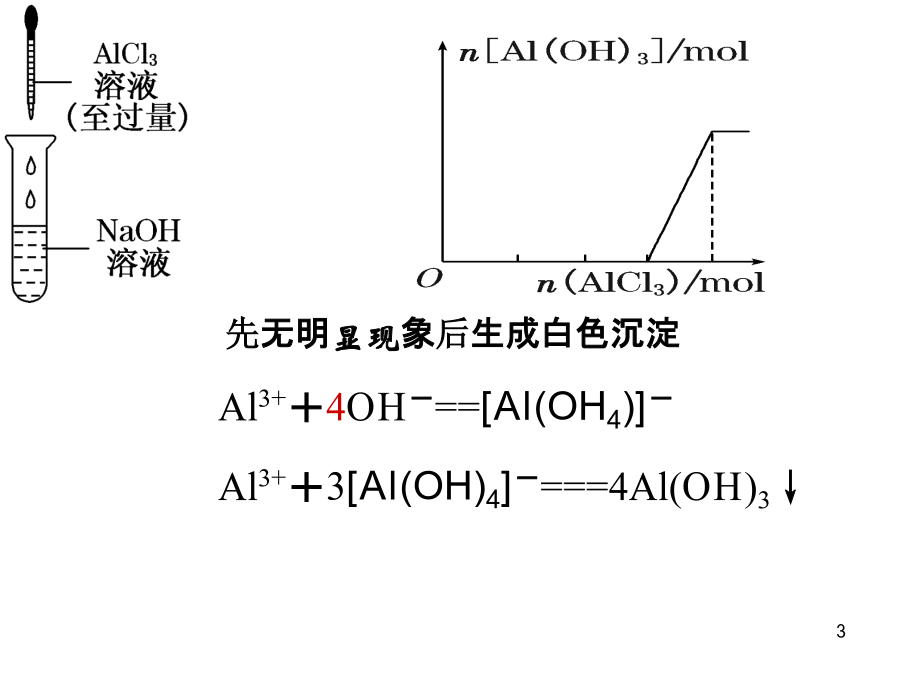
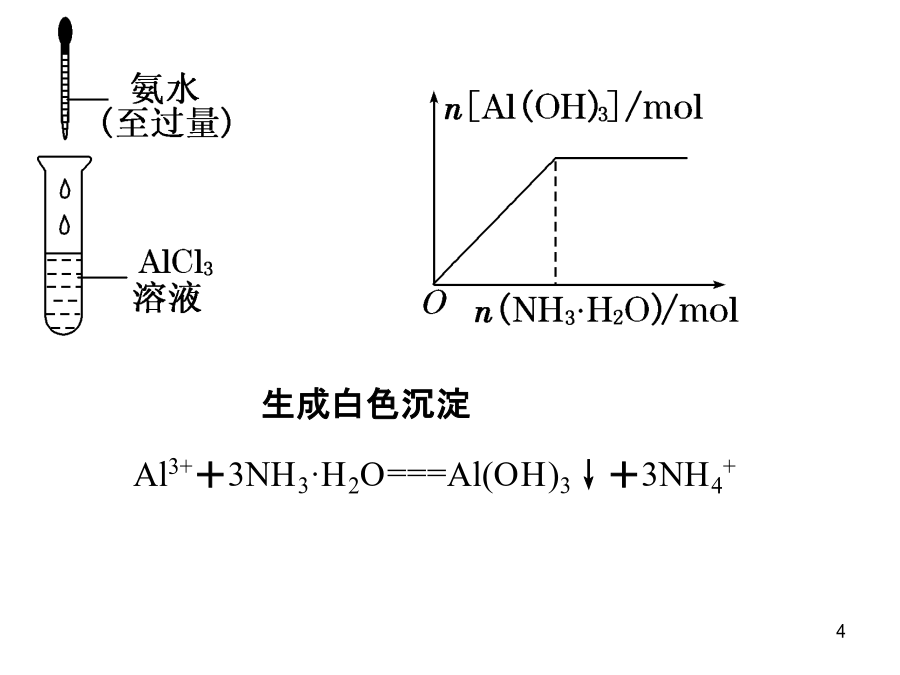
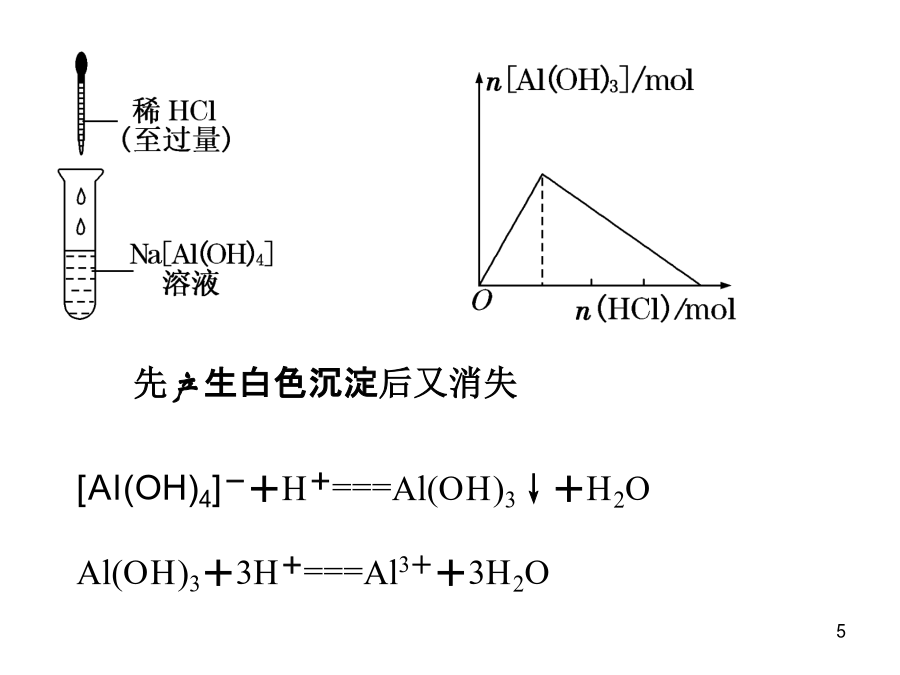
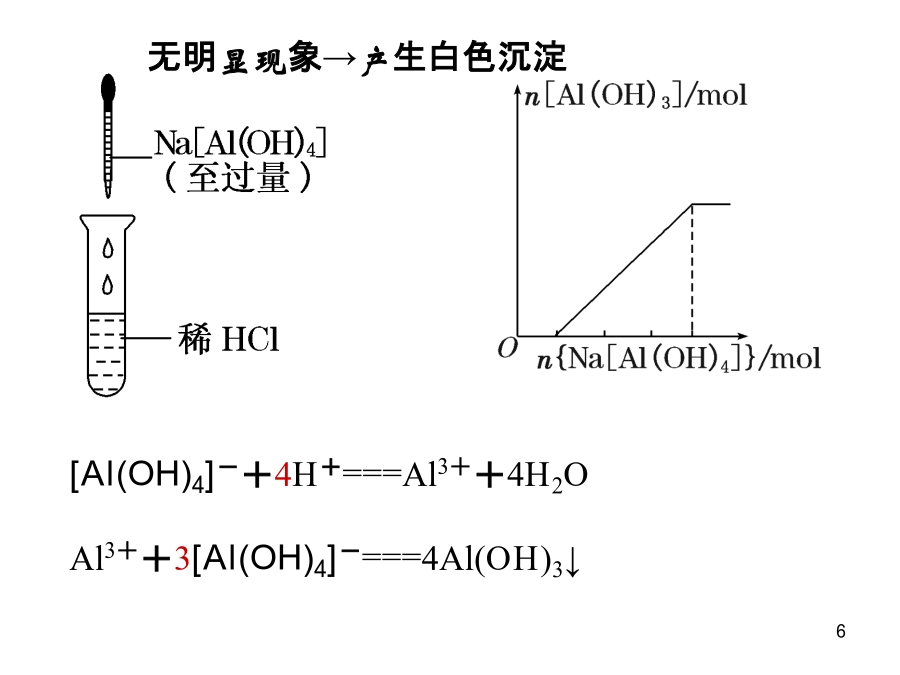
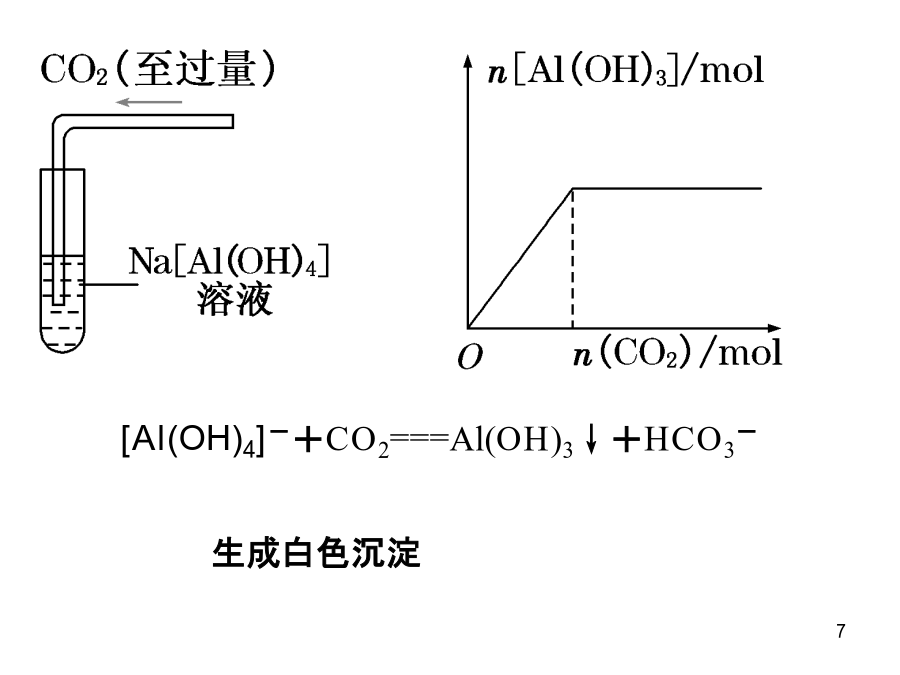
有关AI(OH)3生成与溶解的图像分析Al3++3OH-===Al(OH)3↓Al(OH)3+OH-===[Al(OH)4]-先产生沉淀后消失Al3++4OH-==[Al(OH4)]-Al3++3[Al(OH)4]-===4Al(OH)3↓Al3++3NH3·H2O===Al(OH)3↓+3NH4+先产生白色沉淀后又消失[Al(OH)4]-+4H+===Al3++4H2OAl3++3[Al(OH)4]-===4Al(OH)3↓[Al(OH)4]-+CO2===Al(OH)3↓+HCO3-重要提示(1)Na

氢氧化铝沉淀图像ppt.pptx
氢氧化铝沉淀图像Al3++3OH-===Al(OH)3↓Al(OH)3+OH-===[Al(OH)4]-先产生沉淀后消失Al3++4OH-==[Al(OH4)]-Al3++3[Al(OH)4]-===4Al(OH)3↓Al3++3NH3·H2O===Al(OH)3↓+3NH4+先产生白色沉淀后又消失[Al(OH)4]-+4H+===Al3++4H2OAl3++3[Al(OH)4]-===4Al(OH)3↓[Al(OH)4]-+CO2===Al(OH)3↓+HCO3-重要提示(1)NaOH溶液与AlCl3溶

氢氧化铝沉淀图像分析.ppt
探究“铝三角”中的图像问题科学探究1:向AlCl3溶液中逐滴加入NaOH溶液至过量向AlCl3溶液中滴加NaOH溶液科学探究2:向NaOH溶液里逐滴加入AlCl3溶液至过量科学探究3:向NaAlO2溶液中逐滴加入盐酸至过量科学探究4:向稀盐酸中逐滴加入NaAlO2溶液至过量科学探究5:向AlCl3溶液中逐滴加入氨水溶液

氢氧化铝沉淀图像学习资料.pptx
会计学Al3++3OH-===Al(OH)3↓Al(OH)3+OH-===[Al(OH)4]-先产生沉淀后消失Al3++4OH-==[Al(OH4)]-Al3++3[Al(OH)4]-===4Al(OH)3↓Al3++3NH3·H2O===Al(OH)3↓+3NH4+先产生白色沉淀后又消失[Al(OH)4]-+4H+===Al3++4H2OAl3++3[Al(OH)4]-===4Al(OH)3↓[Al(OH)4]-+CO2===Al(OH)3↓+HCO3-重要提示(1)NaOH溶液和AlCl3溶液滴加顺序

有关氢氧化铝沉淀的图像分析.ppt
有关氢氧化铝沉淀的图像分析
